1 . 已知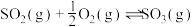 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:

(1)由图可知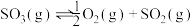 为
为_______ (填“吸热”或“放热”)反应。
(2)E所代表的能量是_______ ;E的大小对该反应的反应热_______ (填“有”或“无”)影响。
(3)请求出反应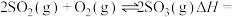
_______  。
。
(4)又知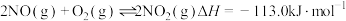 ,请根据题给条件求出反应
,请根据题给条件求出反应 的焓变
的焓变
_______  。
。
(5)25℃、101kP时,11g丙烷( )完全燃烧生成
)完全燃烧生成 和液态水时放出的热量是555.0kJ,则表示丙烷燃烧热的热化学方程式是
和液态水时放出的热量是555.0kJ,则表示丙烷燃烧热的热化学方程式是_______ 。
(6)已知:
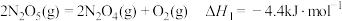 ①
①
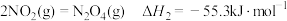 ②
②
则反应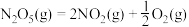 的
的
_______  。
。
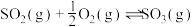 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
(1)由图可知
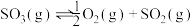 为
为(2)E所代表的能量是
(3)请求出反应
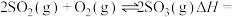
 。
。(4)又知
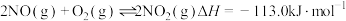 ,请根据题给条件求出反应
,请根据题给条件求出反应 的焓变
的焓变
 。
。(5)25℃、101kP时,11g丙烷(
 )完全燃烧生成
)完全燃烧生成 和液态水时放出的热量是555.0kJ,则表示丙烷燃烧热的热化学方程式是
和液态水时放出的热量是555.0kJ,则表示丙烷燃烧热的热化学方程式是(6)已知:
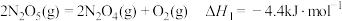 ①
①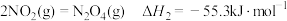 ②
②则反应
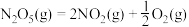 的
的
 。
。
您最近一年使用:0次
2023高三·全国·专题练习
2 . 化学反应都伴随着能量的变化。回答下列问题:
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
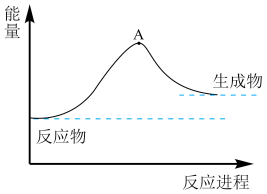
(2)一种分解海水制氢气的方法为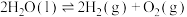 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将_______ (填“升高”、“降低”或“不变”)。
(3)已知: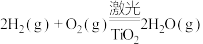
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:
由此计算x=___________ 。(用含a、c、d的代数式表示)
(1)可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是___________(填字母)。
A. | B. |
C. | D.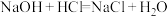 |
(2)一种分解海水制氢气的方法为
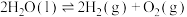 。如图为该反应的能量变化示意图,使用催化剂
。如图为该反应的能量变化示意图,使用催化剂 后,图中A点将
后,图中A点将
(3)已知:
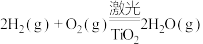
 ,部分化学键的键能数据如表:
,部分化学键的键能数据如表:| 化学键 |  |  |  |
 | x | c | d |
您最近一年使用:0次
名校
3 . 回答下列问题:
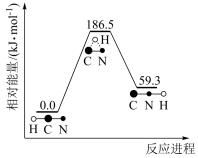
(1)理论研究表明,在101kPa和298K下,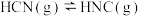 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
(2)已知共价键的健能与热化学方程式信息如下表:
则 的
的 为
为
(1)理论研究表明,在101kPa和298K下,
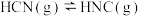 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
| A.HCN比HNC稳定 | B.该异构化反应的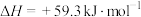 |
| C.正反应与逆反应的活化能相等 | D.使用催化剂,可以改变反应的反应热 |
(2)已知共价键的健能与热化学方程式信息如下表:
| 共价键 | H-H | H-O |
键能/( ) ) | 436 | 463 |
| 热化学方程式 |   | |
 的
的 为
为 A.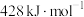 | B.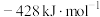 | C.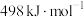 | D.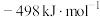 |
您最近一年使用:0次
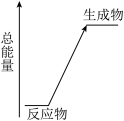
4 . 化学反应同时伴随着能量变化,是人类获取能量的重要途径。以下是常见的化学反应。
A.镁与盐酸的反应
B.氢氧化钠与盐酸的反应
C.盐酸与碳酸氢钠的反应
D.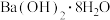 晶体与
晶体与 晶体的反应
晶体的反应
(1)以上化学反应中能用上图表示其能量变化的是_____ (填标号),此类反应中有能量变化的原因是:断开反应物中的化学键需吸收的总能量_____ (填“大于”或“小于”)形成生成物中的化学键需释放的总能量。
(2)从以上反应中选择一个反应设计成如图装置的原电池。
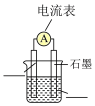
①将图中原电池装置补充完整_____ 。
②证实化学能转化为电能的实验现象是_____ (写出两种)。
③正极的电极反应式是_____ 。
④溶液中的_____ (填溶质电离出的离子的符号)向负极方向移动。

A.镁与盐酸的反应
B.氢氧化钠与盐酸的反应
C.盐酸与碳酸氢钠的反应
D.
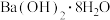 晶体与
晶体与 晶体的反应
晶体的反应(1)以上化学反应中能用上图表示其能量变化的是
(2)从以上反应中选择一个反应设计成如图装置的原电池。

①将图中原电池装置补充完整
②证实化学能转化为电能的实验现象是
③正极的电极反应式是
④溶液中的
您最近一年使用:0次
名校
解题方法
5 . 完成下列问题。
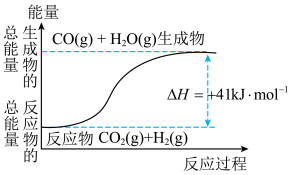
(1)根据如图所示情况,判断下列说法中正确的是___________。
(2)已知反应: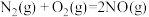

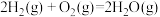

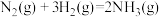

利用上述三个反应,计算 的反应焓变
的反应焓变 为
为___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(3)已知反应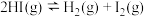 的
的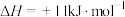 ,
, 、
、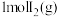 分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则
分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则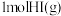 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为___________ kJ。
(1)根据如图所示情况,判断下列说法中正确的是___________。

A.其热化学方程式为:  |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
D.若当 为液态时反应热为 为液态时反应热为 ,则 ,则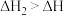 |
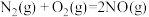

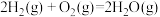

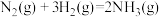

利用上述三个反应,计算
 的反应焓变
的反应焓变 为
为 、
、 、
、 的式子表示)。
的式子表示)。(3)已知反应
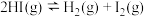 的
的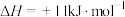 ,
, 、
、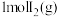 分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则
分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则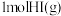 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为
您最近一年使用:0次
6 . 回答下列问题:
(1)已知工业上采用高温煅烧石灰石的方法来制备CO2,其反应的化学方程式为_______ ;该反应是_______ (填“吸热”或“放热”)反应。
已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)=CH2=CH2(g)+4H2O(g) ΔH
(2)几种物质的能量(kJ·mol-1)如表所示(在25 ℃、101 kPa条件下,规定单质的能量为0,测得其他物质生成时的反应热为其具有的能量):
则该反应的ΔH=_______ kJ·mol-1。
(3)几种化学键的键能(kJ·mol-1)如表所示:
a=_______ 。
(1)已知工业上采用高温煅烧石灰石的方法来制备CO2,其反应的化学方程式为
已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)=CH2=CH2(g)+4H2O(g) ΔH
(2)几种物质的能量(kJ·mol-1)如表所示(在25 ℃、101 kPa条件下,规定单质的能量为0,测得其他物质生成时的反应热为其具有的能量):
| 物质 | CO2(g) | H2(g) | CH2=CH2(g) | H2O(g) |
| 能量/(kJ·mol-1) | -394 | 0 | 52 | -242 |
(3)几种化学键的键能(kJ·mol-1)如表所示:
| 化学键 | C=O | H—H | C=C | C—H | H—O |
| 能量/(kJ·mol-1) | 803 | 436 | 615 | a | 463 |
您最近一年使用:0次
7 . 吸热反应、放热反应
(1)放热反应:释放热量的化学反应,反应物的总能量_______ 生成物的总能量,反应体系的能量_______ ,故
_______ 0,即 为
为_______ 。
(2)吸热反应:吸收热量的化学反应,反应物的总能量_______ 生成物的总能量,反应体系的能量_______ ,故
_______ 0,即 为
为_______ 。
(3)常见的吸热反应和放热反应
(1)放热反应:释放热量的化学反应,反应物的总能量

 为
为(2)吸热反应:吸收热量的化学反应,反应物的总能量

 为
为(3)常见的吸热反应和放热反应
吸热反应( ) ) | 放热反应(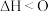 ) ) |
① 与 与 的反应 的反应②大多数的分解反应 ③弱电解质的电离 ④盐类水解 ⑤C和  )、C和 )、C和 的反应 的反应 | ①中和反应 ②燃烧反应 ③金属与酸或氧气的反应 ④铝热反应 ⑤酸性氧化物或碱性氧化物与水的反应 ⑥大多数的化合反应 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 .  和
和 是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ:
是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ: 。
。
(1)汽车行驶时, 和
和 在电火花作用下产生
在电火花作用下产生 ,各物质所含化学键键能数据如下表:
,各物质所含化学键键能数据如下表:
相同条件下, 、
、 、
、 三种物质中最稳定的是
三种物质中最稳定的是_______ ;
_______ 。
(2)工业上可通过 和
和 化合制备甲醇,反应的化学方程式为
化合制备甲醇,反应的化学方程式为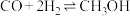 。
。
已知:①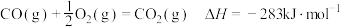
②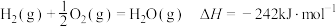
③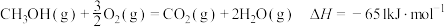
写出工业上用 和
和 合成
合成 的热化学方程式:
的热化学方程式:_______ 。
(3)反应I在常温下可以自发进行,则该反应的正反应为_______ (填“吸热”或“放热”)反应。
(4)为减少汽车尾气污染,下列措施合理的有_______(填字母)。
 和
和 是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ:
是汽车尾气的主要成分,它们能缓慢地发生反应Ⅰ: 。
。(1)汽车行驶时,
 和
和 在电火花作用下产生
在电火花作用下产生 ,各物质所含化学键键能数据如下表:
,各物质所含化学键键能数据如下表:| 物质 |  |  |  |
化学键键能 | 946 | 498 | 632 |
 、
、 、
、 三种物质中最稳定的是
三种物质中最稳定的是
(2)工业上可通过
 和
和 化合制备甲醇,反应的化学方程式为
化合制备甲醇,反应的化学方程式为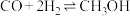 。
。已知:①
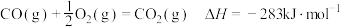
②
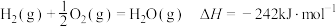
③
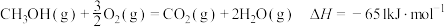
写出工业上用
 和
和 合成
合成 的热化学方程式:
的热化学方程式:(3)反应I在常温下可以自发进行,则该反应的正反应为
(4)为减少汽车尾气污染,下列措施合理的有_______(填字母)。
| A.开发氢能源 | B.寻找反应I的高效催化剂 |
| C.市民大量移居城市郊区 | D.戴上呼吸面具 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 .  与
与 经催化重整,制得合成气:
经催化重整,制得合成气: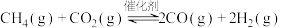 ,已知上述反应中相关的化学键键能数据如下:
,已知上述反应中相关的化学键键能数据如下:
则该反应的
_______ 。分别在 恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入
恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入 和
和 各
各 的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______ (填“A”或“B”)。
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: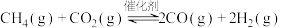 ,已知上述反应中相关的化学键键能数据如下:
,已知上述反应中相关的化学键键能数据如下:| 化学键 |  |  |  | 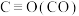 |
键能 | 413 | 745 | 436 | 1075 |

 恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入
恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入 和
和 各
各 的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
您最近一年使用:0次



