2023高三·全国·专题练习
1 . 铋基催化剂对 电化学还原制取
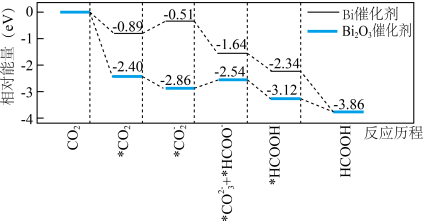
电化学还原制取 具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
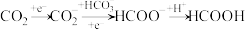
(1)使用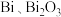 两种催化剂哪个更有利于
两种催化剂哪个更有利于 的吸附?
的吸附?_______ 。简述判断依据:_______ 。
(2) 电化学还原制取
电化学还原制取 的反应
的反应
_______ 0。
(3)使用 催化剂时,最大能垒是
催化剂时,最大能垒是_______ ,使用 催化剂时,最大能垒是
催化剂时,最大能垒是_______ 。
(4)由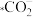 生成
生成 的反应为
的反应为_______ 。
 电化学还原制取
电化学还原制取 具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。
具有高效的选择性。其反应历程与能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。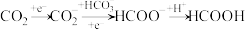

(1)使用
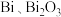 两种催化剂哪个更有利于
两种催化剂哪个更有利于 的吸附?
的吸附?(2)
 电化学还原制取
电化学还原制取 的反应
的反应
(3)使用
 催化剂时,最大能垒是
催化剂时,最大能垒是 催化剂时,最大能垒是
催化剂时,最大能垒是(4)由
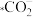 生成
生成 的反应为
的反应为
您最近一年使用:0次
解题方法
2 . 常见化学反应的分类
| 化学反应 | 按反应物、生成物种类及数目多少 | |
| 按反应中 | 离子反应 | |
| 非离子反应 | ||
| 按反应中 | 氧化还原反应 | |
| 非氧化还原反应 | ||
| 按反应进行的程度和方向 | ||
| 按反应的能量变化 | ||
您最近一年使用:0次
3 . CO、CO2的回收和综合利用有利于实现“碳中和”。
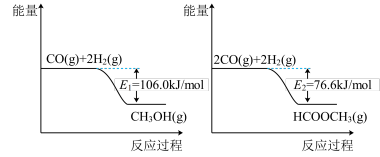
(1)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算2CH3OH(g) HCOOCH3(g)+2H2(g)ΔH=
HCOOCH3(g)+2H2(g)ΔH=_______ 。
已知键能数据如下表。
则C O的键能为
O的键能为 _______ 。
(2)已知:反应1:2CO(g)+4H2(g)═CH3CH2OH(g)+H2O(g)ΔH=-128.8kJ⋅mol﹣1
反应2:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)ΔH=-78.1kJ⋅mol﹣1
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是 _______(填字母)。
(3)CO2催化加氢制甲醇可分两步完成,反应历程如图所示。已知CO(g)+2H2(g)═CH3OH(g)ΔH=-106kJ⋅mol﹣1,则CO2(g)+3H2(g)═CH3OH(g)+H2O(g)ΔH=_______ 。
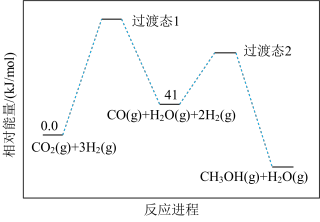
该反应进程中总反应速率由第_______ (“1”或“2”)步决定。
(1)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算2CH3OH(g)
 HCOOCH3(g)+2H2(g)ΔH=
HCOOCH3(g)+2H2(g)ΔH=
已知键能数据如下表。
| 化学键 | H﹣H | C﹣O | C O O | H﹣O | C﹣H |
| 键能/(kJ⋅mol﹣1) | 436 | 326 | a | 464 | 414 |
 O的键能为
O的键能为 (2)已知:反应1:2CO(g)+4H2(g)═CH3CH2OH(g)+H2O(g)ΔH=-128.8kJ⋅mol﹣1
反应2:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)ΔH=-78.1kJ⋅mol﹣1
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是 _______(填字母)。
A.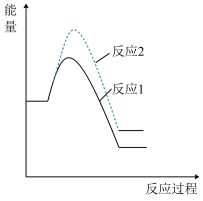 | B. |
C.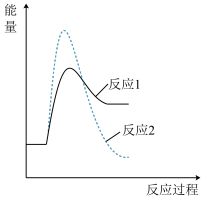 | D.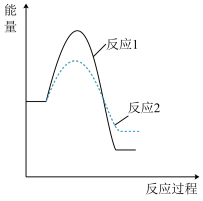 |

该反应进程中总反应速率由第
您最近一年使用:0次
2022-11-28更新
|
199次组卷
|
2卷引用:河南省宋基信阳实验中学2022-2023学年高三上学期11月月考化学试题
4 . 已知:Ⅰ.环丁烯( )的结构简式可表示为
)的结构简式可表示为 。
。
Ⅱ.苯(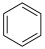 )、环已二烯(
)、环已二烯(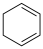 )和环己烯(
)和环己烯(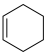 )相对
)相对 的能量如图所示:
的能量如图所示:
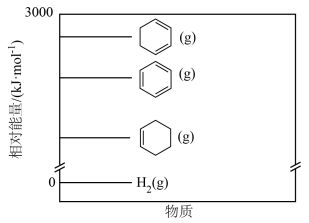
回答下列问题:
(1)苯的一种不含不饱和键的同分异构体的结构简式为_______ 。
(2)1 mol环已二烯(g)与1 mol氢气(g)的加成反应属于_______ (填“吸热”或“放热”)反应。
(3)T℃下,在恒容密闭容器中加入
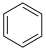 (g)和
(g)和 ,发生反应:
,发生反应: (g)
(g)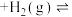
 (g)和
(g)和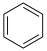 (g)
(g)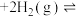
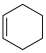 (g),若达到平衡后,苯、环已二烯和环己烯的物质的量相同。则:
(g),若达到平衡后,苯、环已二烯和环己烯的物质的量相同。则:
①苯的平衡转化率是_______ (保留三位有效数字);平衡时 的体积分数是
的体积分数是_______ 。
②升高温度,苯的消耗速率_______ (填“增大”“减小”或“不变”,下同),苯的生成速率_______ 。
 )的结构简式可表示为
)的结构简式可表示为 。
。Ⅱ.苯(
 )、环已二烯(
)、环已二烯( )和环己烯(
)和环己烯( )相对
)相对 的能量如图所示:
的能量如图所示:
回答下列问题:
(1)苯的一种不含不饱和键的同分异构体的结构简式为
(2)1 mol环已二烯(g)与1 mol氢气(g)的加成反应属于
(3)T℃下,在恒容密闭容器中加入

 (g)和
(g)和 ,发生反应:
,发生反应: (g)
(g)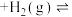
 (g)和
(g)和 (g)
(g)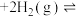
 (g),若达到平衡后,苯、环已二烯和环己烯的物质的量相同。则:
(g),若达到平衡后,苯、环已二烯和环己烯的物质的量相同。则:①苯的平衡转化率是
 的体积分数是
的体积分数是②升高温度,苯的消耗速率
您最近一年使用:0次
5 . 汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
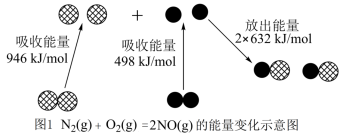
(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会____ (选填“吸收”或“放出”)____ kJ的能量。
(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g) 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①反应进行到10s时,正反应速率____ 逆反应速率(选填“>”“<”或“=”),0~10s内用CO2表示的平均反应速率是____ mol/(L•s)。
②该条件下,NO的最大转化率为____ 。
③下列措施一定能增大该反应速率的是____ (填标号)。
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
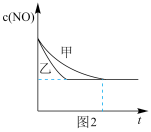
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂____ (选填“甲”或“乙”)的催化效果更好。
(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的____ 极(选填“正”或“负”),电极A的电极反应为____ 。

(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会

(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g)
 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
①反应进行到10s时,正反应速率
②该条件下,NO的最大转化率为
③下列措施一定能增大该反应速率的是
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂

(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的

您最近一年使用:0次
21-22高二·全国·课时练习
6 . 在金催化剂表面水煤气变换的反应历程如图所示,其中吸附在金催化剂表面的物种用*标注。

则水煤气变换反应的
___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)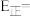
___________  ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:___________ 。

则水煤气变换反应的

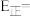
 ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:
您最近一年使用:0次
2022高一·上海·专题练习
7 . 对知识的归纳和总结是学好化学的重要方法。在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图所示),即氢氧化钙与图中四类物质能够发生化学反应。
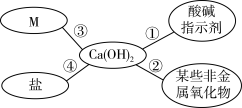
(1)图中M所属的物质类别是_______ 。
(2)氢氧化钙可由生石灰与水反应制得,该反应能_______ (填“吸收”或“放出”)热量。
(3)利用图中氢氧化钙能与_______ 反应的性质,可以解释“用石灰浆粉刷墙壁,干燥后墙面就变硬了”的现象。
(4)利用图中④氢氧化钙与盐反应的性质中,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该反应的化学方程式_______ 。

(1)图中M所属的物质类别是
(2)氢氧化钙可由生石灰与水反应制得,该反应能
(3)利用图中氢氧化钙能与
(4)利用图中④氢氧化钙与盐反应的性质中,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该反应的化学方程式
您最近一年使用:0次
8 . 回答下列问题:
(1)生石灰和氢氧化钠固体溶于水放热,而硝酸铵溶于水吸热。氢氧化钠固体溶于水放热的原因是_______ 。
(2)热胀冷缩是自然界的普遍现象,但当温度由0℃上升至4℃时,水的密度却增大,主要原因是_______ 。
(1)生石灰和氢氧化钠固体溶于水放热,而硝酸铵溶于水吸热。氢氧化钠固体溶于水放热的原因是
(2)热胀冷缩是自然界的普遍现象,但当温度由0℃上升至4℃时,水的密度却增大,主要原因是
您最近一年使用:0次
9 . 以CO2生产甲醇(CH3OH)是实现“碳中和”的重要途径。其原理是CO2(g) + 3H2(g) CH3OH(g) + H2O(g)。
CH3OH(g) + H2O(g)。
(1)该反应的能量变化如图所示,该反应为_______ (填“放热”或“吸热”)反应。
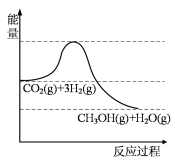
(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_______。
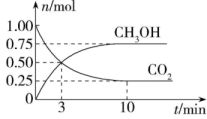
(3)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2、CH3OH的物质的量随时间变化如图。从反应开始到3 min末,用H2浓度变化表示的平均反应速率v(H2)=_______ ;反应达到平衡状态,此时H2的转化率为_______ 。
(4)在相同温度、容积不变的条件下,不能 说明该反应已达平衡状态的是_______。
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图。
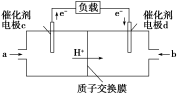
①则电极c是_______ (填“正极” 或“负极”),电极d的电极反应式_______ 。
②若线路中转移1 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。
 CH3OH(g) + H2O(g)。
CH3OH(g) + H2O(g)。(1)该反应的能量变化如图所示,该反应为
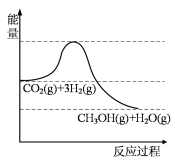
(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_______。
| A.升高温度 | B.充入He | C.加入合适的催化剂 | D.降低压强 |

(4)在相同温度、容积不变的条件下,
| A.CO2、H2的浓度均不再变化 |
| B.体系压强不变 |
| C.n(CH3OH)∶n(H2O)=1∶1 |
| D.H2的消耗速率与CH3OH的生成速率之比为3∶1 |

①则电极c是
②若线路中转移1 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
2022-04-22更新
|
664次组卷
|
3卷引用:福建省福州第十五中学2022-2023学年高三上学期11月线上限时训练化学试题
10 . 2022年北京冬奥会的火炬“飞扬”是世界首款高压储氢火炬,它运用了液体火箭发动机的氢能技术。由氨气制取氢气是一种新工艺,氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气制取氢气。
方法I:氨热分解法制氢气
(1)已知该反应为可逆反应,在一定温度下,利用催化剂将 分解为
分解为 和
和 的化学方程式为
的化学方程式为_______ 。
(2)该反应为吸热反应,说明反应物的总能量_______ 生成物的总能量(填“大于”“小于”或“等于”)。
(3)在一定温度和催化剂的条件下,向 容积固定的密闭容器中充入
容积固定的密闭容器中充入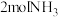 发生该反应,
发生该反应,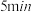 末测得容器中
末测得容器中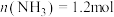 ,则在
,则在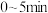 内,用
内,用 的浓度变化表示该反应的平均速率是:
的浓度变化表示该反应的平均速率是:
_______  。
。
(4)该反应达到化学平衡的标志是_______(填序号)。
方法II:氨电解法制氢气
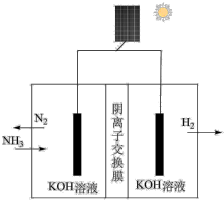
(5)利用电解原理,将氨转化为高纯氢气,其装置如图所示。装置中将太阳能转化为电能的电池,其主要材料是_______ 。装置中生成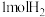 时,电路中通过
时,电路中通过_______  电子。为提高制取氢气的反应速率,可采取的方法是
电子。为提高制取氢气的反应速率,可采取的方法是_______ 。
方法I:氨热分解法制氢气
(1)已知该反应为可逆反应,在一定温度下,利用催化剂将
 分解为
分解为 和
和 的化学方程式为
的化学方程式为(2)该反应为吸热反应,说明反应物的总能量
(3)在一定温度和催化剂的条件下,向
 容积固定的密闭容器中充入
容积固定的密闭容器中充入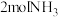 发生该反应,
发生该反应,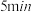 末测得容器中
末测得容器中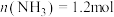 ,则在
,则在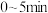 内,用
内,用 的浓度变化表示该反应的平均速率是:
的浓度变化表示该反应的平均速率是:
 。
。(4)该反应达到化学平衡的标志是_______(填序号)。
A. 的浓度为0 的浓度为0 | B. 的物质的量保持不变 的物质的量保持不变 |
| C.正反应速率与逆反应速率相等 | D. 的物质的量之比为 的物质的量之比为 |
方法II:氨电解法制氢气
(5)利用电解原理,将氨转化为高纯氢气,其装置如图所示。装置中将太阳能转化为电能的电池,其主要材料是
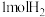 时,电路中通过
时,电路中通过 电子。为提高制取氢气的反应速率,可采取的方法是
电子。为提高制取氢气的反应速率,可采取的方法是
您最近一年使用:0次



