解题方法
1 . 氮及其化合物在生产、环保研究等方面用途非常广泛,回答下列问题:
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0kJ/mol
4NO(g)+2H2O(g)+3O2(g)=4HNO3(g) △H=_______ kJ/mol。
(2)FeSO4(aq)+NO(g)=Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是_______。(填标号)
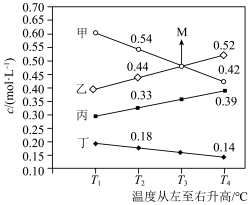
(3)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,各物质的浓度与温度关系如图所示。________ (填化学式),写出该反应的化学方程式:_____________ 。
②正反应△H______ (填“>”“<”或“=”)0,判断依据是__________ 。
③T3K时NH3的平衡转化率为__________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0kJ/mol
4NO(g)+2H2O(g)+3O2(g)=4HNO3(g) △H=
(2)FeSO4(aq)+NO(g)=Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是_______。(填标号)
| A.溶液颜色不变,反应达到平衡状态 |
| B.其他条件不变,充入少量O2,平衡不移动 |
| C.其他条件不变,加少量FeSO4,溶液颜色加深 |
| D.其他条件不变,微热,溶液颜色加深 |
(3)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,各物质的浓度与温度关系如图所示。
②正反应△H
③T3K时NH3的平衡转化率为
您最近一年使用:0次
2024-04-21更新
|
110次组卷
|
2卷引用:2024届青海省海东市高三下学期二模理科综合试卷-高中化学
解题方法
2 . 二甲醚可用于护发、护肤药品和涂料中作各类气雾推进剂。在制药、染料、农药等工业中有许多独特的用途。
(1)已知:CO(g)、H2(g)、CH3OCH3(g)的燃烧热ΔH分别为-283kJ·mol-1、-285.8kJ·mol-1、-1460kJ·mol-1,H2O(g)=H2O(l) ΔH1=-44 kJ·mol-1。则2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH2=_______ ,该反应能否自发进行与_______ 有关。
(2)T1 ℃时,在恒容密闭容器中通入CH3OCH3 ,发生反应CH3OCH3(g)⇌CO(g)+H2(g) +CH4(g) ,测得容器内初始压强为50kPa,反应过程中反应时间t与气体总压p总的关系如下表所示。
①该温度下,反应达到平衡时,CH3OCH3的分解率为_______ ;t=350s时,混合气体的平均摩尔质量为_______ (保留三位有效数字)g·mol-1。
②若反应达到平衡后,升高温度,CH3OCH3的浓度增大,则正反应为_______ (填“放热”或“吸热”)反应。
③该温度下,要缩短反应达到平衡所需的时间,可采取的措施是_______ 。
(3)在T2℃、p0kPa(恒温、恒压)下,将等物质的量的CO与H2通入容积为VL的容器内,发生反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)。反应达到平衡时,测得容器容积为0.6VL,用气体分压[气体分压(p)=气体总压(p总)×体积分数]代替平衡浓度表示的平衡常数Kp=_______ (kPa)-4。反应速率v=v正-v逆=k正p2(CO)·p4(H2)-k逆p(CH3OCH3)p(H2O),k正、k逆分别为正、逆反应速率常数,p为气体的分压。该温度下,当容器体积为0.8VL时, =
=_______ 。
(1)已知:CO(g)、H2(g)、CH3OCH3(g)的燃烧热ΔH分别为-283kJ·mol-1、-285.8kJ·mol-1、-1460kJ·mol-1,H2O(g)=H2O(l) ΔH1=-44 kJ·mol-1。则2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH2=
(2)T1 ℃时,在恒容密闭容器中通入CH3OCH3 ,发生反应CH3OCH3(g)⇌CO(g)+H2(g) +CH4(g) ,测得容器内初始压强为50kPa,反应过程中反应时间t与气体总压p总的关系如下表所示。
| 反应时间t/s | 0 | 100 | 350 | 850 | 2000 | 2500 |
| 气体总压p总/kPa | 50.0 | 55.0 | 65.0 | 83.2 | 125.0 | 125.0 |
②若反应达到平衡后,升高温度,CH3OCH3的浓度增大,则正反应为
③该温度下,要缩短反应达到平衡所需的时间,可采取的措施是
(3)在T2℃、p0kPa(恒温、恒压)下,将等物质的量的CO与H2通入容积为VL的容器内,发生反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)。反应达到平衡时,测得容器容积为0.6VL,用气体分压[气体分压(p)=气体总压(p总)×体积分数]代替平衡浓度表示的平衡常数Kp=
 =
=
您最近一年使用:0次



