2023高三·全国·专题练习
解题方法
1 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_______  。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为_______ mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为_______ 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2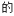 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
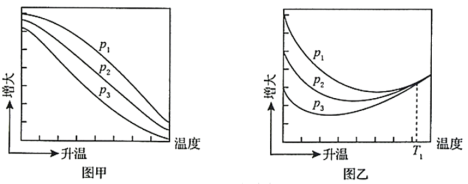
已知:CO2的平衡转化率=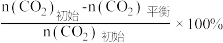
CH3OH的平衡产率=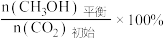
其中纵坐标表示CO2平衡转化率的是图_______ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_______ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_______ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)

 。
。(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2
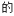 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:CO2的平衡转化率=
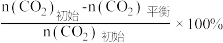
CH3OH的平衡产率=
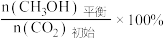
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
2023-01-31更新
|
546次组卷
|
4卷引用:专题09 化学反应速率与化学平衡(测)-2023年高考化学二轮复习讲练测(新高考专用)
(已下线)专题09 化学反应速率与化学平衡(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素广东北江实验学校2023—2024学年高二上学期10月月考化学试题山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
名校
解题方法
2 . 在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:
反应Ⅰ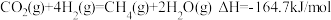
反应Ⅱ
反应Ⅲ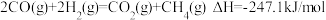
向恒压、密闭容器中通入 和
和 ,平衡时
,平衡时 、
、 、
、 的物质的量随温度的变化如图所示,下列叙述错误的是
的物质的量随温度的变化如图所示,下列叙述错误的是

反应Ⅰ
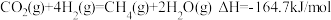
反应Ⅱ

反应Ⅲ
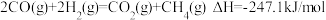
向恒压、密闭容器中通入
 和
和 ,平衡时
,平衡时 、
、 、
、 的物质的量随温度的变化如图所示,下列叙述错误的是
的物质的量随温度的变化如图所示,下列叙述错误的是
A.反应Ⅲ在a点的平衡常数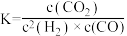 |
B.图中曲线B表示平衡时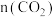 随温度的变化关系 随温度的变化关系 |
C. 的 的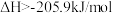 |
D.在低温条件下,可同时提高 平衡转化率和 平衡转化率和 的平衡产率 的平衡产率 |
您最近一年使用:0次
2021-04-23更新
|
1233次组卷
|
5卷引用:专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】
(已下线)专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】山东省聊城市2021届高三下学期第二次模拟考试化学试题江苏省南京市第一中学2021-2022学年高二下学期期中考试化学试题江西省宜春市奉新县第一中学2021-2022学年高二下学期第一次月考化学试题第二章 综合拔高练
名校
解题方法
3 . “绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
Ⅰ.汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一、请回答下列问题:
(1)已知:
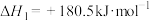

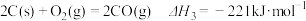
若某反应的平衡常数表达式为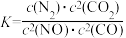 ,则此反应的热化学方程式为
,则此反应的热化学方程式为_______ 。
(2)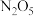 在一定条件下可发生分解:
在一定条件下可发生分解: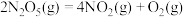 ,一定温度下,在恒容密闭容器中充入一定量
,一定温度下,在恒容密闭容器中充入一定量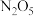 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是_______ (填字母)。
a. 和
和 的浓度比保持不变 b.容器中压强不再变化
的浓度比保持不变 b.容器中压强不再变化
c.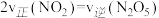 d.气体的密度保持不变
d.气体的密度保持不变
Ⅱ.甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
(3)已知 CO2(g) + 3H2(g)⇌ CH3OH(g) + H2O(g),将 和
和 按物质的量之比1∶3充入体积为2.0 L的恒容密闭容器中反应生成
按物质的量之比1∶3充入体积为2.0 L的恒容密闭容器中反应生成 ,如图1表示压强为0.1 MPa和5.0 MPa下
,如图1表示压强为0.1 MPa和5.0 MPa下 转化率随温度的变化关系。
转化率随温度的变化关系。
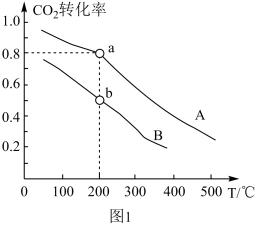
①a、b两点化学反应速率分别用Va、Vb,表示,则Va_______ Vb (填“大于”、“小于”或“等于”)。
②列出a点对应的平衡常数表达式K=_______ 。
(4)在1.0 L恒容密闭容器中投入1 mol CO2和2.75 mol H2发生反应:CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是_______ 。
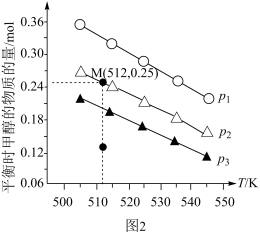
A.该反应的正反应为放热反应
B.压强大小关系为P1<P2<P3
C.M点对应的平衡常数K的值约为
D.在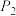 及512 K时,图中N点
及512 K时,图中N点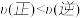
(5) 催化加氢合成乙醇的反应为:2CO2(g) + 6H2(g)⇌C2H5OH(g) + 3H2O(g)
催化加氢合成乙醇的反应为:2CO2(g) + 6H2(g)⇌C2H5OH(g) + 3H2O(g)  ;m代表起始时的投料比,即
;m代表起始时的投料比,即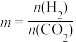 。
。
①图3中投料比相同,温度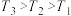 ,则该反应的焓变
,则该反应的焓变
_______ 0(填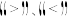 )。
)。

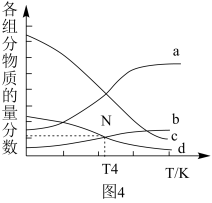
②m=3时,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为_______ (填化学式)。
Ⅰ.汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一、请回答下列问题:
(1)已知:

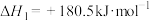

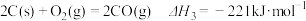
若某反应的平衡常数表达式为
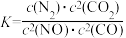 ,则此反应的热化学方程式为
,则此反应的热化学方程式为(2)
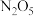 在一定条件下可发生分解:
在一定条件下可发生分解: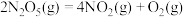 ,一定温度下,在恒容密闭容器中充入一定量
,一定温度下,在恒容密闭容器中充入一定量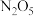 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是a.
 和
和 的浓度比保持不变 b.容器中压强不再变化
的浓度比保持不变 b.容器中压强不再变化c.
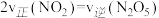 d.气体的密度保持不变
d.气体的密度保持不变Ⅱ.甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
(3)已知 CO2(g) + 3H2(g)⇌ CH3OH(g) + H2O(g),将
 和
和 按物质的量之比1∶3充入体积为2.0 L的恒容密闭容器中反应生成
按物质的量之比1∶3充入体积为2.0 L的恒容密闭容器中反应生成 ,如图1表示压强为0.1 MPa和5.0 MPa下
,如图1表示压强为0.1 MPa和5.0 MPa下 转化率随温度的变化关系。
转化率随温度的变化关系。
①a、b两点化学反应速率分别用Va、Vb,表示,则Va
②列出a点对应的平衡常数表达式K=
(4)在1.0 L恒容密闭容器中投入1 mol CO2和2.75 mol H2发生反应:CO2(g) + 3H2(g)⇌CH3OH(g) + H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是

A.该反应的正反应为放热反应
B.压强大小关系为P1<P2<P3
C.M点对应的平衡常数K的值约为

D.在
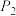 及512 K时,图中N点
及512 K时,图中N点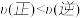
(5)
 催化加氢合成乙醇的反应为:2CO2(g) + 6H2(g)⇌C2H5OH(g) + 3H2O(g)
催化加氢合成乙醇的反应为:2CO2(g) + 6H2(g)⇌C2H5OH(g) + 3H2O(g)  ;m代表起始时的投料比,即
;m代表起始时的投料比,即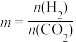 。
。①图3中投料比相同,温度
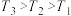 ,则该反应的焓变
,则该反应的焓变
 )。
)。
②m=3时,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为

您最近一年使用:0次
2021-02-02更新
|
674次组卷
|
3卷引用:专题十二化学反应速率与平衡
名校
解题方法
4 . 以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程如图所示。
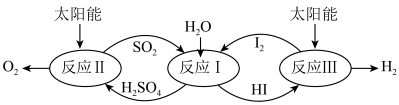
相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1
反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是

相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是
| A.该过程实现了太阳能到化学能的转化 |
| B.SO2和I2对总反应起到了催化作用 |
| C.总反应的热化学方程式为2H2O(l)=2H2(g)+O2(g) H=+286kJ•mol-1 |
| D.该过程降低了水分解制氢的活化能,但总反应的H不变 |
您最近一年使用:0次
2020-10-12更新
|
2808次组卷
|
28卷引用:考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》
(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》2019年秋高三化学复习强化练习—— 盖斯定律及其应用(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)(已下线)高中化学《新教材变化解读与考法剖析》第一章 化学反应的热效应(人教版2019选择性必修1)(已下线)2023年北京卷高考真题变式题(选择题11-14)【区级联考】北京市海淀区2019届高三第一学期上学期期末考试化学试题【全国百强校】浙江省学军中学2019届高三下学期4月选考模拟冲刺化学试题【全国百强校】内蒙古自治区赤峰二中2018-2019学年高一下学期第二次月考化学试题河南省实验中学2020届高三12月月考化学试题北京市2020届高三12月月考(新高考选考模式)化学试题北京市2020届高三质量监测化学试题山东省济南市历城第二中学2021届高三10月份学情检测化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 过模拟 2年模拟精编精练湖北省部分省重点中学2020-2021学年高二上学期期中联考化学试题湖北省部分重点中学2020-2021学年高二上学期期中考试化学试题安徽省怀宁中学2020-2021学年高一下学期第一次月考化学试题山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题北京市第三十一中学2021-2022学年高二上学期期中考试化学试题山东省聊城市第二中学2022-2023学年高二上学期第一次月考化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题山东省临沂市平邑县第一中学2022-2023学年高二上学期10月月考化学试题 湖北省仙桃中学2022-2023学年高一上学期10月月考化学试题湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题湖南省南雅中学2023-2024学年高二上学期第一次月考化学试题江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题河北省唐山市丰润区2023-2024学年高二上学期期中考试化学试题福建省厦门市集美中学2023-2024学年高二上学期10月第一次月考化学试题
2019高三·全国·专题练习
名校
5 . 环戊二烯(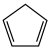 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: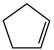 (g) =
(g) =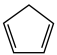 (g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应:
(g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应: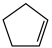 (g)+ I2(g) =
(g)+ I2(g) = (g)+2HI(g) ③ ΔH3=
(g)+2HI(g) ③ ΔH3=___________ kJ·mol −1。
(2)某温度下,等物质的量的碘和环戊烯(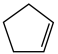 )在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为
)在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为_________ ,该反应的平衡常数Kp=_________ Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________ (填标号)。
A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________ (填标号)。
A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L−1
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:(1)已知:
 (g) =
(g) = (g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应:
(g)+H2(g) ΔH1=100.3 kJ·mol −1①H2(g)+ I2(g) =2HI(g) ΔH2=−11.0 kJ·mol −1②,对于反应: (g)+ I2(g) =
(g)+ I2(g) = (g)+2HI(g) ③ ΔH3=
(g)+2HI(g) ③ ΔH3=(2)某温度下,等物质的量的碘和环戊烯(
 )在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为
)在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是

A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L−1
您最近一年使用:0次
2019-06-26更新
|
2666次组卷
|
20卷引用:专题09 反应速率、化学平衡——2019年高考真题和模拟题化学分项汇编
(已下线)专题09 反应速率、化学平衡——2019年高考真题和模拟题化学分项汇编(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》(已下线)专题7.2 化学平衡状态 化学平衡移动(讲)-《2020年高考一轮复习讲练测》(已下线)第23讲 化学平衡状态 化学平衡的移动 (精讲)——2021年高考化学一轮复习讲练测(已下线)第19讲 化学平衡(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)江西省高安中学2019-2020学年高二上学期期末考试化学(B卷)试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2章 综合检测高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二章素养检测(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过高考四川省遂宁市2020-2021学年高二下学期期末考试化学试题选择性必修1(SJ)专题2专题培优专练山东省临沂市平邑县第一中学实验部2021-2022学年高二上学期第二次月考化学试题江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题河南省洛阳市第一中学2022-2023学年高二上学期期末检测化学试题福建省泉州市南安市侨光中学2022-2023学年高二上学期10月月考化学试题湖南省邵阳市新邵县2023-2024学年高二上学期期末考试化学试题
2019高三·全国·专题练习
6 . 氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H2和CO2,其物质的量之比为4∶1,甲烷和水蒸气反应的方程式是______ 。
②已知反应器中还存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
iii.CH4(g)=C(s)+2H2(g) ΔH3
……
iii为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用______ 反应的ΔH。
甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H2和CO2,其物质的量之比为4∶1,甲烷和水蒸气反应的方程式是
②已知反应器中还存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
iii.CH4(g)=C(s)+2H2(g) ΔH3
……
iii为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用
您最近一年使用:0次
2019-06-21更新
|
349次组卷
|
7卷引用:专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编
(已下线)专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)1.3.1+盖斯定律-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)辽宁省大连市第四十四中学2022-2023学年高三上学期10月考试化学试题
名校
7 . 已知:2C(s)+O2(g)===2CO(g) ΔH=-Q1 kJ·mol-1;
C(s)+O2(g)===CO2(g) ΔH=-Q2 kJ·mol-1;
S(s)+O2(g)===SO2(g) ΔH=-Q3 kJ·mol-1。
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( )
C(s)+O2(g)===CO2(g) ΔH=-Q2 kJ·mol-1;
S(s)+O2(g)===SO2(g) ΔH=-Q3 kJ·mol-1。
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( )
| A.SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-2Q2+Q3) kJ·mol-1 |
| B.S(s)+2CO(g)===SO2(g)+2C(s) ΔH=(Q1-Q3) kJ·mol-1 |
| C.SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(Q1-2Q2+Q3) kJ·mol-1 |
| D.SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-Q2+2Q3) kJ·mol-1 |
您最近一年使用:0次
2017-11-11更新
|
948次组卷
|
7卷引用:《2018-2019学年同步单元双基双测AB卷》第一单元 化学反应与能量单元测试(B卷)



