名校
1 . 二氧化碳加氢是对温室气体的有效转化,同时也是生成再生能源与化工原料的重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为 。
。
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成 该物质的焓变。则该反应的反应热
该物质的焓变。则该反应的反应热
_______ 。
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有_______ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是_______ (填字母)。
a. b.容器内气体密度不再改变
b.容器内气体密度不再改变
c. 的物质的量分数不再改变 d.
的物质的量分数不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
(2) 催化加氢制低碳烯烃的反应历程如图所示,
催化加氢制低碳烯烃的反应历程如图所示, 首先在
首先在 表面解离成2个
表面解离成2个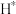 ,随后参与到
,随后参与到 的转化过程。
的转化过程。
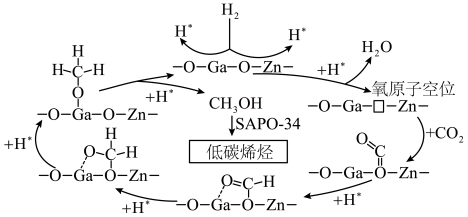
注:“□”表示氧原子空位,“*”表示吸附在催化剂上的微粒。
理论上反应历程中消耗的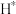 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为_______ 。
(3)一定条件下 与
与 可生成甲酸
可生成甲酸 ,化学方程式为
,化学方程式为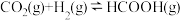 。
。
①在 下,等物质的量的
下,等物质的量的 与
与 的混合气体反应生成甲酸,化学反应速率
的混合气体反应生成甲酸,化学反应速率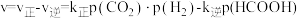 ,
,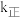 、k逆分别为正反应、逆反应的速率常数,
、k逆分别为正反应、逆反应的速率常数, 为气体的分压(气体分压=气体总压
为气体的分压(气体分压=气体总压 体积分数)。用气体分压表示的平衡常数
体积分数)。用气体分压表示的平衡常数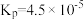 ,则
,则 的转化率为
的转化率为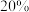 时,
时,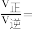
_______ 。
②恒定压强为 时,向密闭容器中充入一定量的
时,向密闭容器中充入一定量的 气体,
气体, 除了能分解成
除了能分解成 和
和 ,还能分解为
,还能分解为 和
和 ,反应为
,反应为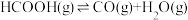 ,则此平衡体系中
,则此平衡体系中 或
或 的选择性和
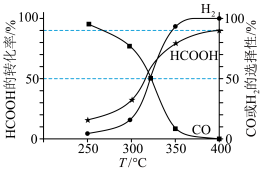
的选择性和 的转化率随温度变化曲线如图所示。图中随着温度升高,
的转化率随温度变化曲线如图所示。图中随着温度升高, 的转化率增大,请解释
的转化率增大,请解释 的选择性下降可能的原因:
的选择性下降可能的原因:_______ 。 时
时 的体积分数为
的体积分数为_______ 。
(1)由
 加氢生成
加氢生成 的反应为
的反应为 。
。①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成 该物质的焓变。则该反应的反应热
该物质的焓变。则该反应的反应热
| 物质 | CO2 | H2 | CH4 | H2O |
 (kJ·mol-1) (kJ·mol-1) | -393.5 | 0 | -74.8 | -241.8 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
 b.容器内气体密度不再改变
b.容器内气体密度不再改变c.
 的物质的量分数不再改变 d.
的物质的量分数不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2(2)
 催化加氢制低碳烯烃的反应历程如图所示,
催化加氢制低碳烯烃的反应历程如图所示, 首先在
首先在 表面解离成2个
表面解离成2个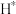 ,随后参与到
,随后参与到 的转化过程。
的转化过程。
注:“□”表示氧原子空位,“*”表示吸附在催化剂上的微粒。
理论上反应历程中消耗的
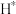 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为(3)一定条件下
 与
与 可生成甲酸
可生成甲酸 ,化学方程式为
,化学方程式为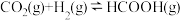 。
。①在
 下,等物质的量的
下,等物质的量的 与
与 的混合气体反应生成甲酸,化学反应速率
的混合气体反应生成甲酸,化学反应速率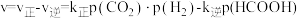 ,
,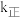 、k逆分别为正反应、逆反应的速率常数,
、k逆分别为正反应、逆反应的速率常数, 为气体的分压(气体分压=气体总压
为气体的分压(气体分压=气体总压 体积分数)。用气体分压表示的平衡常数
体积分数)。用气体分压表示的平衡常数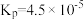 ,则
,则 的转化率为
的转化率为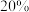 时,
时,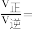
②恒定压强为
 时,向密闭容器中充入一定量的
时,向密闭容器中充入一定量的 气体,
气体, 除了能分解成
除了能分解成 和
和 ,还能分解为
,还能分解为 和
和 ,反应为
,反应为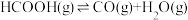 ,则此平衡体系中
,则此平衡体系中 或
或 的选择性和
的选择性和 的转化率随温度变化曲线如图所示。图中随着温度升高,
的转化率随温度变化曲线如图所示。图中随着温度升高, 的转化率增大,请解释
的转化率增大,请解释 的选择性下降可能的原因:
的选择性下降可能的原因: 时
时 的体积分数为
的体积分数为
您最近一年使用:0次
2 . 实验小组设计了如图实验装置探究化学能与热能的转化。
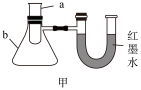
回答下列问题:
(1)A同学向装置甲的a仪器中加入镁和稀硫酸,能证明该反应是放热反应的现象是_______ ,若标准状况下生成5.6LH2时放热QkJ,该反应的热化学方程式为_______ 。
(2)B同学向装置甲的a仪器中加入适量硝酸铵固体和水,并用玻璃棒搅拌,可观察到的现象是_______ ,说明硝酸铵固体溶于水时要_______ (填“吸收”或“放出”)热量。
(3)装置乙不能证明“镁和稀硫酸反应是吸热反应还是放热反应”的理由是_______ 。
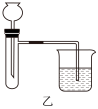
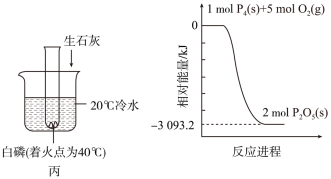
(4)C同学利用装置丙证明生石灰与水反应是放热反应,试管中的现象是_______ 。P4和O2反应的能量变化如图丁所示。该反应的热化学方程式为_______ 。

回答下列问题:
(1)A同学向装置甲的a仪器中加入镁和稀硫酸,能证明该反应是放热反应的现象是
(2)B同学向装置甲的a仪器中加入适量硝酸铵固体和水,并用玻璃棒搅拌,可观察到的现象是
(3)装置乙不能证明“镁和稀硫酸反应是吸热反应还是放热反应”的理由是

(4)C同学利用装置丙证明生石灰与水反应是放热反应,试管中的现象是

您最近一年使用:0次
2022-09-02更新
|
177次组卷
|
2卷引用:辽宁省朝阳市凌源市2022-2023学年高二上学期第一次月考化学试题
名校
3 . 纳米碗C40H10是一种奇特的碗状共轭体系。高温条件下,C40H10可以由C40H20分子经过连续5步氢抽提和闭环脱氢反应生成。其中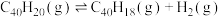 的反应机理和能量变化如图。下列说法不正确的是
的反应机理和能量变化如图。下列说法不正确的是
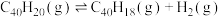 的反应机理和能量变化如图。下列说法不正确的是
的反应机理和能量变化如图。下列说法不正确的是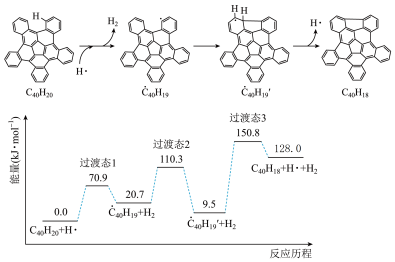
| A.选择相对较高的温度更有利于制备纳米碗 |
| B.推测 C40H10纳米碗中含5个五元环 |
C.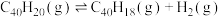 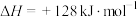 |
| D.该反应历程包含了3步基元反应,且第3步是该反应的决速步骤 |
您最近一年使用:0次
2024-05-03更新
|
475次组卷
|
3卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(七)
名校
解题方法
4 . 下列说法不正确的是
| A.化学反应除了物质的变化,还伴随着能量的变化,能量的变化不仅表现在化学能与热能之间,还表现在化学能与电能、光能等 |
| B.需要加热才能发生的反应都是吸热反应 |
| C.当反应物的总能量高于生成物时,该反应放热 |
| D.化学电池是新能源和可再生能源的重要组成部分 |
您最近一年使用:0次
单选题
|
适中(0.65)
|
名校
5 . 一定条件下,在水溶液中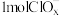 (x=0,1,2,3)的相对能量(kJ)大小如图所示。下列有关说法
(x=0,1,2,3)的相对能量(kJ)大小如图所示。下列有关说法错误 的是
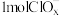 (x=0,1,2,3)的相对能量(kJ)大小如图所示。下列有关说法
(x=0,1,2,3)的相对能量(kJ)大小如图所示。下列有关说法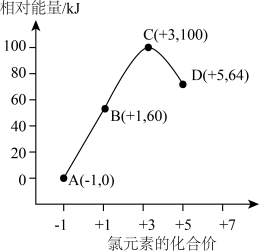
| A.上述离子中最稳定的是A |
B.反应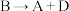 的热化学方程式为 的热化学方程式为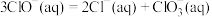 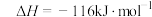 |
C.反应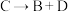 中反应物的键能之和大于生成物的键能之和 中反应物的键能之和大于生成物的键能之和 |
D.相同条件下,上述离子中结合 能力最强的是B 能力最强的是B |
您最近一年使用:0次
名校
解题方法
6 . 已知反应: 为放热反应。下列关于该反应的说法正确的是
为放热反应。下列关于该反应的说法正确的是
 为放热反应。下列关于该反应的说法正确的是
为放热反应。下列关于该反应的说法正确的是| A.M的能量一定低于X |
| B.断裂反应物中化学键所吸收能量大于形成生成物中化学键所放出能量 |
| C.该反应为放热反应,故常温下反应一定可以发生 |
| D.X和Y的总能量一定高于M和N的总能量 |
您最近一年使用:0次
名校
7 . 铬及其化合物在催化方面具有重要应用。Cr2O3在丙烷脱氢:C3H8(g)=3C(石墨,s)+4H2(g)过程中起到催化作用,其中的部分反应历程如图所示。下列说法错误的是
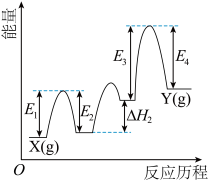

| A.Cr2O3在丙烷脱氢的反应过程中可能作氧化剂和氧化产物 |
| B.该反应的焓变为E1-E2+ΔH2+E3-E4 |
| C.C3H8(g)=3C(石墨,s)+4H2(g),该反应在高温条件下能自发进行 |
| D.该反应可实现将化学能转化为热能 |
您最近一年使用:0次
2024-01-13更新
|
95次组卷
|
3卷引用:湖南省长沙市麓山国际实验学校2023-2024学年高二上学期第三次月考化学试题
8 . 在一定体积下,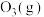 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是

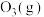 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是
A.根据图像可知: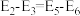 |
B.形成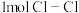 键时释放的能量为 键时释放的能量为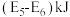 |
C. 的平衡转化率:历程I=历程II 的平衡转化率:历程I=历程II |
D.在该历程中速率最快步骤的热化学方程式为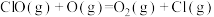  |
您最近一年使用:0次
2024-02-13更新
|
91次组卷
|
2卷引用:山东省泰安第一中学2023-2024学年高二上学期12月月考化学试题
9 . 2SO2(g)+O2(g) 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是| A.基元反应发生的先决条件是反应物分子发生有效碰撞 |
| B.增大SO2的浓度可以显著提高总反应的速率 |
| C.V2O5的存在提高了该反应活化分子百分数,使有效碰撞次数增加,反应速率加快 |
| D.逆反应的活化能比正反应的活化能大198kJ•mol-1 |
您最近一年使用:0次
10 . 催化剂Ⅰ和Ⅱ均能催化反应 ,反应历程(如图所示)中,M为中间产物。其他条件相同时,下列说法错误的是
,反应历程(如图所示)中,M为中间产物。其他条件相同时,下列说法错误的是

 ,反应历程(如图所示)中,M为中间产物。其他条件相同时,下列说法错误的是
,反应历程(如图所示)中,M为中间产物。其他条件相同时,下列说法错误的是
| A.该反应反应物的总能量大于生成物的总能量 |
| B.当催化剂为Ⅰ时,增大压强,反应速率加快,R的平衡转化率增大 |
| C.使用催化剂Ⅰ的最高活化能小于Ⅱ的最高活化能 |
| D.Ⅰ和Ⅱ相比,使用催化剂Ⅰ时,反应过程中M所能达到的最高浓度更大 |
您最近一年使用:0次
2023-10-12更新
|
121次组卷
|
2卷引用:湖南省部分学校2023-2024学年高二上学期10月联考化学试题



