名校
解题方法
1 . I.磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。

回答下列问题:
(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图

①该反应的化学方程式为_______ (A用化学式表示)
②前10s的平均反应速率v(Cl2)=_______
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
③A与热水反应的化学方程式为_______
II.(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)__________________ 。
(2)该装置中负极的电极方程式为_______ 。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子_______ mol。

回答下列问题:
(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图

①该反应的化学方程式为
②前10s的平均反应速率v(Cl2)=
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
③A与热水反应的化学方程式为
II.(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)
(2)该装置中负极的电极方程式为
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子
您最近一年使用:0次
名校
解题方法
2 . 在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现新期特的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
(1)控制条件,让反应在恒容密闭容器中进行如下反应: 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。
前2s内的平均反应速率
___________ ,从表格看,已达化学平衡的时间段为:___________ 。
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,发生反应
气体后,发生反应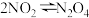 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
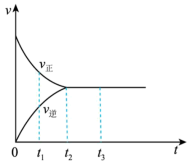
下列叙述正确的是___________ 。
a. 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小
b. 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行
c. 各物质浓度不再变化
各物质浓度不再变化
d. 各物质浓度相等
各物质浓度相等
e. ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
(3)在压强为 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
___________ ,
___________ 。
(4)比较相同浓度的 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定___________ 来实现。
(5)在四个不同的容器中,在不同的条件下进行合成氨反应: 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
(1)控制条件,让反应在恒容密闭容器中进行如下反应:
 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,发生反应
气体后,发生反应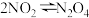 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
下列叙述正确的是
a.
 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小b.
 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行c.
 各物质浓度不再变化
各物质浓度不再变化 d.
 各物质浓度相等
各物质浓度相等e.
 ,
, 浓度增大
浓度增大 f.反应过程中气体的颜色不变
(3)在压强为
 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:

| 实验编号 |  (℃) (℃) |  |  |
| ① | 180 |  | 0.1 |
| ② |  |  | 5 |
| ③ | 350 |  | 5 |
 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定(5)在四个不同的容器中,在不同的条件下进行合成氨反应:
 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________A. | B. |
C. | D. |
您最近一年使用:0次
2023-05-16更新
|
477次组卷
|
2卷引用:江西省上犹中学2022-2023学年高一下学期6月期末考试化学试题
名校
解题方法
3 . 某研究团队以NO和H2为原料,在Fe基催化下有效地合成NH3.回答下列问题:
已知:①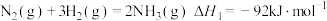
②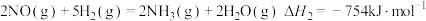
(1)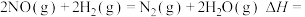
___________  。
。
(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是___________ (填标号)。
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现, 分两步进行:
分两步进行:
第1步: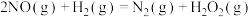 (慢反应);
(慢反应);
第2步:___________ (补充)(快反应)。
加入催化剂,主要是降低第___________ (填“1”或“2”)步反应活化能。
(4) 的反应速率方程式为
的反应速率方程式为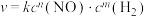 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
根据上述数据计算:m=___________ ,n=___________ ,c=___________ 。
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应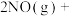
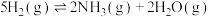 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。

温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是___________ 。a点时生成NH3的物质的量为___________ (结果保留3位有效数字)。
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)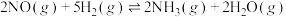 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
___________  (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
已知:①
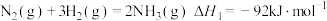
②
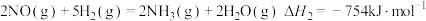
(1)
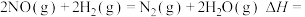
 。
。(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现,
 分两步进行:
分两步进行:第1步:
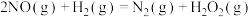 (慢反应);
(慢反应);第2步:
加入催化剂,主要是降低第
(4)
 的反应速率方程式为
的反应速率方程式为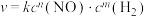 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:| 序号 | 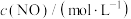 | 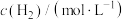 | 速率 |
| I | 0.1 | 0.1 | v |
| II | 0.2 | 0.1 | 4v |
| III | 0.2 | 0.2 | 8v |
| IV | c | 0.4 | 36v |
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应
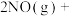
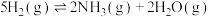 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。
温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)
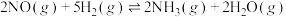 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
 (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
您最近一年使用:0次
2024-01-19更新
|
164次组卷
|
3卷引用:江西省部分学校2023-2024学年高三上学期12月月考化学试题
名校
4 . 甲醇是重要的化学工业基础原料和清洁液体燃料,工业上利用CO和 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。
(1)已知反应中有关物质的化学键键能数据如下表所示:
则

_____________ 
(2)在1L恒容密闭容器中充入2mol CO和4mol ,CO的平衡转化率(α)随温度和压强变化的如图所示。
,CO的平衡转化率(α)随温度和压强变化的如图所示。

②
_____________  (填“<”、“=”、“>”)。理由
(填“<”、“=”、“>”)。理由_________________ ;
②在一定条件下,经过10min达到平衡状态a点处。则在该条件下,从开始至达到平衡状态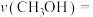
______ ,abc三点对应平衡常数 、
、 、
、 的大小关系:
的大小关系:_____________ 。
③能说明该反应已达平衡状态的是_____________ 。
A. B.CO和
B.CO和 的浓度之比不再随时间改变
的浓度之比不再随时间改变
C.混合气体的密度不随时间变化 D.气体的平均相对分子质量不再随时间改变
(3) 也可由
也可由 和
和 合成。一定条件下,向1L恒容密闭容器中充入1mol
合成。一定条件下,向1L恒容密闭容器中充入1mol  和2mol
和2mol  ,一定条件下反应
,一定条件下反应
 ,平衡时测得生成甲醇0.5mol,该反应的平衡常数
,平衡时测得生成甲醇0.5mol,该反应的平衡常数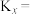
___________________ (对于反应 ,
, ,x为物质的量分数)。
,x为物质的量分数)。
 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。(1)已知反应中有关物质的化学键键能数据如下表所示:
| 化学键 | H-H | C-O | C O O | H-O | C-H |
| E/(kJ/mol) | 436 | 342 | 1076 | 465 | 413 |
则



(2)在1L恒容密闭容器中充入2mol CO和4mol
 ,CO的平衡转化率(α)随温度和压强变化的如图所示。
,CO的平衡转化率(α)随温度和压强变化的如图所示。
②

 (填“<”、“=”、“>”)。理由
(填“<”、“=”、“>”)。理由②在一定条件下,经过10min达到平衡状态a点处。则在该条件下,从开始至达到平衡状态
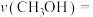
 、
、 、
、 的大小关系:
的大小关系:③能说明该反应已达平衡状态的是
A.
 B.CO和
B.CO和 的浓度之比不再随时间改变
的浓度之比不再随时间改变C.混合气体的密度不随时间变化 D.气体的平均相对分子质量不再随时间改变
(3)
 也可由
也可由 和
和 合成。一定条件下,向1L恒容密闭容器中充入1mol
合成。一定条件下,向1L恒容密闭容器中充入1mol  和2mol
和2mol  ,一定条件下反应
,一定条件下反应
 ,平衡时测得生成甲醇0.5mol,该反应的平衡常数
,平衡时测得生成甲醇0.5mol,该反应的平衡常数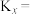
 ,
, ,x为物质的量分数)。
,x为物质的量分数)。
您最近一年使用:0次
名校
解题方法
5 . 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有_______ (填序号)。
①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)在2 L密闭绝热容器中,投入4 mol N2和6 mol H2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如下表:
①下列能说明该反应已达到平衡状态的是_______ 。
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②在T3温度下,达到平衡时N2的体积分数_______ 。
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:

①表示H2浓度变化的曲线是_______ (填“A”、“B”或“C”)。
②在0~25 min内N2的平均反应速率为_______ 。
(4)CO2与NH3反应可合成尿素:CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
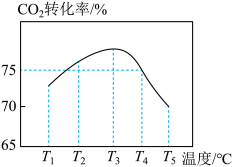
①该反应的ΔH_______ (填“>”或“<”)0。
②T4℃时反应的平衡常数K=_______ 。
③T1~T3℃之间,CO2转化率逐渐增大,其原因是_______
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)在2 L密闭绝热容器中,投入4 mol N2和6 mol H2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如下表:
| 温度/K | T1 | T2 | T3 | T4 |
| n(NH3)/mol | 3.6 | 3.2 | 2.8 | 2.0 |
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②在T3温度下,达到平衡时N2的体积分数
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)
 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
①表示H2浓度变化的曲线是
②在0~25 min内N2的平均反应速率为
(4)CO2与NH3反应可合成尿素:CO2(g)+2NH3(g)
 CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
①该反应的ΔH
②T4℃时反应的平衡常数K=
③T1~T3℃之间,CO2转化率逐渐增大,其原因是
您最近一年使用:0次
2023-02-02更新
|
177次组卷
|
2卷引用:江西省吉水中学2023届高三下学期一模考试化学试题
名校
解题方法
6 . 甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。一定条件下,在体积为 的密闭容器中,充入
的密闭容器中,充入 和
和 ,发生反应:
,发生反应: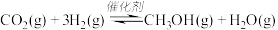 ,测得
,测得 的物质的量随时间变化如表所示,该反应的能量变化如图所示:
的物质的量随时间变化如表所示,该反应的能量变化如图所示:

(1)该反应为_____ (填放热或吸热)反应。
(2)从反应开始到5min末,用氢气浓度变化表示的平均反应速率v(H2)=___ ,容器内平衡时与起始时的压强之比为____ 。
(3)在相同温度容积不变的条件下,能说明该反应已达平衡状态的是____ (填写序号字母)。
a.容器内的平均相对分子质量保持不变 b.容器内压强保持不变
c. 的消耗速率与
的消耗速率与 的生成速率之比为3:1 d.
的生成速率之比为3:1 d.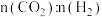 的比值保持不变
的比值保持不变
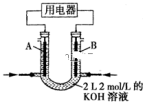
(4)将 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得电池工作时OHˉ向B电极定向移动,则
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得电池工作时OHˉ向B电极定向移动,则_____ (填“A”或“B”)处电极入口通甲醇,当电路中通过 电子时,理论上消耗
电子时,理论上消耗 质量为
质量为_____ 克。
(5)下列化学电池不易造成环境污染的是____ (填字母)。
A.甲醇氧气燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
铅蓄电池是最常见的二次电池,放电时的化学方程式为: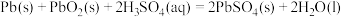 。该蓄电池放电时,正极电极反应方程式为
。该蓄电池放电时,正极电极反应方程式为__________ 。
 的密闭容器中,充入
的密闭容器中,充入 和
和 ,发生反应:
,发生反应: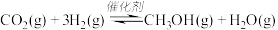 ,测得
,测得 的物质的量随时间变化如表所示,该反应的能量变化如图所示:
的物质的量随时间变化如表所示,该反应的能量变化如图所示:
 | 0 | 2 | 5 | 10 | 15 |
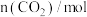 | 2 | 0.75 | 0.5 | 0.25 | 0.25 |
(1)该反应为
(2)从反应开始到5min末,用氢气浓度变化表示的平均反应速率v(H2)=
(3)在相同温度容积不变的条件下,能说明该反应已达平衡状态的是
a.容器内的平均相对分子质量保持不变 b.容器内压强保持不变
c.
 的消耗速率与
的消耗速率与 的生成速率之比为3:1 d.
的生成速率之比为3:1 d.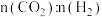 的比值保持不变
的比值保持不变(4)将
 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得电池工作时OHˉ向B电极定向移动,则
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得电池工作时OHˉ向B电极定向移动,则 电子时,理论上消耗
电子时,理论上消耗 质量为
质量为
(5)下列化学电池不易造成环境污染的是
A.甲醇氧气燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
铅蓄电池是最常见的二次电池,放电时的化学方程式为:
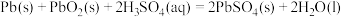 。该蓄电池放电时,正极电极反应方程式为
。该蓄电池放电时,正极电极反应方程式为
您最近一年使用:0次
2020-07-29更新
|
141次组卷
|
3卷引用:江西省萍乡市2019-2020学年高一下学期期末考试化学试题
7 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态氮原子的价层电子轨道表示式为:______ 。
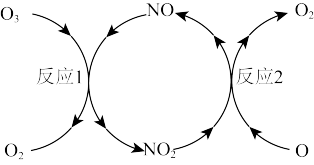
(2)NO加速臭氧层被破坏,其反应过程如下图所示:
已知: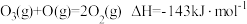
反应1: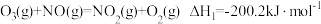 。
。
反应2的热化学方程式为___________ 。
(3)工业上以CO和 为原料合成甲醇的反应:
为原料合成甲醇的反应: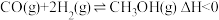 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
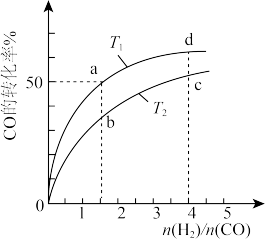
①判断T1___________ T2 (选填“<”、“>”或“=”);
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为
___________ ;
③该反应平衡常数的表达式为K=___________ ,d点的平衡常数的值为___________ ;
④a点状态下再通入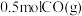 和
和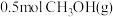 ,平衡
,平衡____ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点H2转化率由大到小的顺序是___________ 。
(1)基态氮原子的价层电子轨道表示式为:
(2)NO加速臭氧层被破坏,其反应过程如下图所示:

已知:
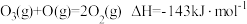
反应1:
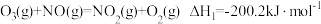 。
。反应2的热化学方程式为
(3)工业上以CO和
 为原料合成甲醇的反应:
为原料合成甲醇的反应: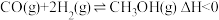 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
①判断T1
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为

③该反应平衡常数的表达式为K=
④a点状态下再通入
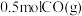 和
和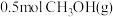 ,平衡
,平衡⑤a、b、c三点H2转化率由大到小的顺序是
您最近一年使用:0次
2022-02-16更新
|
302次组卷
|
2卷引用:江西省吉安市第三中学2022-2023学年高二上学期1月期末考试化学试题
8 . 甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) =H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________
(2)甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:

①600K时,Y点甲醇的υ(逆)_____ υ(正)(填“>”或“<”)
②若改变条件使之从Y点到X点,则改变条件可以是___________ 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(I)和(II)分别进行催化CH3OH的脱氢实验:CH3OH(g) HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
可以判断:实验①的前20 min的平均反应速率 ν(H2)=________ ;实验温度T1_____ T2(填“>”、“<”);催化剂的催化效率:实验①________ 实验②(填“>”、“<”)。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程, 除去甲醇的离子方程式为____________

(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) =H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)甲醇脱氢可制取甲醛CH3OH(g)
 HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
①600K时,Y点甲醇的υ(逆)
②若改变条件使之从Y点到X点,则改变条件可以是
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(I)和(II)分别进行催化CH3OH的脱氢实验:CH3OH(g)
 HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
HCHO(g)+H2(g),CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程, 除去甲醇的离子方程式为

您最近一年使用:0次
解题方法
9 . 化学反应原理在科研和生产中有广泛应用.
Ⅰ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是 (填图中数字序号)。
(2)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:________NH4+ + 5O2== 2NO2- + ________H+ +__________+__________
Ⅱ.工业合成氨原理是:N2(g)+3H2(g) 2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图。
2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图。

(1)曲线a对应的温度是 。
(2)关于工业合成氨的反应,下列叙述正确的是 。
Ⅲ.尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_________________________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为______________________。
Ⅰ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是 (填图中数字序号)。
(2)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:________NH4+ + 5O2== 2NO2- + ________H+ +__________+__________
Ⅱ.工业合成氨原理是:N2(g)+3H2(g)
 2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图。
2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图。
(1)曲线a对应的温度是 。
(2)关于工业合成氨的反应,下列叙述正确的是 。
| A.及时分离出NH3可以提高H2的平衡转化率 |
| B.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N) |
| C.M点比N点的反应速率快 |
| D.如果N点时c(NH3)=0.2mol·L-1,N点的化学平衡常数K≈0.93L2/mol2 |
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_________________________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为______________________。
您最近一年使用:0次
10 . (1)恒温,容积为1 L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)  2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:

①写出能表示硫的燃烧热的热化学方程式: ___________________。
②ΔH2=________kJ·mol-1。
③在相同条件下,充入1 mol SO3和0.5 mol的O2,则达到平衡时SO3的转化率为________;此时该反应________(填“放出”或“吸收”)________kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
①有效“减碳”的手段之一是节能,下列制氢方法最节能的是________(填序号)。
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O(g) 2H2+O2
2H2+O2
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O(g) CO+3H2
CO+3H2
②CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。

③能说明上述反应达到平衡状态的是________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g) CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应ΔS<0
C.在T℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 MPa)和250℃,是因为此条件下,原料气转化率最高
 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式: ___________________。
②ΔH2=________kJ·mol-1。
③在相同条件下,充入1 mol SO3和0.5 mol的O2,则达到平衡时SO3的转化率为________;此时该反应________(填“放出”或“吸收”)________kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
①有效“减碳”的手段之一是节能,下列制氢方法最节能的是________(填序号)。
A.电解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑B.高温使水分解制氢:2H2O(g)
 2H2+O2
2H2+O2C.太阳光催化分解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑D.天然气制氢:CH4+H2O(g)
 CO+3H2
CO+3H2②CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
③能说明上述反应达到平衡状态的是________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g)
 CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应ΔS<0
C.在T℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 MPa)和250℃,是因为此条件下,原料气转化率最高
您最近一年使用:0次



