名校
1 . 恒温恒压下向密闭容器中充入4mol SO2和2mol O2,反应如下:2SO2(g)+O2(g) 2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析
2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析不正确 的是
 2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析
2SO3(g) ΔH<0;2min时反应达到平衡,生成1.4mol SO3,同时放出热量Q kJ。则下列分析| A.若反应开始时容器体积为2L,则0~2min内v(SO3)>0.35mol/(L·min) |
| B.2min后向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量不变 |
| C.若把条件“恒温恒压”改为“绝热恒压”,则平衡后n(SO3)>1.4mol |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近一年使用:0次
2 . 恒温恒压下向密闭容器中充入4mol SO2和2mol O2,反应如下:2SO2(g)+O2(g) 2SO3(g) ΔH<0.2min时反应达到平衡,生成1.4mol SO3,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0.2min时反应达到平衡,生成1.4mol SO3,同时放出热量QkJ。则下列分析正确的是
 2SO3(g) ΔH<0.2min时反应达到平衡,生成1.4mol SO3,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0.2min时反应达到平衡,生成1.4mol SO3,同时放出热量QkJ。则下列分析正确的是| A.若反应开始时容器体积为2L,则0~2min内v(SO3)>0.35mol/(L·min) |
| B.2min后向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量增大 |
| C.若把条件“恒温恒压”改为“绝热恒压”,则平衡后n(SO3)大于1.4mol |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ |
您最近一年使用:0次
解题方法
3 . 在一定温度下向体积为 的恒容密闭容器中,充入一定量的气体A和气体B,反应生成气体C和固体D,各物质的含量随时间的变化情况如图所示,下列说法错误的是
的恒容密闭容器中,充入一定量的气体A和气体B,反应生成气体C和固体D,各物质的含量随时间的变化情况如图所示,下列说法错误的是

 的恒容密闭容器中,充入一定量的气体A和气体B,反应生成气体C和固体D,各物质的含量随时间的变化情况如图所示,下列说法错误的是
的恒容密闭容器中,充入一定量的气体A和气体B,反应生成气体C和固体D,各物质的含量随时间的变化情况如图所示,下列说法错误的是
A.该反应的化学方程式为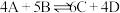 |
B. 内用D表示的化学反应速率: 内用D表示的化学反应速率: |
| C.反应体系内气体的密度不再发生变化说明反应达到平衡 |
D.该反应在 时改变的条件不可能是加入催化剂 时改变的条件不可能是加入催化剂 |
您最近一年使用:0次
名校
4 . 氨( )中氢含量高,是一种优良的储氢载体,可通过氨热分解法制氢气。在一定温度下,将
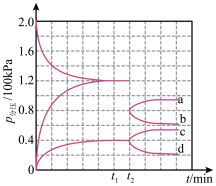
)中氢含量高,是一种优良的储氢载体,可通过氨热分解法制氢气。在一定温度下,将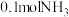 通入3L的刚性密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。下列说法错误的是
通入3L的刚性密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。下列说法错误的是
 )中氢含量高,是一种优良的储氢载体,可通过氨热分解法制氢气。在一定温度下,将
)中氢含量高,是一种优良的储氢载体,可通过氨热分解法制氢气。在一定温度下,将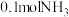 通入3L的刚性密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。下列说法错误的是
通入3L的刚性密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。下列说法错误的是
A. 时反应达到平衡, 时反应达到平衡, 时间内的反应速率 时间内的反应速率 |
B.该反应的平衡常数为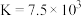 |
C. 时将容器容积迅速缩小至原来的一半并保持不变,曲线b表示压缩后 时将容器容积迅速缩小至原来的一半并保持不变,曲线b表示压缩后 分压的变化 分压的变化 |
D. 时加入催化剂可同时改变该反应的速率和 时加入催化剂可同时改变该反应的速率和 |
您最近一年使用:0次
2023-01-13更新
|
202次组卷
|
3卷引用:山东省临沂第一中学2021-2022学年高二上学期期末检测化学试题
名校
5 . 一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(s)⇌xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.1mol·L-1·s-1,同时生成1molD,下列叙述中不正确 的是
| A.反应达到平衡状态时A的转化率为60% |
| B.x=2 |
| C.减小容器的体积,反应物A的百分含量变小 |
| D.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为5∶6 |
您最近一年使用:0次
2022-10-26更新
|
77次组卷
|
2卷引用:山东省临沂市平邑县第一中学2022-2023学年高二上学期10月月考化学试题
13-14高二下·安徽·期中
名校
6 . T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论正确的是( )


| A.反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min) |
| B.容器中发生的反应可表示为:3X(g)+Y(g)⇌2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
您最近一年使用:0次
2020-06-29更新
|
113次组卷
|
4卷引用:2013-2014学年安徽师大附中高二下学期期中考查化学试卷
(已下线)2013-2014学年安徽师大附中高二下学期期中考查化学试卷2020届高三化学知识点强化训练—化学反应速率河南省许昌市长葛市第一高级中学2019-2020学年高二月考化学试题河南省长葛市第一高级中学2020-2021学年高二上学期阶段性测试试卷化学试题



