1 . 为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
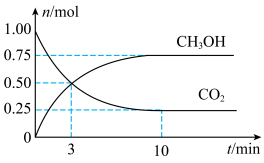
(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
(2)达到平衡时,H2的浓度为___________ mol·L-1。
(3)改变条件后,化学反应速率会减小的是___________(填字母)
(4)平衡时,CO2的体积分数为___________ %
(5)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为CO(g)+2H2(g)⇌CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)

(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=
(2)达到平衡时,H2的浓度为
(3)改变条件后,化学反应速率会减小的是___________(填字母)
| A.降低温度 | B.加入催化剂 | C.增大容器容积 | D.恒容下充入He |
(5)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为CO(g)+2H2(g)⇌CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________。(填字母)
| A.反应中CO与CH3OH的物质的量之比为1∶1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1molCO,同时生成1molCH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
您最近一年使用:0次
2 . 为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol CO2、3mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
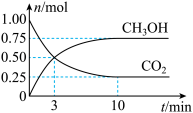
(1)在3min末,H2的浓度为_______ ,这时,反应速率 υ(正)_______ υ(逆)(选填>、<或 =)。
(2)从反应开始到平衡,平均反应速率υ(CO2)=_______ 。达到平衡时,H2的转化率为_______ 。
(3)下列措施不能提高反应速率的是_______。
(4)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:υ(H2)=0.3 mol∙L−1∙s−1;乙:υ(CO2)=0.12 mol∙L−1∙s−1;丙:υ(CH3OH)=4.8 mol∙L−1∙min−1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)在3min末,H2的浓度为
(2)从反应开始到平衡,平均反应速率υ(CO2)=
(3)下列措施不能提高反应速率的是_______。
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
您最近一年使用:0次
解题方法
3 . 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。合成氨反应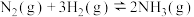

(1)在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内用N2表示的平均反应速率为_______ 。
(2)该反应平衡常数表达式为K=_______ ,在其他条件不变的情况下,若升高温度,平衡常数K会减小,则a_______ 0(填“大于”,“小于”或“等于”)。
(3)当该反应达到化学平衡时,如果此时向容器中增加氮气,平衡向_______ 移动(填“正反应方向”、“逆反应方向”、“不移动”),氮气的转化率会_______ (填“增大”、“不变”或“减小”)。使用催化剂反应的ΔH会_______ (填“增大”、“减小”或“不改变”)。
(4)恒温、恒压下,在一个容积可变的容器中,开始时放入1molN2和3molH2,达到平衡后生成了amolNH3。
①若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3amol,则开始时放入H2的物质的量为_______ mol(平衡时NH3的质量分数原平衡相同)。
②若开始时放入xmolN2、6molH2和2molNH3达到平衡后,N2和NH3的物质的量分别为ymol和3amol,则y=_______ 。平衡时H2的物质的量_______ (选填一个编号)。
A.大于6mol B.等于6mol C.小于6mol D.可能大于、小于或等于6mol
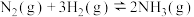

(1)在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内用N2表示的平均反应速率为
(2)该反应平衡常数表达式为K=
(3)当该反应达到化学平衡时,如果此时向容器中增加氮气,平衡向
(4)恒温、恒压下,在一个容积可变的容器中,开始时放入1molN2和3molH2,达到平衡后生成了amolNH3。
①若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3amol,则开始时放入H2的物质的量为
②若开始时放入xmolN2、6molH2和2molNH3达到平衡后,N2和NH3的物质的量分别为ymol和3amol,则y=
A.大于6mol B.等于6mol C.小于6mol D.可能大于、小于或等于6mol
您最近一年使用:0次
4 . CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷燃烧生成CO和液态水时放出38kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的 =
=___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。

①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的浓度为___________ mol/L。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(4)某种甲烷燃料电池的工作原理如图所示

甲烷通入的一极为电源的___________ 极,该电极反应式:___________ 当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)___________ L
(1)已知25℃、101kPa时,1g甲烷燃烧生成CO和液态水时放出38kJ热量,则该条件下反应2CH4(g)+3O2(g)=2CO(g)+4H2O(l)的
 =
=(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(4)某种甲烷燃料电池的工作原理如图所示

甲烷通入的一极为电源的
您最近一年使用:0次
5 . CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
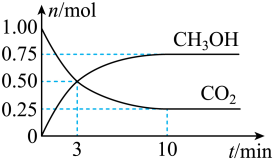
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的转化率为___________ 。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的转化率为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
您最近一年使用:0次
名校
6 . 向体积为2 L的固定密闭容器中通入2mol X气体,在一定温度下发生如下反应:2X(g)  Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
(1)用Y表示的化学反应速率为_____ ,X的转化率为______ ,平衡时反应吸收的热量为_________ 。
(2)在定温,定容的条件下向平衡体系中再充入1mol X(g)气体,平衡______ (填“正向”“不”“逆向”)移动, X(g)的转化率______ (填“增大”“减小”“不变”),Y(g)的质量分数______ (填“增大”“减小”“不变”)。
(3)在相同温度,相同容积的密闭容器中起始时充入0.8molX(g),0.6molY(g),1.8molZ(g),此时V正______ V逆(填“大于”、“小于”或“等于”);平衡时X(g)的百分含量______ (填“大于”、“小于”或“等于”)原平衡。
 Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。
Y(g)+3Z(g)ΔH=+92.0kJ· mol-1。经5 min 后反应达到平衡,此时测得容器内的压强为起始时的1.5倍。(1)用Y表示的化学反应速率为
(2)在定温,定容的条件下向平衡体系中再充入1mol X(g)气体,平衡
(3)在相同温度,相同容积的密闭容器中起始时充入0.8molX(g),0.6molY(g),1.8molZ(g),此时V正
您最近一年使用:0次
7 . Ⅰ。在下列事实中,什么因素影响了化学反应速率?
(1)集气瓶中有 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸___________ ;
黄铁矿煅烧时要粉碎成细小的矿粒。___________ ;
熔化的 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。___________ ;
夏天食品容易变质,冬天就不易发生该现象。___________ ;
同样大小的石灰石分别在 的盐酸和
的盐酸和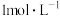 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。___________ 。
Ⅱ。某温度时,在 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量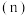 随时间
随时间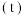 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析:___________ 。
(3)反应开始至 ,用
,用 表示的平均反应速率为
表示的平均反应速率为___________ 。此时, 的转化率为
的转化率为___________ 。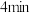 时,加入1体积
时,加入1体积 ,反应速率
,反应速率___________ (填“变大”、“变小”、“不变”)
(4)下列叙述不能说明上述反应达到化学平衡状态的是___________ (填序号)。
A. 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化
B. 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.
E.
F.单位时间内每消耗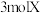 ,同时生成
,同时生成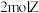
(1)集气瓶中有
 和
和 的混合气体,在瓶外点燃镁条时发生爆炸
的混合气体,在瓶外点燃镁条时发生爆炸黄铁矿煅烧时要粉碎成细小的矿粒。
熔化的
 放出气泡很慢,加入少量
放出气泡很慢,加入少量 后很快产生气体。
后很快产生气体。夏天食品容易变质,冬天就不易发生该现象。
同样大小的石灰石分别在
 的盐酸和
的盐酸和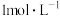 的盐酸中反应,反应速率不同。
的盐酸中反应,反应速率不同。Ⅱ。某温度时,在
 密闭容器中
密闭容器中 三种气态物质的物质的量
三种气态物质的物质的量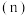 随时间
随时间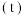 变化的曲线如图所示,由图中数据分析:
变化的曲线如图所示,由图中数据分析: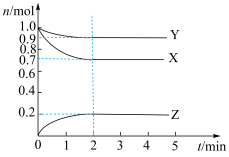
(3)反应开始至
 ,用
,用 表示的平均反应速率为
表示的平均反应速率为 的转化率为
的转化率为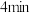 时,加入1体积
时,加入1体积 ,反应速率
,反应速率(4)下列叙述不能说明上述反应达到化学平衡状态的是
A.
 的物质的量不随时间变化而变化
的物质的量不随时间变化而变化 B.
 的质量分数不随时间变化而变化
的质量分数不随时间变化而变化C.混合气体的总物质的量不随时间变化而变化
D.

E.

F.单位时间内每消耗
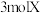 ,同时生成
,同时生成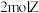
您最近一年使用:0次
名校
解题方法
8 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气器材的消毒,可由乙酸与 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: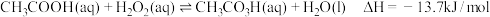
(1)市售过氧乙酸的浓度一般不超过21%,原因是___________ 。
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
(3)取质量相等的冰醋酸和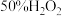 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
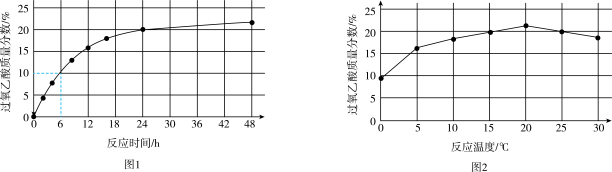
①实验1中,若反应混合液的总质量为 ,依据图1数据计算,在
,依据图1数据计算,在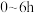 间,
间,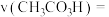
___________ 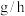 。(用含m的代数式表示)
。(用含m的代数式表示)
②综合图1、图2分析,与 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是___________ (写出2条)。
(4)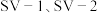 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
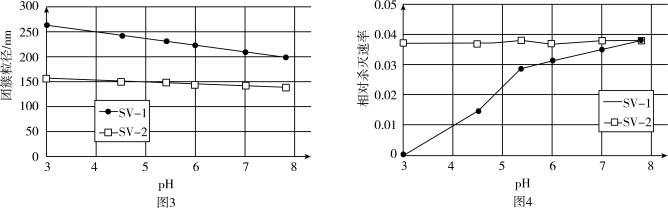
依据图3、图4分析,过氧乙酸对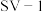 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是___________ 。
 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: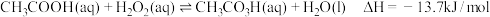
(1)市售过氧乙酸的浓度一般不超过21%,原因是
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
| A.降低温度 | B.增加 用量(溶液体积不变) 用量(溶液体积不变) |
| C.加水稀释溶液 | D.增加乙酸的用量(溶液体积不变) |
(3)取质量相等的冰醋酸和
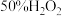 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。实验1:在
 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。

①实验1中,若反应混合液的总质量为
 ,依据图1数据计算,在
,依据图1数据计算,在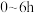 间,
间,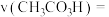
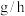 。(用含m的代数式表示)
。(用含m的代数式表示)②综合图1、图2分析,与
 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是(4)
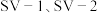 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
依据图3、图4分析,过氧乙酸对
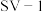 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是
您最近一年使用:0次
名校
解题方法
9 . 在一定温度下,将 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为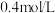 ,用C表示的反应速率为
,用C表示的反应速率为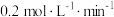 请填写下列空白:
请填写下列空白:
(1)x值等于___________ 。
(2)A的转化率为___________ 。
(3)如果增大反应体系的压强,则平衡体系中C的质量分数___________ (增大、减小或不变)。
(4)在此温度下,该化学反应的平衡常数K=___________ 。
(5)在此条件下,向该容器内加入 、
、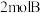 、
、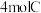 、
、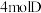 后,
后,
___________ (填“>”“<”或“=”) 。
。
(6)在此条件下, 末再向容器内加入
末再向容器内加入 、
、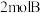 ,则平衡移动的方向
,则平衡移动的方向___________ ,再次达到平衡后A的转化率___________ (增大、减小或不变),C的物质的量分数___________ (增大、减小或不变)。
 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为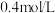 ,用C表示的反应速率为
,用C表示的反应速率为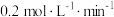 请填写下列空白:
请填写下列空白:(1)x值等于
(2)A的转化率为
(3)如果增大反应体系的压强,则平衡体系中C的质量分数
(4)在此温度下,该化学反应的平衡常数K=
(5)在此条件下,向该容器内加入
 、
、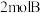 、
、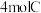 、
、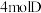 后,
后,
 。
。(6)在此条件下,
 末再向容器内加入
末再向容器内加入 、
、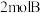 ,则平衡移动的方向
,则平衡移动的方向
您最近一年使用:0次
名校
10 . 研究化学反应的原理,对掌握物质的应用有重要的意义。
Ⅰ.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
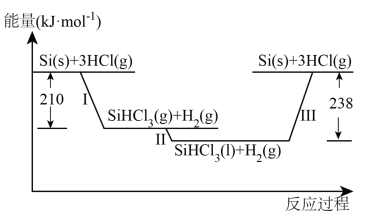
(1)工业上用 ,为原料制备粗硅。反应的化学方程式为
,为原料制备粗硅。反应的化学方程式为_______ 。
(2)反应Ⅲ生成2mol Si(s)时,_______ (填“吸收”或“放出”)_______ 热量。
(3)在2L密闭容器中投入过量Si(s)和3mol HCl(g)发生反应Ⅰ,经过t min反应达到平衡状态,测得容器中HCl的平衡浓度为0.6 。
。
①反应开始到t min,用HCl浓度变化表示的平均反应速率为_______  。
。
②下列叙述不能说明反应Ⅰ一定达到平衡状态的是_______ (填标号)。
A.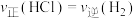 B.硅的质量保持不变
B.硅的质量保持不变
C.HCl的质量分数保持不变 D.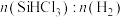 保持不变
保持不变
Ⅱ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
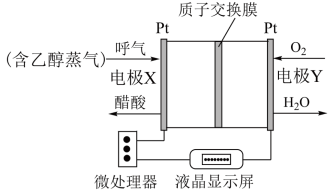
(4)电极X为_______ (填“正极”、“负极”)。
(5)电池工作时,质子通过交换膜_______ (填“从左到右”“从右到左”)迁移。
(6)正极的电极反应式为_______ 。
Ⅰ.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

(1)工业上用
 ,为原料制备粗硅。反应的化学方程式为
,为原料制备粗硅。反应的化学方程式为(2)反应Ⅲ生成2mol Si(s)时,
(3)在2L密闭容器中投入过量Si(s)和3mol HCl(g)发生反应Ⅰ,经过t min反应达到平衡状态,测得容器中HCl的平衡浓度为0.6
 。
。①反应开始到t min,用HCl浓度变化表示的平均反应速率为
 。
。②下列叙述不能说明反应Ⅰ一定达到平衡状态的是
A.
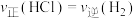 B.硅的质量保持不变
B.硅的质量保持不变C.HCl的质量分数保持不变 D.
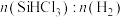 保持不变
保持不变Ⅱ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

(4)电极X为
(5)电池工作时,质子通过交换膜
(6)正极的电极反应式为
您最近一年使用:0次



