名校
1 . 某化学小组选用酸性高锰酸钾溶液和草酸( )溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
)溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
(1)实验原理的离子方程式:____________ 。
(2)实验2中的
______ ,目的是____________ 。
(3)根据上表中的实验数据,可以得到的结论是____________ 。
(4)利用实验1中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
______ mol/(L⋅min)。
 )溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:
)溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
a mol/L |
| 0.05 mol/L | 3 mol/L稀硫酸 | ||
1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
2 | 2.0 | v | 4.0 | 2.0 | 5.2 |
3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
(2)实验2中的

(3)根据上表中的实验数据,可以得到的结论是
(4)利用实验1中数据计算,用
 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
您最近一年使用:0次
2024-05-04更新
|
178次组卷
|
2卷引用:北京交大附中2023-2024学年高一下学期期中考试化学试题
名校
解题方法
2 . 工业制硫酸的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和足量O2,在催化剂、500℃的条件下发生反应。SO2、SO3的物质的量随时间的变化如图。下列说法不正确 的是
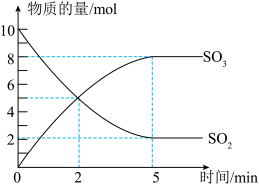
| A.在上述条件下,SO2不可能100%地转化为SO3 |
| B.反应到2min时,正逆反应速率相等 |
| C.反应开始至5min末,以SO2浓度的变化表示该反应的平均反应速率是0.8mol/(L·min) |
| D.使用催化剂是为了加快反应速率,提高生产效率 |
您最近一年使用:0次
2024-05-04更新
|
319次组卷
|
2卷引用:北京市陈经纶中学2023-2024学年高一下学期期中诊断化学试卷
3 . 氢能的开发和利用是推动我国能源结构转型,保障国家能源安全,实现“碳达峰”、“碳中和”目标的重要途径。目前,我国已成为世界第一大产氢国,主要有三类工业制氢路线:
(1)化工燃料重整制氢
已知:
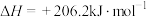

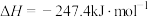
则 与
与 反应生成
反应生成 和
和 的反应热是
的反应热是___________  。
。
(2)工业副产氢
已知:工业上用水煤气法制氢气,有关化学方程式是:
反应一:

反应二:

①反应一在 时达到化学平衡状态,则此温度下该反应的平衡常数表达式
时达到化学平衡状态,则此温度下该反应的平衡常数表达式
___________ 。
②在 时将
时将 和
和 各
各 通入体积为
通入体积为 的密闭容器中反应发生反应二,
的密闭容器中反应发生反应二, 时达到平衡状态,该反应的平衡常数是9,则
时达到平衡状态,该反应的平衡常数是9,则 的转化率是
的转化率是___________ ,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率 是
是___________  。
。
(3)清洁能源电解制氢
已知:利用电解饱和食盐水可制得氢气,下图为电解装置示意图: 电极是极
电极是极___________ (填“阴”或“阳”), 电极的电极反应式
电极的电极反应式___________ 。
②假设室温条件下电解 饱和食盐水一段时间,当两极产生的气体共
饱和食盐水一段时间,当两极产生的气体共 (标准状况下)时,溶液的
(标准状况下)时,溶液的 为
为___________ (溶液体积没有变化)。
(1)化工燃料重整制氢
已知:

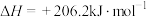

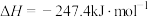
则
 与
与 反应生成
反应生成 和
和 的反应热是
的反应热是 。
。(2)工业副产氢
已知:工业上用水煤气法制氢气,有关化学方程式是:
反应一:


反应二:


①反应一在
 时达到化学平衡状态,则此温度下该反应的平衡常数表达式
时达到化学平衡状态,则此温度下该反应的平衡常数表达式
②在
 时将
时将 和
和 各
各 通入体积为
通入体积为 的密闭容器中反应发生反应二,
的密闭容器中反应发生反应二, 时达到平衡状态,该反应的平衡常数是9,则
时达到平衡状态,该反应的平衡常数是9,则 的转化率是
的转化率是 的浓度变化表示的反应速率
的浓度变化表示的反应速率 是
是 。
。(3)清洁能源电解制氢
已知:利用电解饱和食盐水可制得氢气,下图为电解装置示意图:

 电极是极
电极是极 电极的电极反应式
电极的电极反应式②假设室温条件下电解
 饱和食盐水一段时间,当两极产生的气体共
饱和食盐水一段时间,当两极产生的气体共 (标准状况下)时,溶液的
(标准状况下)时,溶液的 为
为
您最近一年使用:0次
名校
解题方法
4 . I.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小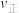
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(5)①本实验待测数据可以是___________ ,实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响﹔实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验发现 比实验
比实验 反应速率快,原因是
反应速率快,原因是___________ 。

 时刻,正逆反应速率大小
时刻,正逆反应速率大小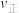
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g |  硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
 | 2.0 | 50.0 | 25 | 0 | 0 |
 | 2.0 | 40.0 | 25 | 0 | 10.0 |
 | 2.0 | 50.0 | 25 | 0.2 | 0 |
 | 2.0 | 50.0 | 35 | 0 | 0 |
(5)①本实验待测数据可以是
 和实验
和实验 可以探究
可以探究 和实验
和实验 可以探究
可以探究②实验发现
 比实验
比实验 反应速率快,原因是
反应速率快,原因是
您最近一年使用:0次
2024-04-28更新
|
329次组卷
|
2卷引用:安徽省合肥市六校联盟2023-2024学年高一下学期4月期中考试化学试题
2024高三下·全国·专题练习
5 . 在“碳达峰”“碳中和”的发展背景下, 催化加氢合成甲醇是重要的碳捕获利用与封
催化加氢合成甲醇是重要的碳捕获利用与封
存技术,该过程主要发生下列反应:
反应①

反应②

回答下列问题:
(1)①现向2L恒容密闭容器中加入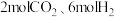 ,在恒温下发生上述反应。10s后反应达到平衡,此时容器内
,在恒温下发生上述反应。10s后反应达到平衡,此时容器内 的浓度为
的浓度为 ,CO为
,CO为 。则前10s内的平均反应速率
。则前10s内的平均反应速率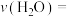
___________ 。
(2)0.5MPa下,将 的混合气体以一定流速通过装有催化剂的反应器,测得
的混合气体以一定流速通过装有催化剂的反应器,测得 的转化率、
的转化率、 或CO的选择性[
或CO的选择性[ ]以及
]以及 的产率(
的产率( 的转化率×
的转化率× 的选择性)随温度的变化如图2所示。
的选择性)随温度的变化如图2所示。___________ (填“ ”或“CO”)的选择性随温度的变化,270℃时,对应
”或“CO”)的选择性随温度的变化,270℃时,对应 的转化率为
的转化率为___________ ;在210~250℃之间, 的产率增大的原因是
的产率增大的原因是___________ 。
 催化加氢合成甲醇是重要的碳捕获利用与封
催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
反应①


反应②


回答下列问题:
(1)①现向2L恒容密闭容器中加入
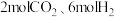 ,在恒温下发生上述反应。10s后反应达到平衡,此时容器内
,在恒温下发生上述反应。10s后反应达到平衡,此时容器内 的浓度为
的浓度为 ,CO为
,CO为 。则前10s内的平均反应速率
。则前10s内的平均反应速率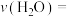
(2)0.5MPa下,将
 的混合气体以一定流速通过装有催化剂的反应器,测得
的混合气体以一定流速通过装有催化剂的反应器,测得 的转化率、
的转化率、 或CO的选择性[
或CO的选择性[ ]以及
]以及 的产率(
的产率( 的转化率×
的转化率× 的选择性)随温度的变化如图2所示。
的选择性)随温度的变化如图2所示。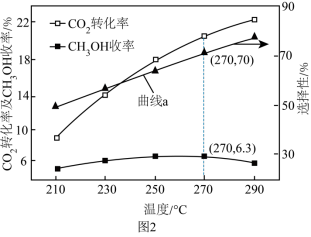
 ”或“CO”)的选择性随温度的变化,270℃时,对应
”或“CO”)的选择性随温度的变化,270℃时,对应 的转化率为
的转化率为 的产率增大的原因是
的产率增大的原因是
您最近一年使用:0次
2024高三下·全国·专题练习
6 . 某科研团队利用 和
和 反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
(1) 均为
均为 的恒容密闭容器,向
的恒容密闭容器,向 容器中充入
容器中充入 和
和 ,向
,向 容器中充入
容器中充入 和
和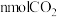 ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: ,测得
,测得 的平衡转化率随温度的变化如图甲所示。
的平衡转化率随温度的变化如图甲所示。 容器中在温度为
容器中在温度为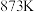 时,
时, 到达
到达 点,用
点,用 表示
表示 内的化学反应速率为
内的化学反应速率为
___________ ,此时的化学平衡常数 为
为___________ (保留两位小数),若在此温度下时向 容器的平衡体系中再充入
容器的平衡体系中再充入 各
各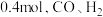 各
各 ,重新达到平衡前,
,重新达到平衡前,
___________  (填“
(填“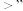 “
“ ”或
”或 )。
)。
② 点时该反应的平衡常数为
点时该反应的平衡常数为 ,则
,则
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③ 两点处容器内气体总压强分别是
两点处容器内气体总压强分别是 ,则
,则 的大小顺序为
的大小顺序为___________ 。
 和
和 反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:
反应使之转化为水煤气,对争取2060年前实现“碳中和”、减缓燃料危机和减轻温室效应具有重要的意义。请回答下列问题:(1)
 均为
均为 的恒容密闭容器,向
的恒容密闭容器,向 容器中充入
容器中充入 和
和 ,向
,向 容器中充入
容器中充入 和
和 ,在催化剂存在下发生反应:
,在催化剂存在下发生反应: ,测得
,测得 的平衡转化率随温度的变化如图甲所示。
的平衡转化率随温度的变化如图甲所示。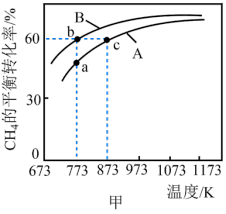
 容器中在温度为
容器中在温度为 时,
时, 到达
到达 点,用
点,用 表示
表示 内的化学反应速率为
内的化学反应速率为
 为
为 容器的平衡体系中再充入
容器的平衡体系中再充入 各
各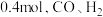 各
各 ,重新达到平衡前,
,重新达到平衡前,
 (填“
(填“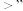 “
“ ”或
”或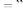 )。
)。②
 点时该反应的平衡常数为
点时该反应的平衡常数为 ,则
,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③
 两点处容器内气体总压强分别是
两点处容器内气体总压强分别是 ,则
,则 的大小顺序为
的大小顺序为
您最近一年使用:0次
2024高三下·全国·专题练习
7 .  是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
(1)650K时,某研究小组测得反应i: 的浓度、速率数据如下:
的浓度、速率数据如下:
已知k为速率常数,一般情况下只与温度有关,实验测得
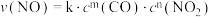 ,通过以上实验数据可知
,通过以上实验数据可知
___________ ,
___________ ;650K时,若 ,
, ,
,
___________  。
。
 是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。(1)650K时,某研究小组测得反应i:
 的浓度、速率数据如下:
的浓度、速率数据如下:| 实验编号 | 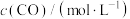 |  |  |
| ① | 0.025 | 0.040 | 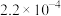 |
| ② | 0.050 | 0.040 |  |
| ③ | 0.025 | 0.120 |  |
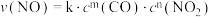 ,通过以上实验数据可知
,通过以上实验数据可知

 ,
, ,
,
 。
。
您最近一年使用:0次
2024高三下·全国·专题练习
8 . 一定条件下,水气变换反应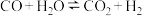 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:
I.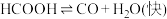
II.
研究发现,在反应I、II中, 仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)反应I正反应速率方程为: ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为___________  ,此时反应I的反应速率
,此时反应I的反应速率
___________  (用含
(用含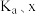 和k的代数式表示)。
和k的代数式表示)。
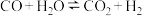 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:I.
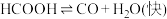
II.

研究发现,在反应I、II中,
 仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:(1)反应I正反应速率方程为:
 ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为 ,此时反应I的反应速率
,此时反应I的反应速率
 (用含
(用含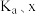 和k的代数式表示)。
和k的代数式表示)。
您最近一年使用:0次
名校
9 . 一定温度下,在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示。下列叙述中正确的是
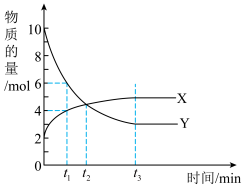
A.反应的化学方程式为 |
| B.t1min时,Y的浓度是X浓度的1.5倍 |
| C.t2min时,正、逆反应速率相等 |
| D.Y的反应速率:t1时刻<t2时刻<t3时刻 |
您最近一年使用:0次
10 . 甲醇是一种可再生的清洁能源,以甲醇为原料制备氢气的原理为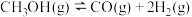 。
。
(1)已知相关物质的标准燃烧热(25℃,101kPa)如表所示,则上述反应的
_____  。
。
(2)中国石油大学陈玉教授团队研究了 在催化剂Pd/MgO(100)表面的催化反应机理,其部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,过渡态用TS表示):
在催化剂Pd/MgO(100)表面的催化反应机理,其部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,过渡态用TS表示):_____ eV,决速步骤的化学方程式为_____ 。
(3)一定温度下,维持100kPa,将 与Ar(g)以一定比例
与Ar(g)以一定比例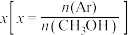 投料发生上述反应,测得
投料发生上述反应,测得 的平衡转化率及
的平衡转化率及 的分压
的分压 随x的变化关系如图所示:
随x的变化关系如图所示: 为用气体分压表示的平衡常数,分压=总压×物质的量分数。
为用气体分压表示的平衡常数,分压=总压×物质的量分数。
①图中表示 的平衡转化率随x变化的曲线为
的平衡转化率随x变化的曲线为_____ (填“A”或“B”),判断理由是_____ 。
②当x=1时,平衡体系中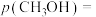
_____ kPa.
③若正、逆反应速率方程分别为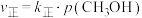 、
、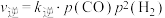 ,
, 、
、 分别为正、逆反应的速率常数,则该反应的平衡常数
分别为正、逆反应的速率常数,则该反应的平衡常数
_____ (用 、
、 表示),当x=5,
表示),当x=5,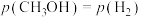 时,
时,
_____ 。
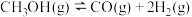 。
。(1)已知相关物质的标准燃烧热(25℃,101kPa)如表所示,则上述反应的

 。
。| 物质 |  |  |  |
标准燃烧热( ) ) |  | 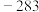 |  |
(2)中国石油大学陈玉教授团队研究了
 在催化剂Pd/MgO(100)表面的催化反应机理,其部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,过渡态用TS表示):
在催化剂Pd/MgO(100)表面的催化反应机理,其部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,过渡态用TS表示):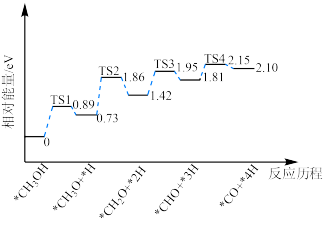
(3)一定温度下,维持100kPa,将
 与Ar(g)以一定比例
与Ar(g)以一定比例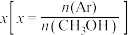 投料发生上述反应,测得
投料发生上述反应,测得 的平衡转化率及
的平衡转化率及 的分压
的分压 随x的变化关系如图所示:
随x的变化关系如图所示:
 为用气体分压表示的平衡常数,分压=总压×物质的量分数。
为用气体分压表示的平衡常数,分压=总压×物质的量分数。①图中表示
 的平衡转化率随x变化的曲线为
的平衡转化率随x变化的曲线为②当x=1时,平衡体系中
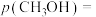
③若正、逆反应速率方程分别为
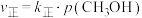 、
、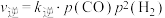 ,
, 、
、 分别为正、逆反应的速率常数,则该反应的平衡常数
分别为正、逆反应的速率常数,则该反应的平衡常数
 、
、 表示),当x=5,
表示),当x=5,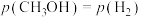 时,
时,
您最近一年使用:0次
2024-04-16更新
|
307次组卷
|
4卷引用:压轴题13?化学反应原理综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
(已下线)压轴题13?化学反应原理综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届四川省雅安市天全中学高三下学期模拟预测化学试题福建省漳州市2024届高三下学期毕业班第三次质量检测三模化学试题(已下线)T13-原理综合题




