名校
1 .  .在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
(5)下列叙述中,能说明该反应达到平衡状态的是___________。
 .某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(6)①本实验待测数据可以是___________ ,实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验 和实验
和实验 的目的是
的目的是___________ 。
(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中
___________ 。
 .在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
 时刻,正逆反应速率大小
时刻,正逆反应速率大小
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)如果升高温度,则

(5)下列叙述中,能说明该反应达到平衡状态的是___________。
| A.单位时间内每消耗1mol N,同时生成0.5mol M |
| B.气体M的体积分数不再变化 |
| C.混合气体的密度不再变化 |
| D.混合气体的平均相对分子质量不再变化 |
 .某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:| 序号 | 纯锌粉/g |  硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
 | 2.0 | 50.0 | 25 | 0 | 0 |
 | 2.0 | 40.0 | 25 | 0 | 10.0 |
 | 2.0 | 50.0 | 25 | 0.2 | 0 |
 | 2.0 | 50.0 | 25 | 4.0 | 0 |
(6)①本实验待测数据可以是
 和实验
和实验 可以探究
可以探究②实验
 和实验
和实验 的目的是
的目的是(7)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | V | 40 | 4.0 | 2.0 |

您最近一年使用:0次
名校
2 . 回答下列问题:
I.硫酸是重要的化工原料,工业制硫酸的其中一步重要反应是
 放热反应
放热反应
一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。 的平均反应速率为
的平均反应速率为_______ 。
(2)图中a点,正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
(3)当反应达到平衡时, 的转化率为
的转化率为_______ %。
(4)下列能说明反应一定已达平衡的是_______(填标号)。
(5)下列说法错误的是_______(填标号)。
II.燃料电池能有效提高能源利用率。
(6)写出甲醇 空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式
空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式_______ 。
I.硫酸是重要的化工原料,工业制硫酸的其中一步重要反应是
 放热反应
放热反应一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。

 的平均反应速率为
的平均反应速率为(2)图中a点,正反应速率
(3)当反应达到平衡时,
 的转化率为
的转化率为(4)下列能说明反应一定已达平衡的是_______(填标号)。
| A.混合气体的密度不再变化 | B. 质量保持不变 质量保持不变 |
C. | D. 、 、 和 和 的物质的量之比为2:1:2 的物质的量之比为2:1:2 |
(5)下列说法错误的是_______(填标号)。
| A.提高反应时的温度,正反应的速率加快,逆反应的速率减慢 |
B.提高反应时的温度,可以实现 的完全转化 的完全转化 |
| C.通过调控反应条件,可以提高该反应进行的程度 |
| D.使用催化剂是为了增大反应速率,提高生产效率 |
II.燃料电池能有效提高能源利用率。
(6)写出甲醇
 空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式
空气燃料电池在碱性条件(KOH溶液)中的负极电极反应式
您最近一年使用:0次
3 . 根据要求,回答下列问题:
(1)为比较 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察______ (填实验现象),即可得出 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是______  和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:
上述反应的离子方程式为______ ,该实验是探究______ 对反应速率的影响。
(3)工业制硫酸的反应之一为 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。 的平均反应速率为
的平均反应速率为______ 。
(2)A点的
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)为比较
 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是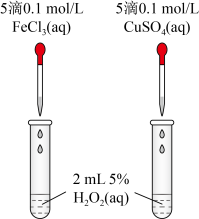
 和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:实验序号 | 草酸溶液 | 酸性高锰酸钾溶液 |
① |
|
|
② |
|
|
(3)工业制硫酸的反应之一为
 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。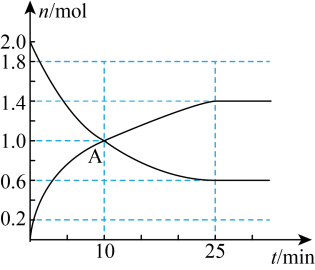
 的平均反应速率为
的平均反应速率为(2)A点的

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
4 . 在2L恒容密闭容器中,通入1mol X、0.6mol Y,发生反应: ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是
 ,2min末,测得Z、W的浓度分别为
,2min末,测得Z、W的浓度分别为 、
、 ,则下列说法错误的是
,则下列说法错误的是A. | B.反应过程中混合气体的平均相对分子质量不变 |
C.0~2min内,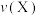 为 为 | D.2min末,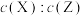 等于8∶3 等于8∶3 |
您最近一年使用:0次
5 . 一定温度下,向2.0L恒容密闭容器中充入1.0mol ,发生反应:
,发生反应: 。反应中测定的部分数据见下表:
。反应中测定的部分数据见下表:
下列说法错误的是
 ,发生反应:
,发生反应: 。反应中测定的部分数据见下表:
。反应中测定的部分数据见下表:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 时,正反应速率最大,逆反应速率为0 时,正反应速率最大,逆反应速率为0 |
| B.150s时,正反应速率大于逆反应速率 |
C.250s时,反应恰好达到平衡, 的转化率为20% 的转化率为20% |
D.当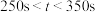 时,反应处于停止状态 时,反应处于停止状态 |
您最近一年使用:0次
解题方法
6 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是___________ 。
A.充入He使容器压强增大,能提高反应速率
B.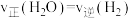 ,说明反应达到平衡状态
,说明反应达到平衡状态
C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为___________ 。
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为___________ ,N2的转化率为___________ ,欲提高合成氨的反应速率可采取的措施为___________ 。(任意答2点)
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为___________ 。
 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。

| A.铝粉与氧化铁的反应 |
B.氯化铵与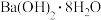 的反应 的反应 |
C.锌片与稀硫酸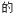 反应 反应 |
| D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是
A.充入He使容器压强增大,能提高反应速率
B.
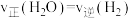 ,说明反应达到平衡状态
,说明反应达到平衡状态C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为
您最近一年使用:0次
解题方法
7 . 为实现碳中和,研究人员开发了双功能催化剂,它具有吸收二氧化碳和将其吸收的二氧化碳与氢气反应转化为甲烷的功能,过程中发生的反应为 。已知:断开
。已知:断开 物质中的化学键所要吸收的能量(单位:
物质中的化学键所要吸收的能量(单位: )如表。
)如表。
(1)若每生成 甲烷,则该反应
甲烷,则该反应______ (填“放出”或“吸收”)______  能量。
能量。 的密闭容器中充入
的密闭容器中充入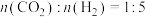 的混合气体,发生上述反应,
的混合气体,发生上述反应,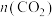 与
与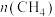 随时间的变化如图所示。
随时间的变化如图所示。
① 内,用
内,用 表示该反应的平均反应速率
表示该反应的平均反应速率
______  ,反应达到平衡状态时,
,反应达到平衡状态时,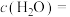
______  。
。
② 、
、 两点用
两点用 表示的化学反应速率:
表示的化学反应速率:
______ (填“>”“<”或“=”)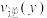 。
。
③下列说法正确的是______ (填字母)。
A. 后该反应停止
后该反应停止
B.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
C. 时,
时,
D.若改变催化剂,则反应达到平衡状态所需的时间一定小于
 。已知:断开
。已知:断开 物质中的化学键所要吸收的能量(单位:
物质中的化学键所要吸收的能量(单位: )如表。
)如表。物质 |
|
|
|
|
吸收的能量 | 1490 | 436 | 1652 | 926 |
(1)若每生成
 甲烷,则该反应
甲烷,则该反应 能量。
能量。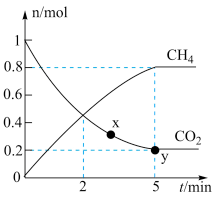
 的密闭容器中充入
的密闭容器中充入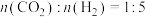 的混合气体,发生上述反应,
的混合气体,发生上述反应,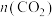 与
与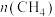 随时间的变化如图所示。
随时间的变化如图所示。①
 内,用
内,用 表示该反应的平均反应速率
表示该反应的平均反应速率
 ,反应达到平衡状态时,
,反应达到平衡状态时,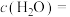
 。
。②
 、
、 两点用
两点用 表示的化学反应速率:
表示的化学反应速率:
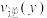 。
。③下列说法正确的是
A.
 后该反应停止
后该反应停止B.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
C.
 时,
时,
D.若改变催化剂,则反应达到平衡状态所需的时间一定小于

您最近一年使用:0次
8 . 试分析有关化学反应速率问题。
(1)某反应在体积为 的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知
的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知 均为气体)。
均为气体)。___________ 。
②反应开始至 时,B的平均反应速率为
时,B的平均反应速率为___________ 。
③平衡时A的转化率为___________ 。
(2)下表是某学习兴趣小组,一定条件下测定 在水溶液中分解浓度减少一半所需时间。已知:
在水溶液中分解浓度减少一半所需时间。已知: 的起始浓度为
的起始浓度为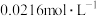 。
。
①在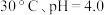 条件下,
条件下, 的分解速率为
的分解速率为___________ 。
② 增大能加速
增大能加速 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是___________ 。
③根据表中数据,推测 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为___________ (填序号)。
a.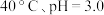 b.
b.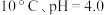 c.
c.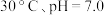
(1)某反应在体积为
 的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知
的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知 均为气体)。
均为气体)。
②反应开始至
 时,B的平均反应速率为
时,B的平均反应速率为③平衡时A的转化率为
(2)下表是某学习兴趣小组,一定条件下测定
 在水溶液中分解浓度减少一半所需时间。已知:
在水溶液中分解浓度减少一半所需时间。已知: 的起始浓度为
的起始浓度为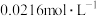 。
。
| 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
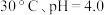 条件下,
条件下, 的分解速率为
的分解速率为②
 增大能加速
增大能加速 分解,表明对
分解,表明对 分解起催化作用的是
分解起催化作用的是③根据表中数据,推测
 在下列条件下分解速率依次增大的顺序为
在下列条件下分解速率依次增大的顺序为a.
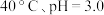 b.
b.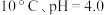 c.
c.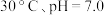
您最近一年使用:0次
名校
9 . 已知反应: ,其浓度数据如下:
,其浓度数据如下:

当用Y浓度的减少来表示该化学反应的速率时,其速率为
 ,其浓度数据如下:
,其浓度数据如下:
当用Y浓度的减少来表示该化学反应的速率时,其速率为
A.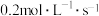 | B.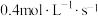 |
C.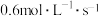 | D. |
您最近一年使用:0次
2024-04-23更新
|
120次组卷
|
2卷引用:云南省临沧市沧源佤族自治县民族中学2022-2023学年高二上学期第二次月考化学试题
解题方法
10 . 研究化学反应中的能量变化可以为提高工业生产效率提供指导性的理论依据。请结合所学化学反应原理相关知识回答下列问题:
(1)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
计算可得:

_______ 
②通过盖斯定律计算。已知:
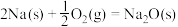
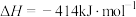

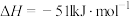
写出Na2O2与Na反应生成Na2O的热化学方程式:_______ 。
(2)实现“节能减排”和“低碳经济”的一项重要课题就是将CO2转化为可利用的资源,工业上有一种方法是用CO2来生产燃料甲醇。
已知:
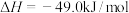 ,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
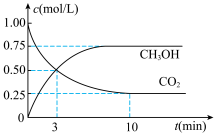
①甲醇中的官能团名称为_______ 。
②反应开始至平衡时,反应速率
_______ mol/(L⋅min)。CO2的平衡转化率为_______ 。
③为了加快化学反应速率,只改变下列某一条件,可采取的措施有_______ (填序号)。
A.升高温度 B.扩大容器体积 C.再充入CO2气体 D.使用合适的催化剂
(1)计算化学反应中的能量变化有多种途径。
①通过化学键的键能计算。已知:
| 化学键 | H—H | Cl—Cl | H—Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |



②通过盖斯定律计算。已知:
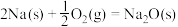
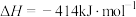

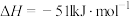
写出Na2O2与Na反应生成Na2O的热化学方程式:
(2)实现“节能减排”和“低碳经济”的一项重要课题就是将CO2转化为可利用的资源,工业上有一种方法是用CO2来生产燃料甲醇。
已知:

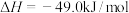 ,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
,在一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2气体和CH3OH(g))的浓度随时间变化曲线如图所示。
①甲醇中的官能团名称为
②反应开始至平衡时,反应速率

③为了加快化学反应速率,只改变下列某一条件,可采取的措施有
A.升高温度 B.扩大容器体积 C.再充入CO2气体 D.使用合适的催化剂
您最近一年使用:0次

 、20mL
、20mL 、30mL
、30mL 、20mL
、20mL /mol
/mol