名校
解题方法
1 . 化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,请回答下列问题。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:___________ (选填“吸热”或“放热)反应。
(2)在容积为 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。___________ (填“a”、“b”、“c”或“d”);用同一物质表示反应速率时,a、c两点的正反应速率: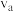
___________ 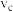 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率___________ 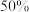 。
。
(3)甲烷燃料电池装置如图所示,通入 的电极为电池的
的电极为电池的___________ (填“正极”或“负极”),通入氧气一端电极反应方程式为___________ ,当有 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是___________ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

(2)在容积为
 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。
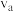
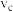 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率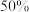 。
。(3)甲烷燃料电池装置如图所示,通入
 的电极为电池的
的电极为电池的 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是
您最近一年使用:0次
名校
2 . 在 密闭容器中充入
密闭容器中充入 气体和
气体和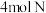 气体,在一定条件下发生反应:
气体,在一定条件下发生反应: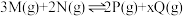 ,
, 时,生成了
时,生成了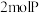 ,经测定,Q的浓度为
,经测定,Q的浓度为 ,下列判断正确的是
,下列判断正确的是
 密闭容器中充入
密闭容器中充入 气体和
气体和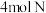 气体,在一定条件下发生反应:
气体,在一定条件下发生反应: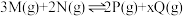 ,
, 时,生成了
时,生成了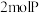 ,经测定,Q的浓度为
,经测定,Q的浓度为 ,下列判断正确的是
,下列判断正确的是A. |
B.反应开始后的 内 内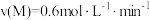 |
C.N的转化率为 |
D. 时,在相同温度下容器内混合气体的压强是反应前的 时,在相同温度下容器内混合气体的压强是反应前的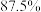 |
您最近一年使用:0次
名校
解题方法
3 . 对于可逆反应 ,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
 ,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是A.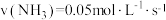 | B.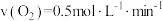 |
C. | D. |
您最近一年使用:0次
名校
解题方法
4 . 乙烯作为现代有机合成的重要原料,研究其制备方法具有重要的意义。
回答下列问题:
I.乙烷制备乙烯
(1)某温度、 下,向反应器中充入
下,向反应器中充入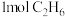 只发生反应
只发生反应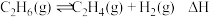 ,
, 的平衡转化率为
的平衡转化率为 ;保持温度和压强不变,向反应器中再充入水蒸气,
;保持温度和压强不变,向反应器中再充入水蒸气, 后达到平衡,此时
后达到平衡,此时 的平衡转化率为
的平衡转化率为 ,需要向反应器中充入
,需要向反应器中充入___________  水蒸气;用压强变化表示的
水蒸气;用压强变化表示的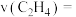
___________  ;此时该反应的
;此时该反应的
___________ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压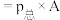 的物质的量分数)。
的物质的量分数)。
(2) 为一种选择性交换膜,其结构如图所示,其中第二周期组成元素的第二电离能与第一电离能差值最大的是
为一种选择性交换膜,其结构如图所示,其中第二周期组成元素的第二电离能与第一电离能差值最大的是___________ (填元素符号),结构中1处 的键角
的键角___________ (填“大于”“小于”或“等于”)2处 的键角。
的键角。
在催化剂作用下,二氧化碳可制取乙烯,发生以下反应:
①
②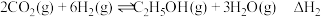
③
(3)
___________  。
。
(4)若将 和
和 按物质的量之比
按物质的量之比 混合,在
混合,在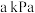 恒压反应器中连续反应,测得
恒压反应器中连续反应,测得 的转化率与
的转化率与 、
、 的选择性随温度变化如图所示。
的选择性随温度变化如图所示。 的转化率曲线是
的转化率曲线是___________ (填“X”“Y”或“Z”,下同), 的选择性曲线是
的选择性曲线是___________ ,说明判断依据:___________ 。
回答下列问题:
I.乙烷制备乙烯
(1)某温度、
 下,向反应器中充入
下,向反应器中充入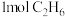 只发生反应
只发生反应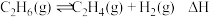 ,
, 的平衡转化率为
的平衡转化率为 ;保持温度和压强不变,向反应器中再充入水蒸气,
;保持温度和压强不变,向反应器中再充入水蒸气, 后达到平衡,此时
后达到平衡,此时 的平衡转化率为
的平衡转化率为 ,需要向反应器中充入
,需要向反应器中充入 水蒸气;用压强变化表示的
水蒸气;用压强变化表示的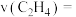
 ;此时该反应的
;此时该反应的
 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压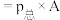 的物质的量分数)。
的物质的量分数)。(2)
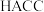 为一种选择性交换膜,其结构如图所示,其中第二周期组成元素的第二电离能与第一电离能差值最大的是
为一种选择性交换膜,其结构如图所示,其中第二周期组成元素的第二电离能与第一电离能差值最大的是 的键角
的键角 的键角。
的键角。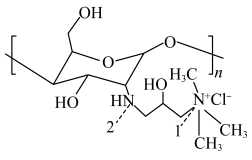
在催化剂作用下,二氧化碳可制取乙烯,发生以下反应:
①

②
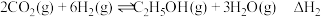
③

(3)

 。
。(4)若将
 和
和 按物质的量之比
按物质的量之比 混合,在
混合,在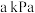 恒压反应器中连续反应,测得
恒压反应器中连续反应,测得 的转化率与
的转化率与 、
、 的选择性随温度变化如图所示。
的选择性随温度变化如图所示。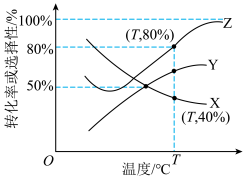
 的转化率曲线是
的转化率曲线是 的选择性曲线是
的选择性曲线是
您最近一年使用:0次
名校
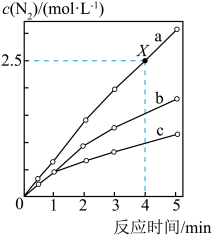
5 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近一年使用:0次
2024-04-26更新
|
44次组卷
|
2卷引用:甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 一定温度下,在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示。下列叙述中正确的是
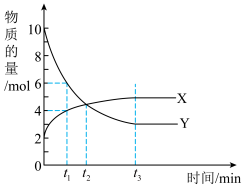
A.反应的化学方程式为 |
| B.t1min时,Y的浓度是X浓度的1.5倍 |
| C.t2min时,正、逆反应速率相等 |
| D.Y的反应速率:t1时刻<t2时刻<t3时刻 |
您最近一年使用:0次
名校
7 . 工业上,常用离子交换法软化自来水,其原理是 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中
。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是
 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中
。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是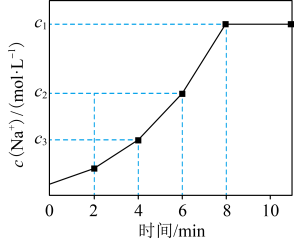
| A.反应达到平衡后,加入少量NaCl,离子交换反应的平衡常数减小 |
| B.6 min时的逆反应速率大于4 min时的逆反应速率 |
| C.其他条件不变时,10 min时离子交换反应已停止 |
D.4~8 min内平均反应速率: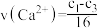 mol⋅L mol⋅L ⋅min ⋅min |
您最近一年使用:0次
2024-04-10更新
|
421次组卷
|
3卷引用:甘肃省靖远县2024届高三下学期第三次联考化学试题
名校
解题方法
8 . 某反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的化学反应速率为
| A.0.01mol/(L·s) | B.0.04mol/(L·s) | C.0.08mol/(L·s) | D.0.05mol/(L·s) |
您最近一年使用:0次
2024-04-05更新
|
482次组卷
|
2卷引用:甘肃省白银市会宁县第四中学2023-2024学年高二上学期第一次月考化学试题
名校
9 . 将足量固体NH4Br置于1L密闭容器中,在一定温度下发生下列反应:
① ;②
;②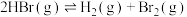 。
。
10min后达到平衡时,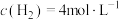 ,
,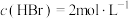 ,下列有关说法中错误的是
,下列有关说法中错误的是
①
 ;②
;②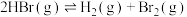 。
。10min后达到平衡时,
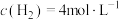 ,
,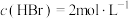 ,下列有关说法中错误的是
,下列有关说法中错误的是A.10min内反应①速率为 |
B.当体系中 不再改变,说明反应达到平衡状态 不再改变,说明反应达到平衡状态 |
| C.该温度下,反应①的平衡常数为20 |
| D.加入NH4Br固体,平衡不移动 |
您最近一年使用:0次
名校
10 . 在一定温度下,向1L的密闭容器中通入1mol 和
和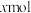
 ,发生反应:
,发生反应:
 ,起始时总压强为25.0MPa,
,起始时总压强为25.0MPa, 点时总压强为17.0MPa,并且测得一定时间内
点时总压强为17.0MPa,并且测得一定时间内 的转化率随温度的变化如图所示,下列说法错误的是
的转化率随温度的变化如图所示,下列说法错误的是
 和
和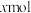
 ,发生反应:
,发生反应:
 ,起始时总压强为25.0MPa,
,起始时总压强为25.0MPa, 点时总压强为17.0MPa,并且测得一定时间内
点时总压强为17.0MPa,并且测得一定时间内 的转化率随温度的变化如图所示,下列说法错误的是
的转化率随温度的变化如图所示,下列说法错误的是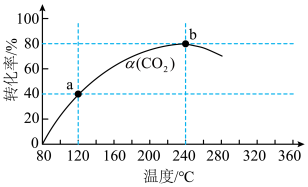
A.20min反应到达a点,在0~20min内的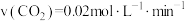 |
B.反应开始时,投入的 的物质的量x=4 的物质的量x=4 |
C.240℃时,该反应的化学平衡常数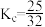 |
| D.a点和b点,温度对化学平衡的影响结果相反 |
您最近一年使用:0次



