1 . 一定条件下, 、
、 、
、 三种气体在某恒容密闭容器中发生反应,各气体的浓度随时间变化的曲线如图所示。
三种气体在某恒容密闭容器中发生反应,各气体的浓度随时间变化的曲线如图所示。 内该反应共吸收了
内该反应共吸收了 (
( )能量。下列说法不正确的是
)能量。下列说法不正确的是
 、
、 、
、 三种气体在某恒容密闭容器中发生反应,各气体的浓度随时间变化的曲线如图所示。
三种气体在某恒容密闭容器中发生反应,各气体的浓度随时间变化的曲线如图所示。 内该反应共吸收了
内该反应共吸收了 (
( )能量。下列说法不正确的是
)能量。下列说法不正确的是
A.达到平衡时, 的浓度不再变化 的浓度不再变化 |
B.反应的化学方程式为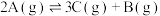 |
C.该条件下,达到平衡时, 的转化率为 的转化率为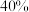 |
D.由图可知, 内, 内, 的反应速率为 的反应速率为 |
您最近一年使用:0次
2 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

您最近一年使用:0次
名校
解题方法
3 . 能源是现代文明的动力,科学家致力于开辟新能源和提高能源的利用率。如图所示的过程是目前直接利用太阳能的研究热点,人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。______ 能。
(2)甲烷是重要的燃料,在空气中燃烧发生反应: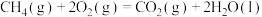 。
。
已知: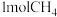 完全燃烧时生成
完全燃烧时生成 和
和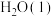 时放出
时放出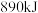 热量;其中,破坏
热量;其中,破坏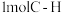 键、
键、 键分别需要吸收
键分别需要吸收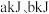 的能量,形成
的能量,形成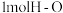 键能释放
键能释放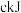 的能量
的能量
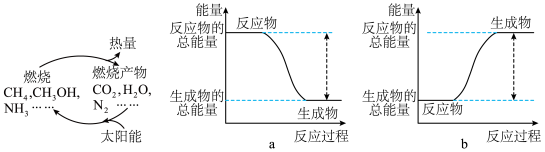
①如图能正确表示甲烷燃烧这一反应中能量变化的是______ (填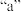 或
或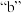 )。
)。
②形成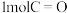 键能释放
键能释放______ 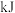 的能量(用含
的能量(用含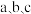 的式子表示)。
的式子表示)。
(3)用人工光合作用得到的甲烷、氧气和 溶液制作燃料电池。装置如图所示:
溶液制作燃料电池。装置如图所示:______ 极(填“正”或“负”)。
②正极发生的电极反应式为______ 。
③当转移 电子时,需要消耗标况下的氧气体积是
电子时,需要消耗标况下的氧气体积是______  。
。
(4)人工光合作用的途径之一就是在一定条件下,将 和
和 转化为甲醇
转化为甲醇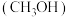 ,该反应的化学方程式为
,该反应的化学方程式为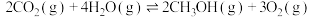 。一定条件下,在
。一定条件下,在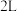 密闭容器中进行上述反应,测得
密闭容器中进行上述反应,测得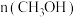 随时间的变化如表所示。则用
随时间的变化如表所示。则用 表示
表示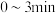 内该反应的平均反应速率为
内该反应的平均反应速率为______ 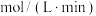 。
。
(2)甲烷是重要的燃料,在空气中燃烧发生反应:
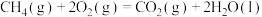 。
。已知:
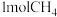 完全燃烧时生成
完全燃烧时生成 和
和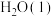 时放出
时放出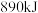 热量;其中,破坏
热量;其中,破坏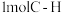 键、
键、 键分别需要吸收
键分别需要吸收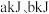 的能量,形成
的能量,形成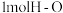 键能释放
键能释放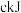 的能量
的能量①如图能正确表示甲烷燃烧这一反应中能量变化的是
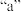 或
或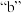 )。
)。②形成
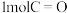 键能释放
键能释放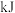 的能量(用含
的能量(用含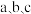 的式子表示)。
的式子表示)。(3)用人工光合作用得到的甲烷、氧气和
 溶液制作燃料电池。装置如图所示:
溶液制作燃料电池。装置如图所示: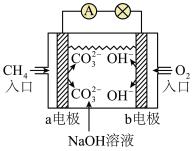
②正极发生的电极反应式为
③当转移
 电子时,需要消耗标况下的氧气体积是
电子时,需要消耗标况下的氧气体积是 。
。(4)人工光合作用的途径之一就是在一定条件下,将
 和
和 转化为甲醇
转化为甲醇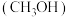 ,该反应的化学方程式为
,该反应的化学方程式为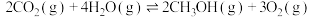 。一定条件下,在
。一定条件下,在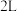 密闭容器中进行上述反应,测得
密闭容器中进行上述反应,测得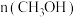 随时间的变化如表所示。则用
随时间的变化如表所示。则用 表示
表示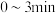 内该反应的平均反应速率为
内该反应的平均反应速率为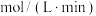 。
。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0 | 0.040 | 0.070 | 0.080 | 0.085 | 0.085 |
您最近一年使用:0次
2024-04-07更新
|
490次组卷
|
2卷引用:广西省钦州市第四中学2023-2024学年高三下学期第八周考试化学试卷
4 . 硅元素更是无机非金属材料的主角,无机非金属材料与人类社会的发展与进步息息相关。
Ⅰ.建筑领域的基石材料-硅酸盐
(1)烧制普通玻璃的原料是________ ,使用HF溶液刻蚀玻璃的化学方程式:________ 。
(2)实验室不用带玻璃塞的试剂瓶盛装氢氧化钠溶液,写出相关原理反应的离子方程式:________ 。
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐,可以将其使用氧化物形式表示,例如Na2SiO3,其氧化物形式为Na2O·SiO2。某种黏土的主要成分为Na[AlSi3O8],将其表示为氧化物的形式为aNa2O·bAl2O3·cSiO2,则a:b:c=________ 。(最简整数比)
Ⅱ.现代信息的明星材料-硅
工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:________ 。
(5)为提高流化床反应器中的反应速率,可以采取的操作有:________ 。(填2个)
(6)还原炉中发生的化学反应方程式为________ 。
(7)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有________ 。
(8)已知反应 ,一定温度下,向2L恒容密闭容器中充入一定量的
,一定温度下,向2L恒容密闭容器中充入一定量的 、
、 和Si(s)发生反应,经过10min达到后,体系中H2、SiHCl3(g)的物质的量浓度分别为2mol·L-1、1mol·L-1。则,从反应开始到10min时SiCl4的平均速率为
和Si(s)发生反应,经过10min达到后,体系中H2、SiHCl3(g)的物质的量浓度分别为2mol·L-1、1mol·L-1。则,从反应开始到10min时SiCl4的平均速率为________ 。
Ⅰ.建筑领域的基石材料-硅酸盐
(1)烧制普通玻璃的原料是
(2)实验室不用带玻璃塞的试剂瓶盛装氢氧化钠溶液,写出相关原理反应的离子方程式:
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐,可以将其使用氧化物形式表示,例如Na2SiO3,其氧化物形式为Na2O·SiO2。某种黏土的主要成分为Na[AlSi3O8],将其表示为氧化物的形式为aNa2O·bAl2O3·cSiO2,则a:b:c=
Ⅱ.现代信息的明星材料-硅
工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:

(5)为提高流化床反应器中的反应速率,可以采取的操作有:
(6)还原炉中发生的化学反应方程式为
(7)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
(8)已知反应
 ,一定温度下,向2L恒容密闭容器中充入一定量的
,一定温度下,向2L恒容密闭容器中充入一定量的 、
、 和Si(s)发生反应,经过10min达到后,体系中H2、SiHCl3(g)的物质的量浓度分别为2mol·L-1、1mol·L-1。则,从反应开始到10min时SiCl4的平均速率为
和Si(s)发生反应,经过10min达到后,体系中H2、SiHCl3(g)的物质的量浓度分别为2mol·L-1、1mol·L-1。则,从反应开始到10min时SiCl4的平均速率为
您最近一年使用:0次
2024-04-06更新
|
234次组卷
|
2卷引用:广西省钦州市第四中学2023-2024学年高三下学期第八周考试化学试卷
名校
5 . 为了降低大气中NO的排放量,可在NH3的作用下,通过催化剂将NO转化为无毒无害的 。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
 。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是
。向2L的恒容密闭容器中加入一定量的NH3、NO、NO2,测得NH3、N2、H2O的浓度随时间的变化情况如图所示。下列说法正确的是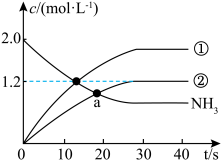
| A.曲线①表示N2的浓度随时间的变化情况 |
B.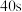 时, 时,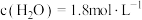 |
C.a点时,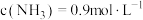 |
D.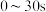 内,用NO表示的平均反应速率为 内,用NO表示的平均反应速率为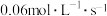 |
您最近一年使用:0次
2024-04-02更新
|
469次组卷
|
3卷引用:广西省钦州市第四中学2023-2024学年高三下学期第八周考试化学试卷
6 . 在 恒容密闭容器中加入一定量
恒容密闭容器中加入一定量 和
和 ,发生反应
,发生反应 ,
, 。绝热条件下容器中
。绝热条件下容器中 物质的量随时间的变化关系如表格所示。不同温度下平衡时
物质的量随时间的变化关系如表格所示。不同温度下平衡时 的体积分数与
的体积分数与 起始时的投料比的变化关系如图所示。则下列结论错误的是
起始时的投料比的变化关系如图所示。则下列结论错误的是

 恒容密闭容器中加入一定量
恒容密闭容器中加入一定量 和
和 ,发生反应
,发生反应 ,
, 。绝热条件下容器中
。绝热条件下容器中 物质的量随时间的变化关系如表格所示。不同温度下平衡时
物质的量随时间的变化关系如表格所示。不同温度下平衡时 的体积分数与
的体积分数与 起始时的投料比的变化关系如图所示。则下列结论错误的是
起始时的投料比的变化关系如图所示。则下列结论错误的是
| 时间/min | 0 | 1 | 2 | 3 | 4 |
| n(A)/mol | 4.0 | 3.8 | 3.0 | 2.4 | 2.0 |
| n(B)/mol | 2.0 | 1.9 | 1.5 | 1.2 | 1.0 |
| n(C)/mol | 0 | 0.1 | 0.5 | 0.8 | 1.0 |
| A.随反应进行,正反应速率先增大后减小 |
B.图中 |
C.前 平均化学反应速率 平均化学反应速率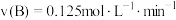 |
D.a、b、c三点 的转化率: 的转化率: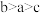 |
您最近一年使用:0次
名校
7 . 向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
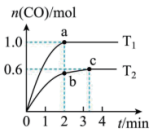
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
| A.该反应在任意温度下均可自发进行 |
B. 温度下, 温度下, 的平衡转化率是30% 的平衡转化率是30% |
C. 、 、 两点平衡常数: 两点平衡常数: |
D. 温度下,0到 温度下,0到 内,用 内,用 表示的平均反应速率为0.1mol·L-1·min-1 表示的平均反应速率为0.1mol·L-1·min-1 |
您最近一年使用:0次
8 . 接触法制硫酸工艺中,其主反应在450℃左右并有催化剂存在下进行: 。
。
(1)该反应的平衡常数表达式K=_______ ,该反应450℃时的平衡常数_______ 500℃时的平衡常数(填“>”或“<”或“=”)。
(2)下列描述能说明上述反应(反应容器体积不变)已达平衡的是_______ 。
a.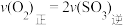
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5L的密闭容器中充入 SO2和
SO2和 O2,半分钟后达到平衡,测得容器中含0.18molSO3,则v(O2)=
O2,半分钟后达到平衡,测得容器中含0.18molSO3,则v(O2)=_______ mol/(L∙min):如果要提高SO2转化率,可以采取哪些措施?请写出两种方法_______ 、_______ 。
 。
。(1)该反应的平衡常数表达式K=
(2)下列描述能说明上述反应(反应容器体积不变)已达平衡的是
a.
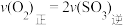
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5L的密闭容器中充入
 SO2和
SO2和 O2,半分钟后达到平衡,测得容器中含0.18molSO3,则v(O2)=
O2,半分钟后达到平衡,测得容器中含0.18molSO3,则v(O2)=
您最近一年使用:0次
9 . 科研、生产中常涉及碳的化合物。回答下列问题:
(1) 时,向容积为
时,向容积为 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:
①反应前 内的平均反应速率
内的平均反应速率
_________ ;表中 的值为
的值为___________ 。
②判定 时达到平衡状态的理由是
时达到平衡状态的理由是___________ 。
(2)工业上可利用煤的气化产物(水煤气)合成二甲醚: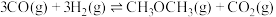
 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是___________(填字母)。
的转化率,可以采取的措施是___________(填字母)。
(3)高炉炼铁中发生的主要反应为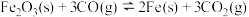 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
___________ ,
___________ 0(填“>”“<”或“=”)。

(4) 和
和 通入聚焦太阳能反应器中,发生反应:
通入聚焦太阳能反应器中,发生反应:
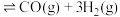 ,将等物质的量的
,将等物质的量的 和
和 充入
充入 恒容密闭反应器中,某温度下反应达到平衡,平衡常数
恒容密闭反应器中,某温度下反应达到平衡,平衡常数 ,此时测得
,此时测得 ,则
,则 的平衡转化率为
的平衡转化率为___________ (保留两位有效数字)。
(1)
 时,向容积为
时,向容积为 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:反应时间 | 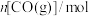 |  |
| 0 | 1.8 | 0.9 |
| 2 | 1.2 |  |
| 4 |  | 0.3 |
 内的平均反应速率
内的平均反应速率
 的值为
的值为②判定
 时达到平衡状态的理由是
时达到平衡状态的理由是(2)工业上可利用煤的气化产物(水煤气)合成二甲醚:
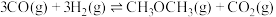
 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是___________(填字母)。
的转化率,可以采取的措施是___________(填字母)。| A.升高温度 | B.加入催化剂 |
C.减小 的浓度 的浓度 | D.增大压强(缩小容器体积) |
(3)高炉炼铁中发生的主要反应为
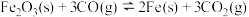 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式


(4)
 和
和 通入聚焦太阳能反应器中,发生反应:
通入聚焦太阳能反应器中,发生反应:
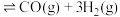 ,将等物质的量的
,将等物质的量的 和
和 充入
充入 恒容密闭反应器中,某温度下反应达到平衡,平衡常数
恒容密闭反应器中,某温度下反应达到平衡,平衡常数 ,此时测得
,此时测得 ,则
,则 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
2024-02-07更新
|
34次组卷
|
2卷引用:广西北海市2023-2024学年高二上学期期末考试化学试题
名校
10 . 一定温度下,某容积为2L 的密闭容器内,某一反应中M、N 的物质的量随反应时间变化的曲线如图所示:

(1)该反应的化学方程式是___________ 。
(2)在图上所示的三个时刻中,___________ (填“t1” “t2”或“t3”)时刻处于平衡状态,此时υ(正)______ υ(逆) (填“>”"<"或"=”);0~t2时间段内 υ(N)= ___________ 。
(3)已知 M、N 均为气体,则下列措施能增大反应速率的是 ___________(选填字母)。
(4)可以判断该反应已经达到平衡的是______。

(1)该反应的化学方程式是
(2)在图上所示的三个时刻中,
(3)已知 M、N 均为气体,则下列措施能增大反应速率的是 ___________(选填字母)。
| A.升高温度 | B.降低压强 |
| C.减小 N 的浓度 | D.将反应容器体积缩小 |
(4)可以判断该反应已经达到平衡的是______。
| A.c(M)=c(N) | B.c(M)保持不变 |
| C.v(M)=v(N) | D.N 的质量保持不变 |
您最近一年使用:0次



