解题方法
1 . 在两个容积均为4L的恒容密闭容器中,起始时均充入0.4mol乙苯,以温度、催化剂为实验条件变量,发生反应:
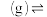
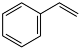
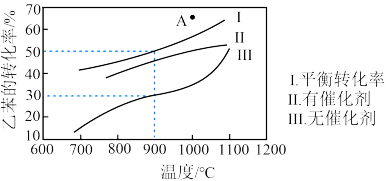
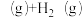 。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是

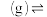

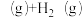 。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
A.900℃时,无催化剂的容器中,ts内H2的平均反应速率为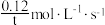 |
| B.1000℃时,有催化剂的容器中,延长反应时间乙苯的转化率可到达A点 |
| C.1100℃时,曲线Ⅱ、Ⅲ几乎重合,可能是因为催化剂失活 |
| D.其他条件不变时,升高温度或减小压强均能使平衡向右移动,均能使平衡常数K增大 |
您最近一年使用:0次
名校
解题方法
2 . 氮氧化物是主要大气污染物,可采用多种方法消除,其中氢气选择性催化还原(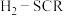 )是一种理想的方法,备受研究者关注,其相关反应如下:
)是一种理想的方法,备受研究者关注,其相关反应如下:
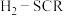 法的主反应:
法的主反应:

副反应: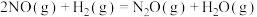

(1)已知: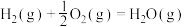
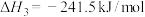
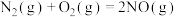
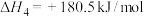
①
_____ 。
②副反应能自发进行的条件是_____ (填“低温”或“高温”)。
(2)恒温条件下,将NO、 充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中
充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中 、
、 的体积分数随温度的变化关系如图所示。
的体积分数随温度的变化关系如图所示。
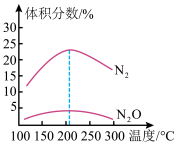
①提高主反应选择性的最佳措施是_____ (填序号)。
A降低温度 B.使用合适的催化剂 C.增大 D.增大压强
D.增大压强
②如图,温度高于205℃时, 的体积分数随温度的升高而减小的原因可能是
的体积分数随温度的升高而减小的原因可能是_____ 。
(3)T℃, 恒容密闭容器中发生上述反应,平衡体系中
恒容密闭容器中发生上述反应,平衡体系中 物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为
物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为 )为
)为_____ 。
(4)一定条件下,恒温恒容容器中充入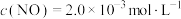 、
、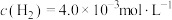 ,只发生
,只发生 反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为
反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为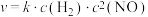 ]
]
当t=20min时,
_____  (速率常数
(速率常数 )
)
(5) 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的_____ 极,正极反应式为_____ 。

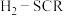 )是一种理想的方法,备受研究者关注,其相关反应如下:
)是一种理想的方法,备受研究者关注,其相关反应如下: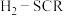 法的主反应:
法的主反应:

副反应:
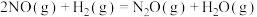

(1)已知:
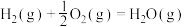
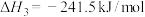
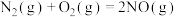
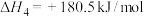
①

②副反应能自发进行的条件是
(2)恒温条件下,将NO、
 充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中
充入某恒容密闭容器中,在催化剂作用下进行反应。在不同温度下,反应相同时间时测得混合气体中 、
、 的体积分数随温度的变化关系如图所示。
的体积分数随温度的变化关系如图所示。
①提高主反应选择性的最佳措施是
A降低温度 B.使用合适的催化剂 C.增大
 D.增大压强
D.增大压强②如图,温度高于205℃时,
 的体积分数随温度的升高而减小的原因可能是
的体积分数随温度的升高而减小的原因可能是(3)T℃,
 恒容密闭容器中发生上述反应,平衡体系中
恒容密闭容器中发生上述反应,平衡体系中 物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为
物质的量分数为10%,平衡压强与起始压强之比为3.6∶4,则NO的有效去除率(转化为 )为
)为(4)一定条件下,恒温恒容容器中充入
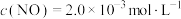 、
、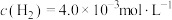 ,只发生
,只发生 反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为
反应,体系的总压强p随时间t的变化如下表所示:[已知该反应速率方程为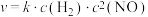 ]
]| t/min | 0 | 10 | 20 | 30 | 40 |
| p/kPa | 24 | 22.6 | 21.6 | 21 | 21 |

 (速率常数
(速率常数 )
)(5)
 、
、 和熔融
和熔融 可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用,则石墨Ⅰ为原电池的
您最近一年使用:0次
名校
3 . 在一恒温恒容的2L密闭容器中充入0.2 X、0.2
X、0.2 Y和0.1
Y和0.1 Z,发生如下两个反应:
Z,发生如下两个反应:
①

②

5min时反应达到平衡,测得体系的压强减少20%,此时剩余的X和Y浓度相同。
下列说法错误的是
 X、0.2
X、0.2 Y和0.1
Y和0.1 Z,发生如下两个反应:
Z,发生如下两个反应:①


②


5min时反应达到平衡,测得体系的压强减少20%,此时剩余的X和Y浓度相同。
下列说法错误的是
A.平衡后 |
B.0~5min内用Z表示的平均反应速率 |
C.该温度下 |
D.平衡后,向容器中再充入0.1 Q和0.05 Q和0.05 Z,反应①不移动 Z,反应①不移动 |
您最近一年使用:0次
4 . 在160℃、250℃条件下,分别向两个固定容积为2L的容器中充入2molCO(g)和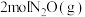 ,发生反应:
,发生反应:
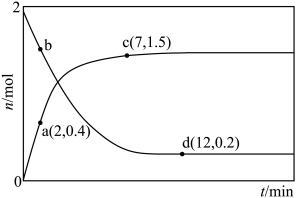
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
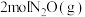 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
A.ac段 的平均反应速率为 的平均反应速率为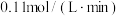 |
| B.曲线bd对应160℃条件下的反应 |
C.正反应速率: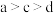 |
D.160℃时,该反应的平衡常数 |
您最近一年使用:0次
名校
解题方法
5 .  的回收利用对减少温室气体排放,改善人类生存环境具有重要意义。
的回收利用对减少温室气体排放,改善人类生存环境具有重要意义。
(1)利用 和
和 重整可制合成气(主要成分为
重整可制合成气(主要成分为 、
、 ,重整过程中部分反应的热化学方程式如下:
,重整过程中部分反应的热化学方程式如下:
①
②
③
则反应 的
的
_________ 。
(2) 可经过催化氢化合成乙烯。反应的化学方程式为:
可经过催化氢化合成乙烯。反应的化学方程式为: 。在
。在 密闭容器中充入
密闭容器中充入 和
和 ,在一定条件下发生反应,
,在一定条件下发生反应, 的转化率与温度、投料比
的转化率与温度、投料比 的关系如图所示:
的关系如图所示:

①A、B两点对应的平衡常数:
_________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②当 时,C点处
时,C点处
_________  。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
③若 、
、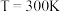 ,当反应进行到50min时,
,当反应进行到50min时, 的转化率为25%,则反应速率
的转化率为25%,则反应速率
_________ 。
(3)一种微生物电化学方法生产甲烷的装置如下图所示:

b为_________ (填“负极”或“正极”),阳极电极反应式为_________ 。理论上,每生成1L甲烷,阳极室产生
_________ L(标准状况)。
 的回收利用对减少温室气体排放,改善人类生存环境具有重要意义。
的回收利用对减少温室气体排放,改善人类生存环境具有重要意义。(1)利用
 和
和 重整可制合成气(主要成分为
重整可制合成气(主要成分为 、
、 ,重整过程中部分反应的热化学方程式如下:
,重整过程中部分反应的热化学方程式如下:①

②

③

则反应
 的
的
(2)
 可经过催化氢化合成乙烯。反应的化学方程式为:
可经过催化氢化合成乙烯。反应的化学方程式为: 。在
。在 密闭容器中充入
密闭容器中充入 和
和 ,在一定条件下发生反应,
,在一定条件下发生反应, 的转化率与温度、投料比
的转化率与温度、投料比 的关系如图所示:
的关系如图所示:
①A、B两点对应的平衡常数:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②当
 时,C点处
时,C点处
 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)③若
 、
、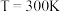 ,当反应进行到50min时,
,当反应进行到50min时, 的转化率为25%,则反应速率
的转化率为25%,则反应速率
(3)一种微生物电化学方法生产甲烷的装置如下图所示:

b为

您最近一年使用:0次
名校
解题方法
6 . T℃下,向某容积为2L的恒容密闭容器中充入1mol 、3mol
、3mol ,发生反应
,发生反应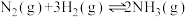 ,反应过程中容器内的总压强随时间的变化如图所示,下列有关说法正确的是
,反应过程中容器内的总压强随时间的变化如图所示,下列有关说法正确的是

 、3mol
、3mol ,发生反应
,发生反应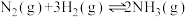 ,反应过程中容器内的总压强随时间的变化如图所示,下列有关说法正确的是
,反应过程中容器内的总压强随时间的变化如图所示,下列有关说法正确的是
A.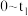 min内, min内,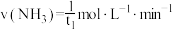 |
B. min时, min时,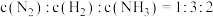 |
C. min时, min时, 的体积分数为60% 的体积分数为60% |
D.T℃下的平衡常数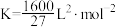 |
您最近一年使用:0次
2022-11-10更新
|
197次组卷
|
8卷引用:2022年重庆高考真题化学试题变式题(选择题11-14)
(已下线)2022年重庆高考真题化学试题变式题(选择题11-14)重庆西南大学附属中学校2022-2023学年高二上学期1月线上定时检测化学试题河南省创新发展联盟2022-2023学年高二上学期期中联考化学试题新疆维吾尔自治区新疆生产建设兵团部分名校2022-2023学年高二上学期期中联考化学试题广西贵港市桂平市浔州高级中学2022-2023学年高二上学期期中考试化学试题四川省泸县第四中学2022-2023学年高二上学期期中考试化学试题(已下线)第04讲 化学平衡状态 化学平衡常数-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
7 . 氢能源是公认的环境友好型二次能源,对其开发和利用是科研领域研究的热点。
回答下列问题:
(1)甲烷与水蒸气的催化反应可制备 和
和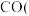 合成气
合成气 。
。
已知:Ⅰ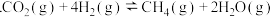
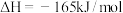 ;
;
Ⅱ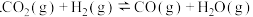
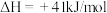 。
。
①制备合成气反应的热化学方程式为_________ 。
②制备合成气时,会因副反应
 而使合成气产率降低。有利于降低副反应的反应条件为
而使合成气产率降低。有利于降低副反应的反应条件为________  任写一点
任写一点 ;有利于提高制备合成气反应选择性的关键因素为
;有利于提高制备合成气反应选择性的关键因素为_____ 。
③一定温度下,向5L恒容密闭容器中充入 和
和 ,只发生反应Ⅱ。10min达到平衡时测得CO的体积分数为
,只发生反应Ⅱ。10min达到平衡时测得CO的体积分数为 。则0—10min内,用
。则0—10min内,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率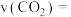
______ ;下列事实能说明该反应达到平衡状态的是____  填选项字母
填选项字母 。
。
A 混合气体密度不再改变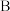 混合气体的平均相对分子质量不再改变
混合气体的平均相对分子质量不再改变
C 容器内气体压强不再改变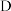 断裂
断裂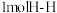 键同时断裂
键同时断裂 键
键
(2)部分合金可用于氢能源的存储。一定温度下,某储氢合金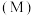 的储氢效率
的储氢效率 固相中氢原子与金属原子的数目之比
固相中氢原子与金属原子的数目之比 与温度
与温度 和氢气的平衡压强
和氢气的平衡压强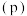 的关系如图所示。在OA段,氢溶解于M中形成固溶体
的关系如图所示。在OA段,氢溶解于M中形成固溶体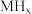 ;在AB段,发生氢化反应的化学方程式为
;在AB段,发生氢化反应的化学方程式为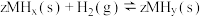 。
。

① 时,该反应的平衡常数
时,该反应的平衡常数
__________  用含
用含 的代数式表示,
的代数式表示, 为用分压表示的平衡常数
为用分压表示的平衡常数 。
。
②
_________________  填“
填“ ”“
”“ ”或“
”或“ ”
”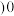 。
。
③当反应处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应可能处于图中的______________ 点 填“b”“c”或“d”
填“b”“c”或“d” 。
。
(3)氢能源在电化学领域的一种存储和应用的原理为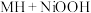

 ,充电时的阳极反应式为
,充电时的阳极反应式为_____________ 。
回答下列问题:
(1)甲烷与水蒸气的催化反应可制备
 和
和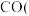 合成气
合成气 。
。已知:Ⅰ
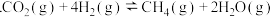
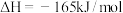 ;
;Ⅱ
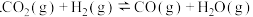
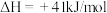 。
。①制备合成气反应的热化学方程式为
②制备合成气时,会因副反应

 而使合成气产率降低。有利于降低副反应的反应条件为
而使合成气产率降低。有利于降低副反应的反应条件为 任写一点
任写一点 ;有利于提高制备合成气反应选择性的关键因素为
;有利于提高制备合成气反应选择性的关键因素为③一定温度下,向5L恒容密闭容器中充入
 和
和 ,只发生反应Ⅱ。10min达到平衡时测得CO的体积分数为
,只发生反应Ⅱ。10min达到平衡时测得CO的体积分数为 。则0—10min内,用
。则0—10min内,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率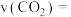
 填选项字母
填选项字母 。
。A 混合气体密度不再改变
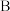 混合气体的平均相对分子质量不再改变
混合气体的平均相对分子质量不再改变C 容器内气体压强不再改变
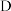 断裂
断裂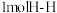 键同时断裂
键同时断裂 键
键(2)部分合金可用于氢能源的存储。一定温度下,某储氢合金
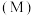 的储氢效率
的储氢效率 固相中氢原子与金属原子的数目之比
固相中氢原子与金属原子的数目之比 与温度
与温度 和氢气的平衡压强
和氢气的平衡压强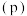 的关系如图所示。在OA段,氢溶解于M中形成固溶体
的关系如图所示。在OA段,氢溶解于M中形成固溶体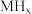 ;在AB段,发生氢化反应的化学方程式为
;在AB段,发生氢化反应的化学方程式为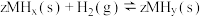 。
。
①
 时,该反应的平衡常数
时,该反应的平衡常数
 用含
用含 的代数式表示,
的代数式表示, 为用分压表示的平衡常数
为用分压表示的平衡常数 。
。②

 填“
填“ ”“
”“ ”或“
”或“ ”
”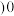 。
。③当反应处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应可能处于图中的
 填“b”“c”或“d”
填“b”“c”或“d” 。
。(3)氢能源在电化学领域的一种存储和应用的原理为
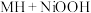

 ,充电时的阳极反应式为
,充电时的阳极反应式为
您最近一年使用:0次



