名校
1 . 氮及其化合物在生产生活中有广泛的应用,按要求回答下列问题:
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取 的化学方程式为
的化学方程式为___________ 。
(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用 、
、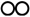 、
、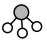 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下, 两电极产生气体的体积比为
两电极产生气体的体积比为___________ , 电极的电极反应方程式为
电极的电极反应方程式为___________ 。
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取
 的化学方程式为
的化学方程式为(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用
 、
、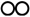 、
、 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。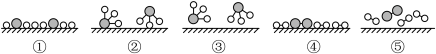
| A.②③④①⑤ | B.③②①④⑤ | C.③②④①⑤ | D.⑤④①②③ |
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下,
 两电极产生气体的体积比为
两电极产生气体的体积比为 电极的电极反应方程式为
电极的电极反应方程式为
您最近一年使用:0次
名校
解题方法
2 . 下列实验操作、现象及所得出的结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下,用pH计分别测定 溶液和 溶液和 溶液的pH 溶液的pH | 测得pH都等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| B | 常温下,将锌片与铝片用导线连接后,插入浓硫酸中 | 锌片缓慢溶解,铝片上有气体产生 | 金属活泼性:铝<锌 |
| C | 向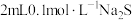 溶液中先后滴加2滴等浓度的 溶液中先后滴加2滴等浓度的 溶液和 溶液和 溶液 溶液 | 先有白色沉淀生成,后又有黑色沉淀 | 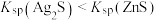 |
| D | 向两支盛有 5% 5% 溶液的试管中,分别加入 溶液的试管中,分别加入 的 的 溶液和 溶液和 蒸馏水 蒸馏水 | 加入 溶液的小试管中产生大量气泡,加入蒸馏水的小试管中无明显现象 溶液的小试管中产生大量气泡,加入蒸馏水的小试管中无明显现象 |  对 对 的分解起催化作用 的分解起催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-24更新
|
145次组卷
|
2卷引用:江苏省南京市2023-2024学年高二下学期期初学业质量调研化学试卷
名校
解题方法
3 . 甲醇制丙烯的反应为:
 ,已知:速率常数k与反应温度T、活化能
,已知:速率常数k与反应温度T、活化能 之间满足关系:
之间满足关系: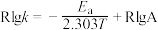 (R和A为常数)。下列说法错误的是
(R和A为常数)。下列说法错误的是

 ,已知:速率常数k与反应温度T、活化能
,已知:速率常数k与反应温度T、活化能 之间满足关系:
之间满足关系: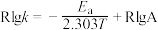 (R和A为常数)。下列说法错误的是
(R和A为常数)。下列说法错误的是
A.加催化剂不能减小 |
| B.升温能改变该反应的速率常数k |
C.已知 、 、 的燃烧热可以计算该反应的 的燃烧热可以计算该反应的 |
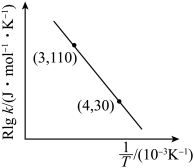
D.若实验得出Rlgk和 的关系如图,可计算该反应的活化能 的关系如图,可计算该反应的活化能 为 为 |
您最近一年使用:0次
2024-01-21更新
|
159次组卷
|
5卷引用:河南省南阳市第一中学校2023-2024学年高二下学期开学考试化学试题
河南省南阳市第一中学校2023-2024学年高二下学期开学考试化学试题 重庆市2024届高三上学期第二次质量检测化学试题重庆市南开中学校2023-2024学年高三上学期10月月考化学试题黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
4 . 某反应的反应机理可以分成如下两步,下列说法错误的是
| 反应机理 | 第一步反应 | 第二步反应 |
 (慢反应) (慢反应) | 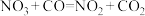 (快反应) (快反应) |
| A.在条件相同时,该反应的速率由第一步反应速率决定 |
| B.该反应的总反应方程式为NO2+CO=NO+CO2 |
| C.升高温度只会影响第一步反应速率,对第二步反应速率无影响 |
| D.加入合适的催化剂可降低反应的活化能,加快反应速率 |
您最近一年使用:0次
2024-01-01更新
|
143次组卷
|
12卷引用:安徽省A10联盟2022届高三上学期摸底考试化学试题
安徽省A10联盟2022届高三上学期摸底考试化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期中考试化学(理)试题(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)2021年广东省高考化学试卷变式题11-21吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题湖北省武汉市部分学校2021-2022学年高二上学期12月联考化学试题四川省兴文第二中学校2023-2024学年高二上学期11月期中考试化学试题陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷 (已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
名校
5 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业,是一种浅黄色、遇水易分解的固体,但溶于浓硫酸后并不分解。某实验小组将在A中产生的SO2通入浓硫酸和浓硝酸的混合溶液中制备亚硝酰硫酸,并测定产品的纯度。
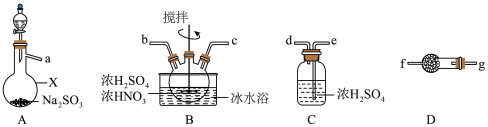
(1)仪器X的名称为___________ ;
(2)按气流从左到右的顺序,上述仪器的连接顺序为(填仪器接口字母)___________ 。
(3)①装置B中发生反应的化学方程式为___________ 。
②开始时反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其可能原因是___________ 。
(4)装置B中维持反应体系温度不高于20℃的主要原因是___________ 。
(5)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00 mL 0.10mol/L的KMnO4溶液和适量H2SO4,摇匀,再将溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20 mol/L的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4,2KMnO4+5Na2C2O4+8H2SO4=K2SO4+2MnSO4+10CO2+5Na2SO4+8H2O。
①滴定终点的现象为___________ 。
②该产品的纯度为___________ % (保留小数点后一位)。

(1)仪器X的名称为
(2)按气流从左到右的顺序,上述仪器的连接顺序为(填仪器接口字母)
(3)①装置B中发生反应的化学方程式为
②开始时反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其可能原因是
(4)装置B中维持反应体系温度不高于20℃的主要原因是
(5)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00 mL 0.10mol/L的KMnO4溶液和适量H2SO4,摇匀,再将溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20 mol/L的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4,2KMnO4+5Na2C2O4+8H2SO4=K2SO4+2MnSO4+10CO2+5Na2SO4+8H2O。
①滴定终点的现象为
②该产品的纯度为
您最近一年使用:0次
6 . 碱式硫酸铁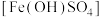 难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
(1)锥形瓶中发生反应的化学方程式为___________ ;某同学认为用 溶液代替稀硝酸更好,理由是
溶液代替稀硝酸更好,理由是___________ 。
(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为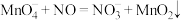 。
。
该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为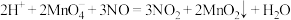 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为___________ 。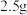 产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用
产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用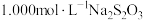 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为 、
、 )。
)。
①盛装 标准溶液的滴定管应选用
标准溶液的滴定管应选用___________ (填“酸式”或“碱式”)滴定管。
②判断达到滴定终点的方法为___________ 。
③该产品的纯度为___________  ,滴定过程中,如果滴定速度过慢,可能导致所测结果
,滴定过程中,如果滴定速度过慢,可能导致所测结果___________ (填“偏高”“偏低”或“无影响”)。
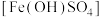 难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:(1)锥形瓶中发生反应的化学方程式为
 溶液代替稀硝酸更好,理由是
溶液代替稀硝酸更好,理由是(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为
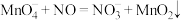 。
。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为
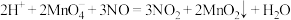 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为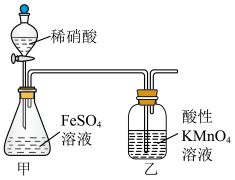
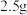 产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用
产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用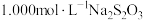 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为 、
、 )。
)。①盛装
 标准溶液的滴定管应选用
标准溶液的滴定管应选用②判断达到滴定终点的方法为
③该产品的纯度为
 ,滴定过程中,如果滴定速度过慢,可能导致所测结果
,滴定过程中,如果滴定速度过慢,可能导致所测结果
您最近一年使用:0次
2023-12-21更新
|
93次组卷
|
2卷引用:安徽省淮北市树人高级中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
7 . 硫化氢与甲醇合成甲硫醇(CH3SH)的催化过程如图。下列说法中错误的是
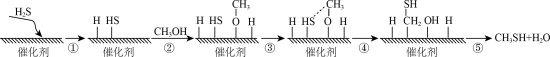

| A.过程①、②均需要吸收能量 |
| B.过程④中,只形成了O-H键 |
| C.反应前后催化剂的质量和化学性质没有改变 |
D.总反应方程式可以表示为 |
您最近一年使用:0次
2023-10-18更新
|
130次组卷
|
2卷引用:广西柳州铁一中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
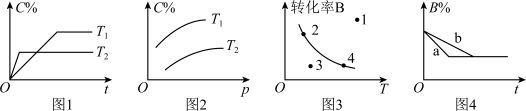
8 . 某化学研究小组探究外界条件对化学反应 的速率和平衡的影响图像如图所示。下列判断错误的是
的速率和平衡的影响图像如图所示。下列判断错误的是
 的速率和平衡的影响图像如图所示。下列判断错误的是
的速率和平衡的影响图像如图所示。下列判断错误的是
A.由图1可知,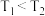 该反应正反应为放热反应 该反应正反应为放热反应 |
B.由图2可知,该反应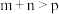 |
C.图3中,表示反应速率 的是点1 的是点1 |
D.图4中,若 ,则a曲线可能使用了催化剂 ,则a曲线可能使用了催化剂 |
您最近一年使用:0次
2023-10-14更新
|
470次组卷
|
9卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题
江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二下学期开学考试化学试卷河南省驻马店市2022-2023学年高二上学期期末考试化学试题湖南师范大学附属中学2022-2023学年高一下学期期末考试化学试题湖南省长沙市雅礼中学2023-2024学年高二上学期第一次月考化学试题(已下线)专题04 化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)宁夏吴忠中学2023-2024学年高二上学期期末考试化学试题陕西省宝鸡市金台区2023-2024学年高二上学期期末检测化学试题
解题方法
9 .  是合成荧光粉、光导体等的重要原料,
是合成荧光粉、光导体等的重要原料, 的开发与利用是科学界研究的热点。回答下列问题:
的开发与利用是科学界研究的热点。回答下列问题:
(1)已知: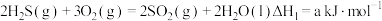 ,
,  ,则空气氧化脱除
,则空气氧化脱除 反应
反应 的
的
___________  。
。
(2)工业上可通过羰基硫(COS)与水蒸气在一定条件下反应制备 ,反应的原理为
,反应的原理为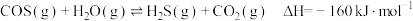 。
。
①T℃时,采用适当的催化剂在密闭容器中将等物质的量的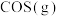 和
和 混合发生反应,已知该条件下该反应的平衡常数
混合发生反应,已知该条件下该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数可能为
的物质的量分数可能为___________ (填字母)
A.0.52 B.0.40 C.0.30 D.0.20
②图甲表示在两个相同的密闭容器中,反应物起始浓度相同,在相同质量不同型号的催化剂催化下,反应相同时间段时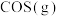 的转化率与温度的关系,则
的转化率与温度的关系,则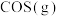 的平衡转化率
的平衡转化率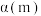
___________ 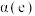 (填“
(填“ ”“
”“ ”或“
”或“ ”);q点时,
”);q点时,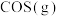 转化率出现突变的原因可能是
转化率出现突变的原因可能是___________ 。

③一定条件下进行该反应,测得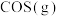 的平衡转化率与起始投料比
的平衡转化率与起始投料比 的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
___________ ,图中与c点的反应温度相同的点有___________ (填字母),若图中a、e两点对应的反应温度分别为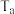 和
和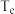 ,则
,则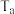
___________ 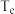 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。

(3)如图所示,质子固体电解质膜 燃料电池可对
燃料电池可对 废气进行资源化利用。
废气进行资源化利用。

电极a的电极反应式为___________ 。
 是合成荧光粉、光导体等的重要原料,
是合成荧光粉、光导体等的重要原料, 的开发与利用是科学界研究的热点。回答下列问题:
的开发与利用是科学界研究的热点。回答下列问题:(1)已知:
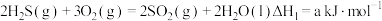 ,
,  ,则空气氧化脱除
,则空气氧化脱除 反应
反应 的
的
 。
。(2)工业上可通过羰基硫(COS)与水蒸气在一定条件下反应制备
 ,反应的原理为
,反应的原理为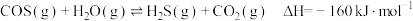 。
。①T℃时,采用适当的催化剂在密闭容器中将等物质的量的
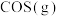 和
和 混合发生反应,已知该条件下该反应的平衡常数
混合发生反应,已知该条件下该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数可能为
的物质的量分数可能为A.0.52 B.0.40 C.0.30 D.0.20
②图甲表示在两个相同的密闭容器中,反应物起始浓度相同,在相同质量不同型号的催化剂催化下,反应相同时间段时
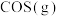 的转化率与温度的关系,则
的转化率与温度的关系,则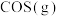 的平衡转化率
的平衡转化率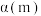
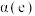 (填“
(填“ ”“
”“ ”或“
”或“ ”);q点时,
”);q点时,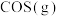 转化率出现突变的原因可能是
转化率出现突变的原因可能是
③一定条件下进行该反应,测得
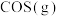 的平衡转化率与起始投料比
的平衡转化率与起始投料比 的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
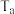 和
和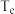 ,则
,则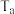
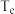 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)如图所示,质子固体电解质膜
 燃料电池可对
燃料电池可对 废气进行资源化利用。
废气进行资源化利用。
电极a的电极反应式为
您最近一年使用:0次
名校
解题方法
10 . 合成氨对人类生存具有重大意义,反应为:N2(g) + 3H2(g)  2NH3(g) ΔH
2NH3(g) ΔH
(1)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如下图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒):

①步骤c的化学方程式为________ 。
②由图像可知合成氨反应的ΔH________ 0(填“>”、“<”或“=”)。
③下列关于合成氨的说法不正确 的是________ (填字母)。
A.因为ΔS<0,所以该反应一定不能自发进行
B.步骤d、e、f中均有N-H键的生成
C.使用该催化剂可提高NH3的产量,降低反应的ΔH
D.加压不仅可加快反应速率,还有利于提高NH3的产量
(2)恒温下,往一个4 L的密闭容器中充入5.2 mol H2和2 mol N2,反应过程中对NH3的物质的量进行检测,得到的数据如下表所示:
①计算此条件下该反应的化学平衡常数K=________ 。
②若维持容器容积不变,温度不变,往原平衡体系中加入H2、N2和NH3各4 mol,化学平衡将向___________ 反应方向移动(填“正”或“逆”)。
 2NH3(g) ΔH
2NH3(g) ΔH(1)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如下图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒):

①步骤c的化学方程式为
②由图像可知合成氨反应的ΔH
③下列关于合成氨的说法
A.因为ΔS<0,所以该反应一定不能自发进行
B.步骤d、e、f中均有N-H键的生成
C.使用该催化剂可提高NH3的产量,降低反应的ΔH
D.加压不仅可加快反应速率,还有利于提高NH3的产量
(2)恒温下,往一个4 L的密闭容器中充入5.2 mol H2和2 mol N2,反应过程中对NH3的物质的量进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| n(NH3)/(mol) | 0.32 | 0.56 | 0.72 | 0.80 | 0.80 | 0.80 |
②若维持容器容积不变,温度不变,往原平衡体系中加入H2、N2和NH3各4 mol,化学平衡将向
您最近一年使用:0次



