名校
1 . 下列有关说法正确的是
A.恒温恒压下,向 平衡体系充入 平衡体系充入 ,正逆反应速率都不变 ,正逆反应速率都不变 |
| B.通过光辐射、超声波、高速研磨等,也有可能改变反应速率 |
| C.升高温度和增大压强都可以提高反应体系内活化分子百分数 |
| D.加入催化剂,不能改变活化分子百分数 |
您最近一年使用:0次
2023-08-08更新
|
463次组卷
|
2卷引用:湖北省重点中学4G+联合体2022-2023学年高二上学期期中考试化学试题
2 .  溶液是中学化学常用的一种试剂。下列实验探究方案能达到探究目的的是
溶液是中学化学常用的一种试剂。下列实验探究方案能达到探究目的的是
 溶液是中学化学常用的一种试剂。下列实验探究方案能达到探究目的的是
溶液是中学化学常用的一种试剂。下列实验探究方案能达到探究目的的是| 选项 | 探究方案 | 探究目的 |
| A | 室温下,向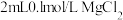 溶液中滴入 溶液中滴入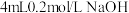 溶液,产生白色沉淀,再滴加5滴 溶液,产生白色沉淀,再滴加5滴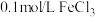 溶液;有红褐色沉淀生成 溶液;有红褐色沉淀生成 | 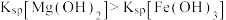 |
| B | 将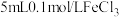 溶液与 溶液与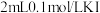 溶液混合于试管中充分反应后,滴加几滴 溶液混合于试管中充分反应后,滴加几滴 溶液,振荡;溶液变为血红色 溶液,振荡;溶液变为血红色 |  与 与 的反应有一定的限度 的反应有一定的限度 |
| C | A、B两支试管中分别加入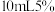 的 的 溶液,在A试管中加入 溶液,在A试管中加入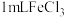 溶液,在B试管中加入 溶液,在B试管中加入 蒸馏水;A试管中产生气泡更快 蒸馏水;A试管中产生气泡更快 |  是 是 分解的催化剂 分解的催化剂 |
| D | 向2mL略浑浊的泥水中加入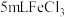 饱和溶液,静置,产生沉淀,溶液变澄清 饱和溶液,静置,产生沉淀,溶液变澄清 |  能吸附水中的悬浮物产生沉淀,具有净水效果 能吸附水中的悬浮物产生沉淀,具有净水效果 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 为消除燃煤烟气中含有的 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。
【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的 、NO转化为
、NO转化为 、
、 。
。
(1)

 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为_______ L。
(2)实验室利用模拟烟气(模拟烟气中 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。

①此方法“脱硫”“脱硝”探究实验的最佳温度为_______ ; 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是_______ 。
② 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为_______ 。
【方法二】 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)
研究表明,铁基催化剂在260~300℃范围内实现 技术的过程如图所示。
技术的过程如图所示。
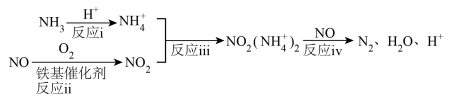
(3)根据上述机理, 在反应过程中的作用为
在反应过程中的作用为_______ ;等物质的量的 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为_______ ;
(4)若使用锰基催化剂(活性物质为 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:_______ 。
(5)向反应体系中添加 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为_______ 。
 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的
 、NO转化为
、NO转化为 、
、 。
。(1)


 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为(2)实验室利用模拟烟气(模拟烟气中
 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
①此方法“脱硫”“脱硝”探究实验的最佳温度为
 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是②
 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为【方法二】
 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)研究表明,铁基催化剂在260~300℃范围内实现
 技术的过程如图所示。
技术的过程如图所示。
(3)根据上述机理,
 在反应过程中的作用为
在反应过程中的作用为 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为(4)若使用锰基催化剂(活性物质为
 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:(5)向反应体系中添加
 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为
您最近一年使用:0次
2022-11-19更新
|
208次组卷
|
2卷引用:湖北省部分学校2022-2023学年高三上学期11月月考化学试题
4 . 已知: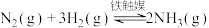
 ,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
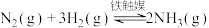
 ,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是| A.可提高反应物的平衡转化率 | B.可改变合成氨反应的焓变 |
| C.可减少合成氨的能耗 | D.可降低合成氨的反应温度 |
您最近一年使用:0次
5 .  和
和 是环境污染性气体,可利用反应
是环境污染性气体,可利用反应 将其转化为无害气体。将一定量的
将其转化为无害气体。将一定量的 和CO在催化剂作用下发生反应,测得单位时间内CO的转化率、催化剂的催化效率与温度的关系如图所示。下列说法错误的是
和CO在催化剂作用下发生反应,测得单位时间内CO的转化率、催化剂的催化效率与温度的关系如图所示。下列说法错误的是

 和
和 是环境污染性气体,可利用反应
是环境污染性气体,可利用反应 将其转化为无害气体。将一定量的
将其转化为无害气体。将一定量的 和CO在催化剂作用下发生反应,测得单位时间内CO的转化率、催化剂的催化效率与温度的关系如图所示。下列说法错误的是
和CO在催化剂作用下发生反应,测得单位时间内CO的转化率、催化剂的催化效率与温度的关系如图所示。下列说法错误的是
A. |
B. 的转化率受温度和催化剂的共同影响 的转化率受温度和催化剂的共同影响 |
| C.300~450℃内,催化效率是影响单位时间内CO转化率的主要因素 |
| D.450~600℃内,升温化学反应速率降低 |
您最近一年使用:0次
解题方法
6 . 乙醇是一种重要的工业原料,广泛应用于能源、化工、食品等领域。
Ⅰ.工业上乙烯水化制乙醇过程中能量变化如图所示:
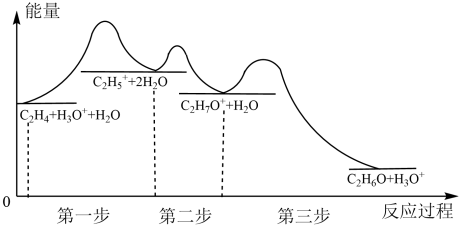
(1)图中所示活化能最大的步骤是第_______ 步。
(2)写出该反应过程中速率最快的基元反应:_______ 。
Ⅱ.研究显示乙酸甲酯催化加氢也可以制取乙醇,主要反应如下:
①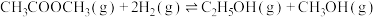
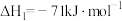
②

(3)已知反应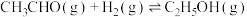 的
的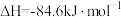 ,则
,则
_______ 。
(4)在体积密闭容器中进行上述反应时发现, 流速过大时乙酸甲酯的转化率下降,其原因可能是
流速过大时乙酸甲酯的转化率下降,其原因可能是_______ 。
Ⅲ.乙醇的一种重要用途是与乙酸反应合成乙酸乙酯。已知纯物质和相关恒沸混合物的常压沸点如下表:
(5)实际生产中,一般控制乙酸过量。若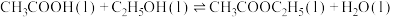
 ,则控制乙酸过量的作用有
,则控制乙酸过量的作用有_______ 。
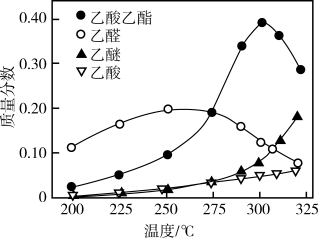
(6)一种新的乙醇催化合成乙酸乙酯的方法如下: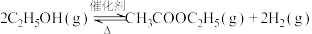 。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是_______。
。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是_______。
Ⅰ.工业上乙烯水化制乙醇过程中能量变化如图所示:

(1)图中所示活化能最大的步骤是第
(2)写出该反应过程中速率最快的基元反应:
Ⅱ.研究显示乙酸甲酯催化加氢也可以制取乙醇,主要反应如下:
①
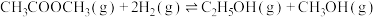
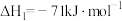
②


(3)已知反应
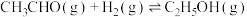 的
的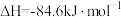 ,则
,则
(4)在体积密闭容器中进行上述反应时发现,
 流速过大时乙酸甲酯的转化率下降,其原因可能是
流速过大时乙酸甲酯的转化率下降,其原因可能是Ⅲ.乙醇的一种重要用途是与乙酸反应合成乙酸乙酯。已知纯物质和相关恒沸混合物的常压沸点如下表:
| 纯物质 | 沸点/℃ | 恒沸混合物(质量分数) | 沸点/℃ |
| 乙醇 | 78.3 | 乙酸乙酯(0.92)+水(0.08) | 70.4 |
| 乙酸 | 117.9 | 乙酸乙酯(0.69)+乙醇(0.31) | 71.8 |
| 乙酸乙酯 | 77.1 | 乙酸乙酯(0.83)+乙醇(0.08)+水(0.09) | 70.2 |
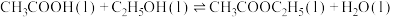
 ,则控制乙酸过量的作用有
,则控制乙酸过量的作用有(6)一种新的乙醇催化合成乙酸乙酯的方法如下:
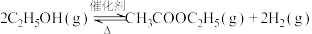 。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是_______。
。在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。关于该方法,下列推测不合理的是_______。
| A.该反应的最宜温度应为325℃ |
| B.适当减小体系压强,有利于提高乙醇平衡转化率 |
| C.在催化剂作用下,乙醚是反应历程中的中间产物 |
| D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键 |
您最近一年使用:0次
2022-11-03更新
|
170次组卷
|
2卷引用:湖北省鄂东南联盟2022-2023学年高三上学期期中联考化学试题
解题方法
7 . Wacker法烯烃氧化的催化循环过程如图所示,下列说法正确的是


A.乙烯双键的电子与 形成了配位键 形成了配位键 |
| B.整个过程中涉及极性键、非极性键的断裂和形成 |
C. 转化是Wacker法烯烃氧化过程中的催化剂 转化是Wacker法烯烃氧化过程中的催化剂 |
| D.该催化循环过程中溶液体系的碱性增强 |
您最近一年使用:0次
2022-11-03更新
|
118次组卷
|
2卷引用:湖北省鄂东南联盟2022-2023学年高三上学期期中联考化学试题
名校
解题方法
8 . 甲酸 含氢量高达4.4%,能够分解制氢。
含氢量高达4.4%,能够分解制氢。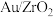 催化甲酸分解的机理如图所示,下列说法
催化甲酸分解的机理如图所示,下列说法错误的是

 含氢量高达4.4%,能够分解制氢。
含氢量高达4.4%,能够分解制氢。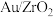 催化甲酸分解的机理如图所示,下列说法
催化甲酸分解的机理如图所示,下列说法
| A.反应过程中涉及极性键的断裂和非极性键的形成 |
| B.在反应液中加入HCOOK可提高反应速率 |
| C.该过程中每一步都发生氧化还原反应 |
D.该反应生成标准状况下2.24L ,转移电子0.2mol ,转移电子0.2mol |
您最近一年使用:0次
2022-10-13更新
|
199次组卷
|
3卷引用:湖北省部分重点中学2022-2023学年高三上学期10月联考化学试题
湖北省部分重点中学2022-2023学年高三上学期10月联考化学试题浙江省浙江大学附属中学(玉泉校区)2022-2023学年高二上学期期中考试 高二化学试卷(已下线)【2022】【高二化学】【期中考】-180
名校
解题方法
9 . 如图表示使用不同催化剂(AuF和AuPF )催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
)催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是

 )催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
)催化乙烯加氢生成乙烷[C2H4(g)+H2(g)=C2H6(g) △H=akJ•mol-1]的反应历程。下列说法错误的是
| A.乙烯催化加氢是放热反应 |
| B.稳定性:过渡态1<过渡态2<乙烷 |
| C.催化剂不同,反应路径不同 |
| D.总能量:断键吸收>成键释放 |
您最近一年使用:0次
2022-10-12更新
|
482次组卷
|
9卷引用:湖北省宜昌市协作体2022-2023学年高二上学期期中考试化学试题
湖北省宜昌市协作体2022-2023学年高二上学期期中考试化学试题河北省故城县高级中学2022-2023学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期第三次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期11月期中考试化学试题江西省赣州市兴国中学等六校2022-2023学年高三上学期12月月考化学试题河南省鹤壁市高中2022-2023学年高二下学期第一次段考化学试题辽宁省朝阳市建平县实验中学2022-2023学年高一下学期7月期末化学试题江西省部分学校2023-2024学年高二上学期10月月考化学试题浙江省金华市东阳市外国语学校2023-2024学年高二上学期10月月考化学试题
解题方法
10 . 我国科学家开发 单原子电催化剂,实现了在温和条件下利用
单原子电催化剂,实现了在温和条件下利用 和
和 合成
合成 。回答下列问题:
。回答下列问题:
(1)工业合成氨的化学方程式为________ 。已知: 和
和 总能量大于
总能量大于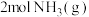 总能量,则工业合成氨的反应是
总能量,则工业合成氨的反应是________ (填“放热”或“吸热”反应。
(2)其他条件相同,在Cat1、Cat2、Cat3三种催化剂作用下,测得反应速率增大倍数与温度关系如图所示。实际生产中,宜选择的催化剂是________ (填“Cat1”、“Cat2”或“Cat3”),如果Cat1、Cat3是同一种催化剂, 时反应速率增大倍数小于
时反应速率增大倍数小于 时的可能原因是
时的可能原因是________ 。

(3)一定温度下,在1L恒容密闭容器中充入 和
和 ,测得
,测得 的物质的量(n)与时间(t)关系如表所示:
的物质的量(n)与时间(t)关系如表所示:
①0~10min内, 的平均反应速率
的平均反应速率
________  。
。
②15min时, 的正反应速率
的正反应速率________ (填“大于”、“小于”或“等于”) 的逆反应速率。
的逆反应速率。
③在上述条件下, 的平衡转化率为
的平衡转化率为________ 。
(4)氨气碱性(KOH溶液)燃料电池能量转化率较高,电池反应为 ,电池放电时,负极的电极反应式为
,电池放电时,负极的电极反应式为________ 。
 单原子电催化剂,实现了在温和条件下利用
单原子电催化剂,实现了在温和条件下利用 和
和 合成
合成 。回答下列问题:
。回答下列问题:(1)工业合成氨的化学方程式为
 和
和 总能量大于
总能量大于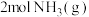 总能量,则工业合成氨的反应是
总能量,则工业合成氨的反应是(2)其他条件相同,在Cat1、Cat2、Cat3三种催化剂作用下,测得反应速率增大倍数与温度关系如图所示。实际生产中,宜选择的催化剂是
 时反应速率增大倍数小于
时反应速率增大倍数小于 时的可能原因是
时的可能原因是
(3)一定温度下,在1L恒容密闭容器中充入
 和
和 ,测得
,测得 的物质的量(n)与时间(t)关系如表所示:
的物质的量(n)与时间(t)关系如表所示:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 物质的量/mol | 0 | 0.30 | 0.50 | 0.65 | 0.70 | 0.70 |
 的平均反应速率
的平均反应速率
 。
。②15min时,
 的正反应速率
的正反应速率 的逆反应速率。
的逆反应速率。③在上述条件下,
 的平衡转化率为
的平衡转化率为(4)氨气碱性(KOH溶液)燃料电池能量转化率较高,电池反应为
 ,电池放电时,负极的电极反应式为
,电池放电时,负极的电极反应式为
您最近一年使用:0次
2022-10-10更新
|
165次组卷
|
5卷引用:湖北省百校联考2022-2023学年高三上学期10月联考化学试题



