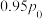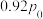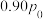1 . 光催化剂在紫外线照射下产生光生电子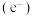 和光生空穴
和光生空穴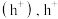 具有强氧化性,留在
具有强氧化性,留在 端,
端, 跃迁到
跃迁到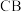 端.科学家利用乙腈
端.科学家利用乙腈 光催化脱氢偶联制备丁二腈
光催化脱氢偶联制备丁二腈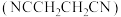 ,反应历程如下图所示.下列说法错误的是
,反应历程如下图所示.下列说法错误的是
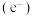 和光生空穴
和光生空穴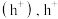 具有强氧化性,留在
具有强氧化性,留在 端,
端, 跃迁到
跃迁到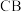 端.科学家利用乙腈
端.科学家利用乙腈 光催化脱氢偶联制备丁二腈
光催化脱氢偶联制备丁二腈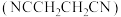 ,反应历程如下图所示.下列说法错误的是
,反应历程如下图所示.下列说法错误的是
A. 端上发生的反应为: 端上发生的反应为: |
| B.副产物乙酰胺只能与酸反应,不能与碱反应 |
C.单位时间内产生“空穴”数越多,反应 速率越快 速率越快 |
| D.提高丁二睛选择性的关键是抑制反应a,降低反应b的活化能 |
您最近半年使用:0次
2 .  甲烷化是“负碳排放”的重要研究方向,某研究团队报道了镍基催化剂上
甲烷化是“负碳排放”的重要研究方向,某研究团队报道了镍基催化剂上 与
与 反应生成甲烷的两种机理如图所示,其中吸附在催化剂表面的物种用*表示。
反应生成甲烷的两种机理如图所示,其中吸附在催化剂表面的物种用*表示。
 甲烷化是“负碳排放”的重要研究方向,某研究团队报道了镍基催化剂上
甲烷化是“负碳排放”的重要研究方向,某研究团队报道了镍基催化剂上 与
与 反应生成甲烷的两种机理如图所示,其中吸附在催化剂表面的物种用*表示。
反应生成甲烷的两种机理如图所示,其中吸附在催化剂表面的物种用*表示。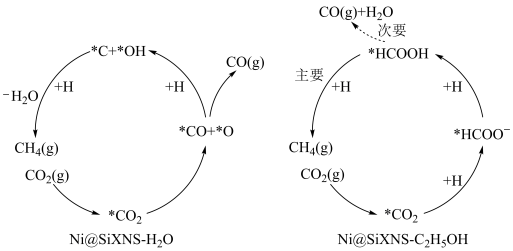
| A.镍基催化剂增加了活化分子的百分数 |
| B.两种机理均涉及极性链的断裂和生成 |
C.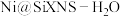 机理中 机理中 的选择性更高 的选择性更高 |
D.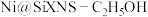 机理涉及反应 机理涉及反应 |
您最近半年使用:0次
3 . 室温下,下列实验方案不能达到探究目的的是
| 选项 | 实验方案 | 探究目的 |
| A | 向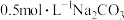 溶液中滴加酚酞,升温,观察溶液颜色变化 溶液中滴加酚酞,升温,观察溶液颜色变化 | 探究温度对 水解平衡的影响 水解平衡的影响 |
| B | 向等体积等浓度的 溶液中分别加入6滴等浓度的 溶液中分别加入6滴等浓度的 和 和 溶液,观察气体产生的速度 溶液,观察气体产生的速度 | 比较 和 和 的催化效果 的催化效果 |
| C | 分别测定 和 和 与盐酸反应生成 与盐酸反应生成 放出的热量 放出的热量 | 确定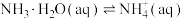 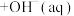 的 的 |
| D | 向2支盛有 不同浓度 不同浓度 溶液的试管中同时加入 溶液的试管中同时加入 溶液 溶液 | 探究 的浓度对该反应速率的影响 的浓度对该反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 .  (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。
 (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。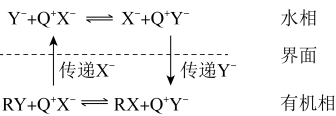
A.总反应为: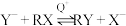 | B.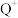 易溶于水相而难溶于有机相 易溶于水相而难溶于有机相 |
C.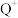 与 与 、 、 之间的离子键强度要适中 之间的离子键强度要适中 | D.PTC催化剂可用作相转移催化剂 |
您最近半年使用:0次
2024-04-26更新
|
355次组卷
|
2卷引用:湖北省圆创联盟2024届高三三月联合测评(一模)化学试卷
5 . 为实现碳达峰,可以将 进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化
进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化 与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
 进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化
进行碳捕集、利用与封存。科学研究发现,羟基季铵盐离子液体可以高效催化 与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
与环氧化合物合成环状碳酸酯的反应,某课题组经研究提出用离子液体三乙基羟乙基溴化铵催化此反应的机理如图所示。下列说法错误的是
| A.三乙基羟乙基溴化铵的催化活性可能优于无羟基结构的四乙基溴化铵 |
| B.该过程有极性键的断裂与形成 |
C.若-R为 ,则 ,则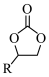 分子中有2个手性碳原子 分子中有2个手性碳原子 |
D.该过程的总反应式可表示为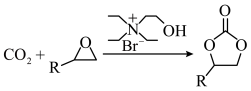 |
您最近半年使用:0次
名校
解题方法
6 . 我国科学家成功利用光伏发电,将电解水获得的 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
(1) 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。 的
的
__________ (用含 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)有学者结合实验和计算机模拟结果,得出 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为__________ ;TS3对应的步骤适合在__________ (填“高温”或“低温”)条件下进行。 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。 的生成速率
的生成速率__________ (填“>”“<”或“=”,下同) 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2__________ Cat1。
②b点之后 的转化率降低,可能的原因是
的转化率降低,可能的原因是__________ 。
(4)已知 催化加氢的主要反应如下:
催化加氢的主要反应如下:
反应Ⅰ.
反应Ⅱ.
①230℃时,将 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
平衡时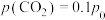 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
__________  (用含
(用含 的代数式表示)。
的代数式表示)。
②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当__________ 。
 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:(1)
 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。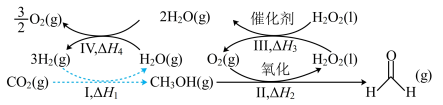
 的
的
 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。(2)有学者结合实验和计算机模拟结果,得出
 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为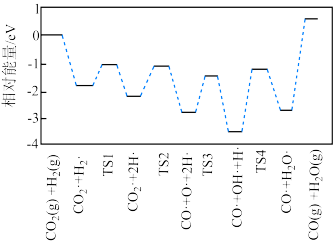
 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。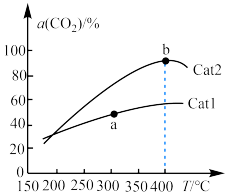
 的生成速率
的生成速率 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2②b点之后
 的转化率降低,可能的原因是
的转化率降低,可能的原因是(4)已知
 催化加氢的主要反应如下:
催化加氢的主要反应如下:反应Ⅰ.

反应Ⅱ.

①230℃时,将
 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。时间/min | 0 | 20 | 40 | 60 | 80 |
压强/MPa |
|
|
|
|
|
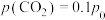 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当
您最近半年使用:0次
2024-04-07更新
|
338次组卷
|
4卷引用:湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
名校
7 . 常温常压下利用Cu/ZnO/ZrO催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注):
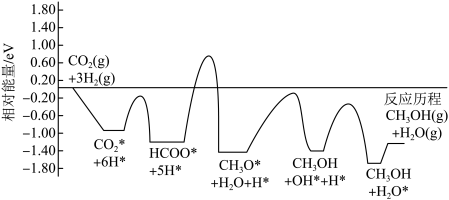
A.转化历程有四个基元反应,决速步为: |
| B.若无Cu/ZnO/ZrO催化剂,二氧化碳加氢制甲醇不能自发进行 |
| C.反应过程中断裂与形成的共价键类型相同 |
D.寻找高效催化剂,有利于 的回收利用,使该反应原子利用率达到100% 的回收利用,使该反应原子利用率达到100% |
您最近半年使用:0次
2024-03-17更新
|
421次组卷
|
3卷引用:湖北省七市州教科研协作体2024届高三下学期二模化学试题
湖北省七市州教科研协作体2024届高三下学期二模化学试题江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
解题方法
8 . 化学与生活、工农业生产息息相关,下列说法正确的是
| A.洁厕灵和食醋是家庭中常见的两种生活用品,食醋比洁厕灵的酸性强 |
| B.增大空气的进入量,可以减少汽车尾气中由于不完全燃烧排放的氨氧化物 |
| C.在冰醋酸中加水制成食醋的过程中,pH随加水量的增大而增大 |
D.利用反应 制氢,相同时间内,使用纳米CaO(催化剂)比微米CaO产率更高 制氢,相同时间内,使用纳米CaO(催化剂)比微米CaO产率更高 |
您最近半年使用:0次
2024-01-23更新
|
155次组卷
|
2卷引用:湖北省武汉市东华中师范大学第一附属中学2023-2024学年高二上学期11月期中化学试题
9 . 肼(N2H4)作为火箭发射的燃料助力神舟十七号载人飞船发射取得圆满成功。回答下列问题:
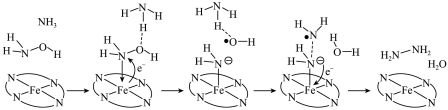
(1)以Fe2+配合物为催化中心,可实现NH2OH与NH3转化为N2H4,反应历程如下所示:___________ ,形成的化学键是___________ (填标号)。
a.N-H键 b.O-H键 c.N-O键 d.N-N键
②若将NH2OH替换为ND2OD,反应所得含氮物质是___________ 。
(2)键能是指气态分子中lmol化学键解离成气态原子所吸收的能量。已知部分化学键的键能如下表所示:
则N2H4(g)和O2(g)反应的热化学方程式是___________ 。
若用F2(g)代替O2(g)作氧化剂,反应释放的能量更大。
已知:H2(g)+F2(g)=2HF(g) H =-538kJ/mol
H =-538kJ/mol
2H2(g)+O2(g)=2H2O(g) H =-484kJ/mol
H =-484kJ/mol
则N2H4(g)+2F2(g)=N2(g)+4HF(g)的 H =
H =_______ kJ/mol。
(3)N2H4是二元弱碱,在水中的电离方式与NH3相似。N2H4第二步电离的方程式是________ ,N2H4与H2SO4形成正盐的化学式是___________ 。
(1)以Fe2+配合物为催化中心,可实现NH2OH与NH3转化为N2H4,反应历程如下所示:
a.N-H键 b.O-H键 c.N-O键 d.N-N键
②若将NH2OH替换为ND2OD,反应所得含氮物质是
(2)键能是指气态分子中lmol化学键解离成气态原子所吸收的能量。已知部分化学键的键能如下表所示:
| 化学键 | N-H | O-H | O=O | N≡N | N-N |
| 键能/(kJ·mol-1) | 391 | 463 | 497 | 945 | 193 |
若用F2(g)代替O2(g)作氧化剂,反应释放的能量更大。
已知:H2(g)+F2(g)=2HF(g)
 H =-538kJ/mol
H =-538kJ/mol2H2(g)+O2(g)=2H2O(g)
 H =-484kJ/mol
H =-484kJ/mol则N2H4(g)+2F2(g)=N2(g)+4HF(g)的
 H =
H =(3)N2H4是二元弱碱,在水中的电离方式与NH3相似。N2H4第二步电离的方程式是
您最近半年使用:0次
名校
解题方法
10 . 通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一,下列实验操作、现象和解释或者结论不正确的有
| 实验操作 | 现象 | 解释或者结论 | |
| A | 分别在20℃、30℃下,取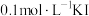 液,向其中先加入淀粉溶液,再加入 液,向其中先加入淀粉溶液,再加入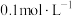 的硫酸( 的硫酸( ) ) | 30℃下,溶液更快出现蓝色 | 温度越高,化学反应速率越快 |
| B | 用 计测定 计测定 溶液和 溶液和 溶液的 溶液的 |  溶液的 溶液的 较大 较大 |  酸性弱于 酸性弱于 |
| C | 向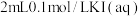 中加入 中加入 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加 ,充分反应,用四氯化碳充分萃取后取上层溶液滴加 | 四氯化碳层显紫色,上层溶液试样变红 |  和 和 的反应存在限度 的反应存在限度 |
| D | 向盛有 溶液的试管中加入酸化后的 溶液的试管中加入酸化后的 溶液 溶液 | 溶液变为棕黄色且出现无色气泡 | 生成了 ,同时 ,同时 催化分解 催化分解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次