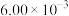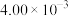1 . 某温度下,在某一恒容密闭容器中,充入一定物质的量的NO和Cl2,发生反应
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.仅适当降低温度,该反应的正逆反应速率均减小 |
B.加入合适的催化剂,该反应达到平衡时 的值将增大 的值将增大 |
| C.该反应的反应物的键能总和大于生成物的键能总和 |
| D.保持其他条件不变,仅充入少量的稀有气体,该反应的速率将增大 |
您最近一年使用:0次
2023-04-24更新
|
260次组卷
|
3卷引用:天津市重点校2023-2024学年高二上学期期末考试化学试题
2 . Ⅰ.铁、铬单质及其化合物的应用非常广泛。
(1)基态Fe原子的价层电子排布式为_______ ,Fe在周期表中的位置_______ 。Cr原子的基态电子排布式为_______ ,价电子排布图为_______ 。
(2)用X射线衍射测定,得到Fe的两种晶胞A、B,其结构如图所示。晶胞A中每个Fe原子紧邻的原子数为_______ 。每个晶胞B中含Fe原子数为_______ 。

(3)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式_______ 。从能量角度分析,铁触媒的作用是_______ 。

Ⅱ.在一定温度下,已知以下三个反应的平衡常数:
反应①:

反应②:

反应③:

(4)反应①的平衡常数表达式为_______ 。
(5)反应③的 与
与 、
、 的关系是
的关系是
_______ 。
(1)基态Fe原子的价层电子排布式为
(2)用X射线衍射测定,得到Fe的两种晶胞A、B,其结构如图所示。晶胞A中每个Fe原子紧邻的原子数为

(3)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式

Ⅱ.在一定温度下,已知以下三个反应的平衡常数:
反应①:


反应②:


反应③:


(4)反应①的平衡常数表达式为
(5)反应③的
 与
与 、
、 的关系是
的关系是
您最近一年使用:0次
名校
3 . 自然界中时刻存在着氮气的转化。实现氮气按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图。下列叙述正确的是
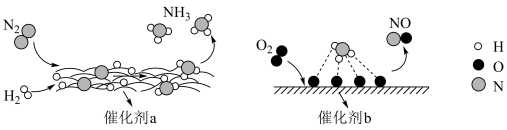
| A.N2→NH3,NH3→NO均属于氮的固定 |
| B.在催化剂a作用下,N2发生了氧化反应 |
| C.催化剂a、b表面均发生了极性共价键的断裂 |
| D.使用催化剂a、b均可以提高单位时间内生成物的产量 |
您最近一年使用:0次
2023-03-07更新
|
1066次组卷
|
23卷引用:天津西青区2022-2023学年高三上学期期末考试化学试题
天津西青区2022-2023学年高三上学期期末考试化学试题北京市丰台区2022-2023学年高一下学期期末考试化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期末考试化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题江苏省南京市第五高级中学2022-2023学年高一下学期3月月考化学试题湖北省沙市中学2022-2023学年高一下学期4月期中考试化学试题北京市第一七一中学2022-2023学年高一下学期期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期5月期中考试化学试题(已下线)第5讲 氮及其化合物四川省泸县第一中学2023-2024学年高二上学期开学考试化学试题广东省东莞实验中学2022-2023学年高一下学期第二次月考化学试题山东省平度市第九中学2020届高三上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——常见无机物及其性质应用——氮及其化合物(提升练习)(已下线)第12讲 氮及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)江苏省淮安市车桥中学2022届高三上学期入学调研(A)化学试题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练河北省博野中学2020-2021学年高三下学期7月月考化学试题湖南省湘潭市第二中学2022届高三下学期4月月考化学试题云南省富源县第一中学2021-2022学年高三下学期4月月考化学试题吉林省九台龙成实验学校2022-2023学年高二上学期第一次月考化学试题广东省湛江市第二十一中学2022-2023学年高二上学期期中考试化学试题湖南省常德市津市市第一中学2023-2024学年高一下学期4月份月考化学试卷 广东省东莞外国语学校 寮步镇外国语学校2023-2024学年高一下学期4月月考化学试题
名校
4 . 下列叙述正确的是
| A.Na与无水乙醇反应时,增大无水乙醇的用量可明显增大化学反应速率 |
| B.原电池中发生的反应达到平衡时,该电池仍有电流产生 |
| C.催化剂能改变化学反应速率,是因为它能改变反应历程和反应的活化能 |
D.Na与 的反应是熵减的放热反应,该反应能自发进行 的反应是熵减的放热反应,该反应能自发进行 |
您最近一年使用:0次
2023-02-27更新
|
181次组卷
|
2卷引用:天津市部分区2022-2023 学年高三上学期1月期末考试化学试题
5 . 等量反应物(R)转化为产物(Q或Q·Z)的能量与反应进程的关系如下图所示:

下列有关说法正确的是

下列有关说法正确的是
| A.进程Ⅰ是放热反应 | B.平衡时R的转化率:Ⅱ>Ⅰ |
| C.生成Q的速率:Ⅲ>Ⅱ | D.进程Ⅳ中,Z有催化作用 |
您最近一年使用:0次
21-22高二上·天津东丽·期末
6 . 甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下: CO2(g) +3H2(g)  CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。
(1)反应过程的能量变化如图所示,起始条件相同,反应过程_______ (填“a”或“b”)达到平衡所需时间短,原因是_______ 。
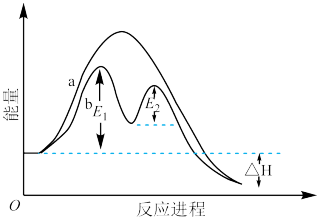
(2)已知容器体积为2L,起始及反应进行2s时部分物质的物质的量如下表:
用H2表示的该反应的反应速率v (H2)=_______ 。
(3)反应的平衡常数表达式为K=_______ ;升高温度, K值_______ (填“增大”、“减小”或“不变”)。
(4)有利于提高平衡时CO2转化率的措施有_______(填字母)。
 CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。(1)反应过程的能量变化如图所示,起始条件相同,反应过程

(2)已知容器体积为2L,起始及反应进行2s时部分物质的物质的量如下表:
| CO2 | H2 | CH3OH | H2O | |
| 起始(mol) | 1.0 | 3.0 | 0 | 0 |
| 2s时(mol) | 0.4 |
(3)反应的平衡常数表达式为K=
(4)有利于提高平衡时CO2转化率的措施有_______(填字母)。
| A.加压 | B.增大CO2的浓度 |
| C.使用催化剂 | D.及时分离出甲醇 |
您最近一年使用:0次
21-22高二上·天津东丽·期末
解题方法
7 . 下列措施对增大反应速率明显有效的是
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取H2时,改用浓硫酸 |
| C.用H2O2溶液制取O2时滴入少量FeCl3溶液 |
| D.Al在氧气中燃烧生成Al2O3,将Al粉改成Al片 |
您最近一年使用:0次
2023-02-11更新
|
181次组卷
|
3卷引用:专题02 化学反应速率与化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)
(已下线)专题02 化学反应速率与化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)天津市东丽区2021-2022学年高二上学期期末考试化学试题【定心卷】2.1.2 影响化学反应速率的因素随堂练习-人教版2023-2024学年选择性必修1
21-22高二上·天津河西·期末
解题方法
8 . 利用催化技术可将汽车尾气中的NO和CO转化成CO2和N2。某课题组查阅资料知:使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。他们为探究增大该化学反应速率的因素,在相同的恒容密闭容器中,进行了三组对比实验,数据如下:
三组实验中c(CO)随时间的变化如图所示:
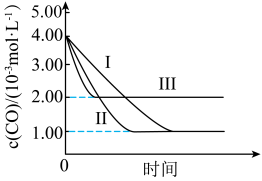
请按要求回答下列问题。
(1)写出反应的化学方程式:_______ 。在上述条件下,该反应均能自发进行,则该反应的ΔH_______ 0(填写“>”、“<”或“=”)
(2)此实验设计探究增大该化学反应速率的因素有_______ 。
(3)T3=_______ ℃。
(4)第Ⅰ组实验中,达到平衡时c(N2)=_______ mol∙L-1。
(5)通过三组实验对比得出结论:
①由实验Ⅰ、Ⅱ可得的结论:在其他条件相同的情况下,_______ 。
②由实验Ⅰ、Ⅲ可得的结论:_______ 。
(6)若与第Ⅰ组实验对比,第Ⅳ组实验仅将c(CO)改为5.00×10-3mol∙L-1,280℃下该反应的平衡常数的值为_______ 。
编号 | T/℃ | c(NO)/( mol∙L-1) | c(CO)/( mol∙L-1) | 催化剂的比表面积/( m2∙g-1) |
Ⅰ | 280. |
|
| 80.0 |
Ⅱ | 360 |
|
| 80.0 |
Ⅲ | T3 |
|
| 120 |

请按要求回答下列问题。
(1)写出反应的化学方程式:
(2)此实验设计探究增大该化学反应速率的因素有
(3)T3=
(4)第Ⅰ组实验中,达到平衡时c(N2)=
(5)通过三组实验对比得出结论:
①由实验Ⅰ、Ⅱ可得的结论:在其他条件相同的情况下,
②由实验Ⅰ、Ⅲ可得的结论:
(6)若与第Ⅰ组实验对比,第Ⅳ组实验仅将c(CO)改为5.00×10-3mol∙L-1,280℃下该反应的平衡常数的值为
您最近一年使用:0次
21-22高二上·天津河西·期末
9 . “人工固氮”对农业生产至关重要。在常温、常压和光照条件下, 在某种催化剂表面与水发生反应为
在某种催化剂表面与水发生反应为 ,反应过程中的能量变化如下图所示。下列有关说法正确的是
,反应过程中的能量变化如下图所示。下列有关说法正确的是
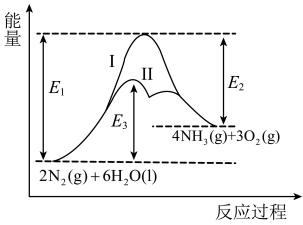
 在某种催化剂表面与水发生反应为
在某种催化剂表面与水发生反应为 ,反应过程中的能量变化如下图所示。下列有关说法正确的是
,反应过程中的能量变化如下图所示。下列有关说法正确的是
A.该反应的焓变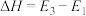 |
| B.升高温度时,活化分子百分数增多 |
| C.过程Ⅱ的平衡转化率比过程Ⅰ的高 |
| D.过程Ⅰ的活化能比过程Ⅱ的高,更易进行 |
您最近一年使用:0次
10 . 工厂的氨氮废水可用电化学催化氧化法加以处理,其中NH3在电极表面的氧化过程的微观示意图如图:
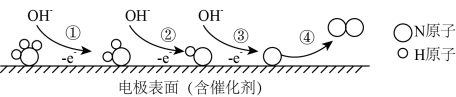
下列说法中,不正确的是

下列说法中,不正确的是
| A.过程①②均有N-H键断裂 |
B.过程③的电极反应式为: |
| C.过程④中没有非极性键形成 |
| D.催化剂可以降低该反应的活化能 |
您最近一年使用:0次
2023-01-12更新
|
208次组卷
|
2卷引用:天津市河西区新华中学2022-2023学年高二上学期期末考试化学试题