解题方法
1 . 向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜,其反应过程如图所示。下列说法不正确 的是
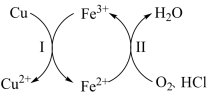

A.制备 的总反应为 的总反应为 |
B.反应Ⅰ中 作氧化剂 作氧化剂 |
C.反应Ⅱ中 作还原剂 作还原剂 |
D.还原性: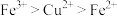 |
您最近一年使用:0次
2 . 乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为C2H5OH(g)+IB(g) ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:
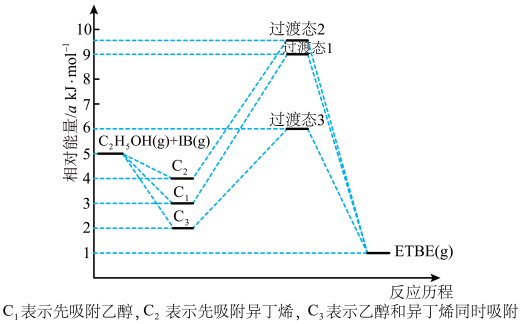
(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=______ kJ•mol-1。反应历程的最优途径是______ (填“C1”、“C2”或“C3”)。 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。
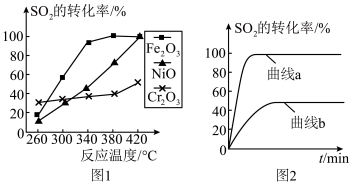
①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是_______ 。
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为______ 。 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=______ ;在图3标出的点中,能表示反应达到平衡状态的点是______ 。
 ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=
 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为
 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
您最近一年使用:0次
3 . 减少 的排放量以及利用
的排放量以及利用 与
与 的反应合成新能源是实现世界气候峰会目标的有效途径。
的反应合成新能源是实现世界气候峰会目标的有效途径。
已知:①
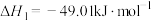
②
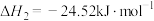
③
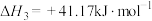
(1)

___________ 
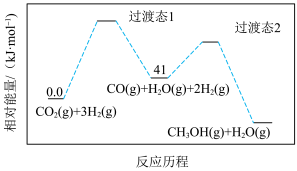
(2)一定条件下, 的反应历程如下图所示。该反应的反应速率由第
的反应历程如下图所示。该反应的反应速率由第___________ (填“1”或“2”)步决定。
(3)向2L恒容密闭容器中充入 和
和 ,在一定条件下,仅发生上述反应①;在甲、乙两种不同催化剂的作用下,反应时间均为
,在一定条件下,仅发生上述反应①;在甲、乙两种不同催化剂的作用下,反应时间均为 时,测得甲醇的物质的量分数随温度的变化如下图所示。
时,测得甲醇的物质的量分数随温度的变化如下图所示。
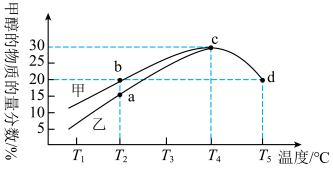
①相同温度下,催化剂效果更好的是___________ (填“甲”或“乙”)。
② 和
和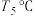 下,平衡常数:
下,平衡常数:
___________ (填“>”、“<”或“=”)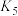 。
。
③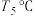 下,反应开始时容器中的总压为
下,反应开始时容器中的总压为 ,该温度下该反应达到平衡时甲醇的分压
,该温度下该反应达到平衡时甲醇的分压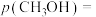
___________ Pa(平衡分压=总压×物质的量分数,只需列出计算式,不必化简)。
(4)已知 的选择性为
的选择性为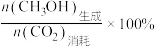 。其他条件相同时,反应温度对
。其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响分别如下图所示。
的选择性的影响分别如下图所示。
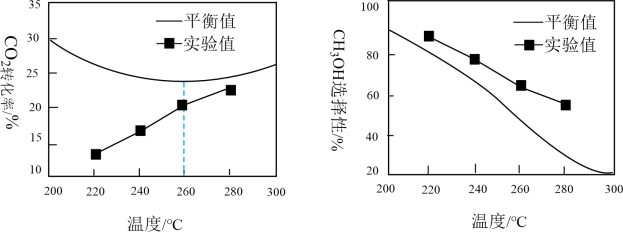
①由温度对 的转化率图可知,实验中反应均未达到化学平衡状态的依据是
的转化率图可知,实验中反应均未达到化学平衡状态的依据是___________ 。
②温度高于260℃时, 的平衡转化率呈上升变化的原因是
的平衡转化率呈上升变化的原因是___________ 。
③由图可知,温度相同时 选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是___________ 。
 的排放量以及利用
的排放量以及利用 与
与 的反应合成新能源是实现世界气候峰会目标的有效途径。
的反应合成新能源是实现世界气候峰会目标的有效途径。已知:①

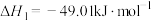
②

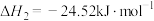
③

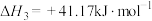
(1)



(2)一定条件下,
 的反应历程如下图所示。该反应的反应速率由第
的反应历程如下图所示。该反应的反应速率由第
(3)向2L恒容密闭容器中充入
 和
和 ,在一定条件下,仅发生上述反应①;在甲、乙两种不同催化剂的作用下,反应时间均为
,在一定条件下,仅发生上述反应①;在甲、乙两种不同催化剂的作用下,反应时间均为 时,测得甲醇的物质的量分数随温度的变化如下图所示。
时,测得甲醇的物质的量分数随温度的变化如下图所示。
①相同温度下,催化剂效果更好的是
②
 和
和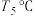 下,平衡常数:
下,平衡常数:
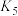 。
。③
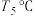 下,反应开始时容器中的总压为
下,反应开始时容器中的总压为 ,该温度下该反应达到平衡时甲醇的分压
,该温度下该反应达到平衡时甲醇的分压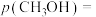
(4)已知
 的选择性为
的选择性为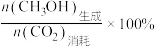 。其他条件相同时,反应温度对
。其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响分别如下图所示。
的选择性的影响分别如下图所示。
①由温度对
 的转化率图可知,实验中反应均未达到化学平衡状态的依据是
的转化率图可知,实验中反应均未达到化学平衡状态的依据是②温度高于260℃时,
 的平衡转化率呈上升变化的原因是
的平衡转化率呈上升变化的原因是③由图可知,温度相同时
 选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
您最近一年使用:0次
名校
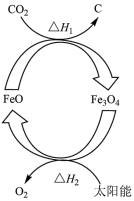
4 . 太阳能的开发与利用是能源领域的一个重要研究方向,由 制取C的太阳能工艺如图所示,下列有关说法
制取C的太阳能工艺如图所示,下列有关说法错误 的是( 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
 制取C的太阳能工艺如图所示,下列有关说法
制取C的太阳能工艺如图所示,下列有关说法 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
A.分解 转移的电子数为 转移的电子数为 |
B.根据盖斯定律, |
C. 在该工艺过程中起催化作用 在该工艺过程中起催化作用 |
| D.该工艺将太阳能转化为化学能 |
您最近一年使用:0次
名校
5 . 下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在 中加入 中加入 ,能加速 ,能加速 的分解速率 的分解速率 |  降低了反应所需的活化能 降低了反应所需的活化能 |
| B | 将盛有 气体的密闭容器浸泡在热水中,容器内气体颜色变深 气体的密闭容器浸泡在热水中,容器内气体颜色变深 |  ,平衡向生成 ,平衡向生成 方向移动 方向移动 |
| C | 向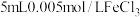 溶液中加入 溶液中加入 溶液,溶液呈红色,再滴加几滴 溶液,溶液呈红色,再滴加几滴 溶液,溶液颜色变浅 溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| D | 在密闭容器中有反应: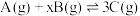 ,达到平衡时测得 ,达到平衡时测得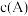 为 为 ,将容器容积扩大到原来的2倍,测得 ,将容器容积扩大到原来的2倍,测得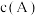 为 为 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-05更新
|
55次组卷
|
2卷引用:甘肃省武威第七中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
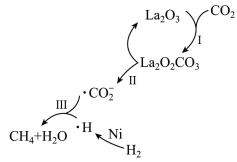
6 . 资源化利用 是实现“碳中和”的重要途径,
是实现“碳中和”的重要途径, 与氢气反应制
与氢气反应制 的一种催化机理如图所示,总反应为
的一种催化机理如图所示,总反应为
 >0,下列说法正确的是
>0,下列说法正确的是
 是实现“碳中和”的重要途径,
是实现“碳中和”的重要途径, 与氢气反应制
与氢气反应制 的一种催化机理如图所示,总反应为
的一种催化机理如图所示,总反应为
 >0,下列说法正确的是
>0,下列说法正确的是
| A.过程Ⅲ中,没有化学键断裂 |
B. 在Ni催化作用下产生·H为吸热过程 在Ni催化作用下产生·H为吸热过程 |
C.反应中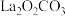 释放出 释放出 |
| D.总反应中,反应物的键能之和小于生成物的键能之和 |
您最近一年使用:0次
2023-11-04更新
|
145次组卷
|
3卷引用:甘肃省白银市靖远县第一中学2023-2024学年高二上学期12月期末考试化学试题
解题方法
7 . 下列各组实验中,化学反应速率最快的是
| 选项 | 反应物 | 催化剂 | 温度 |
| A | 5 mL 10%  溶液 溶液 | 无 | 20℃ |
| B | 5 mL 10%  溶液 溶液 | 无 | 30℃ |
| C | 5 mL 10%  溶液 溶液 |  粉末 粉末 | 20℃ |
| D | 5 mL 10%  溶液 溶液 |  粉末 粉末 | 30℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-02更新
|
170次组卷
|
2卷引用:甘肃省临夏州2022-2023学年高一下学期期末质量检测化学试题
8 . 在一定温度下,向一恒容密闭容器中充入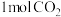 和
和 ,仅发生反应:
,仅发生反应: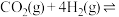
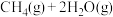 。下列能加快该反应速率的是
。下列能加快该反应速率的是
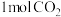 和
和 ,仅发生反应:
,仅发生反应: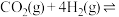
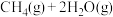 。下列能加快该反应速率的是
。下列能加快该反应速率的是A.向容器中再通入 | B.加入合适的催化剂 |
| C.降低该反应的温度 | D.移出部分产物 |
您最近一年使用:0次
2023-07-14更新
|
79次组卷
|
2卷引用:甘肃省部分学校2022-2023学年高一下学期期末考试化学试题
名校
9 . 在 催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是

 催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
A. 是反应中间体 是反应中间体 | B.反应过程中C的成键数目保持不变 |
| C.含N分子参与的反应一定有电子转移 | D.催化剂参与了化学反应过程 |
您最近一年使用:0次
2023-07-12更新
|
151次组卷
|
2卷引用:甘肃省酒泉市2022-2023学年高一下学期期末考试化学试题
10 . 下列有关化学反应速率和限度的说法中,不正确的是( )
| A.在金属钠与足量水反应中,增加水的量能加快反应速率 |
| B.实验室用H2O2分解制O2,加入几滴FeCl3溶液后,反应速率明显加快 |
C.一定条件下的反应:2SO2+O2 2SO3中,SO2的转化率不能达到100% 2SO3中,SO2的转化率不能达到100% |
| D.实验室用碳酸钙和稀盐酸反应制取CO2,用碳酸钙粉末比块状碳酸钙反应要快 |
您最近一年使用:0次



