名校
解题方法
1 . 工业合成氨对粮食增产、增加人口具重要价值。1913年,Haber-Bosch发明的催化合成氨技术实现了工业化生产:N2(g)+3H2(g)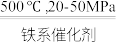 2NH3(g),298K时反应相关数据如表所示:
2NH3(g),298K时反应相关数据如表所示:
已知:化学反应吉布斯自由能变化量ΔG=ΔH -TΔS (通常温度区间,ΔH和ΔS可视为常量),ΔG与压力平衡常数Kp的关系为:lgKp = 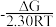 ,Kp为压力平衡常数;R为气体摩尔常数8.314 J·K-1· mol-1;T为热力学温度,单位:K。
,Kp为压力平衡常数;R为气体摩尔常数8.314 J·K-1· mol-1;T为热力学温度,单位:K。
(1)298K时,合成氨反应______ (选填“能”或“不能”)自发进行,理由是___________ 。
(2)实验研究表明,特定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为: ν=kc(N2)·c1.5(H2)·c-1(NH3),下列措施不能提高反应速率的是______ 。
A.适度增加氮气的浓度 B.适度增加氢气的浓度
C.及时将产物氨气分离出反应体系 D.适度提高反应温度
E.在低压下进行反应 F.加入铁催化剂
(3)T℃下,设反应N2(g)+3H2(g) 2NH3(g)的平衡常数为K,反应NH3(g)
2NH3(g)的平衡常数为K,反应NH3(g)
 N2(g)+
N2(g)+  H2(g)的平衡常数为
H2(g)的平衡常数为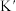 ,则K与
,则K与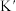 之间的关系是
之间的关系是________ 。298K时,合成氨反应的压力平衡常数Kp(298K )=______ (保留2位有效数字);向一恒定温度的刚性密闭容器中充入物质的量之比为1:1的N2和H2混合气体,初始压强为30MPa,在不同催化剂作用下反应,相同时间内H2的转化率随温度的变化如图所示,b点v正_____ v逆(填“>”、“<”或“=”)。图中a点混合气体平均相对分子质量为18.75,a点对应温度(T4)下反应的平衡常数Kp=______ (保留两位有效数字,Kp为以分压表示的平衡常数,分压=总压 物质的量分数),由此知T4
物质的量分数),由此知T4______ 298K,(选填“>”、“<”或“=”)。

(4)格哈德·埃特尔证实氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:

下列关于合成氨反应的叙述中错误的是________。
(5)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前要经过铜氨溶液处理以除去 CO,反应为:[Cu(NH3)2]2++CO+NH3 [Cu(NH3)3CO]2+ ΔH<0。
[Cu(NH3)3CO]2+ ΔH<0。
①铜氨溶液吸收CO的适宜生产条件是_________ 。
②吸收CO后的铜氨溶液经过适当处理再生,恢复其吸收 CO的能力,可循环使用,铜氨溶液再生的适宜条件是_________ 。
 2NH3(g),298K时反应相关数据如表所示:
2NH3(g),298K时反应相关数据如表所示:| ΔH(kJ·mol-1) | -92.2 |
| ΔS(J·K-1·mol-1) | -198.2 |
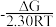 ,Kp为压力平衡常数;R为气体摩尔常数8.314 J·K-1· mol-1;T为热力学温度,单位:K。
,Kp为压力平衡常数;R为气体摩尔常数8.314 J·K-1· mol-1;T为热力学温度,单位:K。(1)298K时,合成氨反应
(2)实验研究表明,特定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为: ν=kc(N2)·c1.5(H2)·c-1(NH3),下列措施不能提高反应速率的是
A.适度增加氮气的浓度 B.适度增加氢气的浓度
C.及时将产物氨气分离出反应体系 D.适度提高反应温度
E.在低压下进行反应 F.加入铁催化剂
(3)T℃下,设反应N2(g)+3H2(g)
 2NH3(g)的平衡常数为K,反应NH3(g)
2NH3(g)的平衡常数为K,反应NH3(g)
 N2(g)+
N2(g)+  H2(g)的平衡常数为
H2(g)的平衡常数为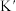 ,则K与
,则K与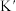 之间的关系是
之间的关系是 物质的量分数),由此知T4
物质的量分数),由此知T4
(4)格哈德·埃特尔证实氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:

下列关于合成氨反应的叙述中错误的是________。
| A.过程表明在化学反应中存在化学键的断裂与形成 |
| B.催化剂能改变化学反应的历程,使反应物化学键更易断裂,活化分子百分比增多 |
| C.过程①③④会放出能量,过程②需吸收能量 |
| D.常温下该反应难以进行,是因为常温下生成物的化学键难以形成 |
(5)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前要经过铜氨溶液处理以除去 CO,反应为:[Cu(NH3)2]2++CO+NH3
 [Cu(NH3)3CO]2+ ΔH<0。
[Cu(NH3)3CO]2+ ΔH<0。①铜氨溶液吸收CO的适宜生产条件是
②吸收CO后的铜氨溶液经过适当处理再生,恢复其吸收 CO的能力,可循环使用,铜氨溶液再生的适宜条件是
您最近半年使用:0次
解题方法
2 . 回答下列问题。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:
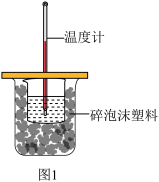
(1)图中装置缺少的仪器是___________ 。
(2)硫酸稍过量的原因是___________ 。
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =___________ (结果保留至小数点后一位)。
(4)上述实验测得中和热的数值小于 57.3kJ·mol-1,产生偏差的原因可能是___________(填字母)。
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
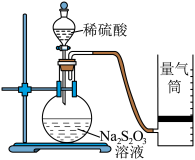
(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是___________ 。除如图所示的实验用品外,还需要的实验仪器 是___________ 。
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是_____________________ 。
实验二:乙同学得到各组实验数据如下表。
(7)实验Ⅰ、Ⅱ探究___________ 对化学反应速率的影响,a=___________ ,V=___________ 。
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是___________ 。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:

(1)图中装置缺少的仪器是
(2)硫酸稍过量的原因是
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =
| 实验序号 | 起始温度t1/℃ | 终止温度T2/℃ | 平均温度差(t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
| 2 | 27.0 | 27.2 | 27.1 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
| A.量取 NaOH 溶液时仰视读数 |
| B.为了使反应充分,向酸溶液中分次加入碱溶液 |
| C.实验装置保温隔热效果差 |
| D.用铜丝代替玻璃搅拌器搅拌 |
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。

(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | |||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | 温度/℃ | |
| I | 0.1 | 3.0 | 0.1 | 3.0 | V | 20 |
| Ⅱ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | a |
| Ⅲ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | 30 |
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
您最近半年使用:0次
3 . 钛是航空、军工、电力等领域重要的金属材料。一种由钛铁矿[主要成分是钛酸亚铁(FeTiO3),还含有少量 等杂质]制备金属钛同时获得
等杂质]制备金属钛同时获得 的工艺流程如图:
的工艺流程如图:
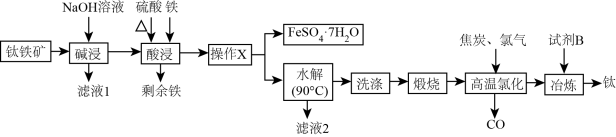
已知:“酸浸”后钛主要以 的形式存在;“水解”后钛以
的形式存在;“水解”后钛以 的形式存在。
的形式存在。
回答下列问题:
(1)基态 的最外层电子排布式为
的最外层电子排布式为_______ 。
(2)写出“水解( )”时发生反应的离子方程式:
)”时发生反应的离子方程式:_______ ;验证“洗涤”达到目的的操作为_______ 。
(3)“高温氯化”时发生反应的化学方程式为_______ ;有利于该过程中“气—固—固”接触的措施是_______ (写一种)。某科研小组模拟“高温氯化”反应理论计算结果显示,在 条件下达到平衡时,
条件下达到平衡时, 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于
,但实际生产中反应温度却远高于 ,其原因是
,其原因是_______ (写一种)。
(4)每次取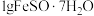 样品,加适量水溶解并加入
样品,加适量水溶解并加入 溶液和
溶液和 溶液,再用
溶液,再用 标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液
标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液 。
。
已知: (黄色)
(黄色)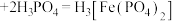 (无色)
(无色)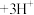 。
。
滴定终点溶液颜色变为_______ ;该样品中 的质量分数为
的质量分数为_______ (填含c,a的表达式)。
 等杂质]制备金属钛同时获得
等杂质]制备金属钛同时获得 的工艺流程如图:
的工艺流程如图:
已知:“酸浸”后钛主要以
 的形式存在;“水解”后钛以
的形式存在;“水解”后钛以 的形式存在。
的形式存在。回答下列问题:
(1)基态
 的最外层电子排布式为
的最外层电子排布式为(2)写出“水解(
 )”时发生反应的离子方程式:
)”时发生反应的离子方程式:(3)“高温氯化”时发生反应的化学方程式为
 条件下达到平衡时,
条件下达到平衡时, 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于
,但实际生产中反应温度却远高于 ,其原因是
,其原因是(4)每次取
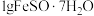 样品,加适量水溶解并加入
样品,加适量水溶解并加入 溶液和
溶液和 溶液,再用
溶液,再用 标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液
标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液 。
。已知:
 (黄色)
(黄色)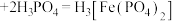 (无色)
(无色)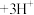 。
。滴定终点溶液颜色变为
 的质量分数为
的质量分数为
您最近半年使用:0次
4 . 辉铜矿主要成分Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,以及少量SiO2、Fe2O3等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰晶体和碱式碳酸铜。主要工艺流程如下:
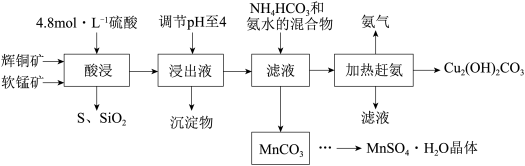
已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
④MnSO4·H2O溶于1份冷水、0.6份沸水,不溶于乙醇。
(1)实验室配制240mL 4.8mol•L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要___________ 。
(2)酸浸时,为了提高浸取率可采取的措施有___________ (任写一点)。
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式:___________ 。
(4)调节浸出液pH=4的作用是___________ 。
(5)写出流程中生成MnCO3的离子方程式___________ 。
(6)MnCO3先加稀硫酸溶解,在经过___________ 得到MnSO4·H2O晶体
(7)本工艺中可循环使用的物质是___________ (写化学式)。

已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
| 金属离子 | Fe3+ | Mn2+ | Cu2+ |
| 开始沉淀pH值 | 1.5 | 8.3 | 4.4 |
| 完全沉淀pH值 | 3.2 | 9.8 | 6.4 |
(1)实验室配制240mL 4.8mol•L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要
(2)酸浸时,为了提高浸取率可采取的措施有
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式:
(4)调节浸出液pH=4的作用是
(5)写出流程中生成MnCO3的离子方程式
(6)MnCO3先加稀硫酸溶解,在经过
(7)本工艺中可循环使用的物质是
您最近半年使用:0次
名校
解题方法
5 . 对Pd单原子催化剂(Pd/SVG)上H2还原NO的反应进行研究,发现Pd/SVG上NO被还原生成N2和NH3的路径机理如图所示:
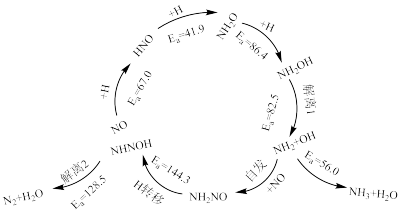
下列说法正确的是

下列说法正确的是
| A.Pd/SVG可以改变NO的平衡转化率 |
| B.NO被还原为N2的总反应为2NO+2H2=N2+2H2O |
| C.NO被还原为NH3的反应决速步为解离1反应 |
| D.Pd/SVG上H2还原NO过程中产物N2的形成更容易 |
您最近半年使用:0次
2021-09-04更新
|
915次组卷
|
3卷引用:安徽省蚌埠市2022届高三上学期第一次教学质量检查化学试题
安徽省蚌埠市2022届高三上学期第一次教学质量检查化学试题(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)安徽省亳州市第二中学2021-2022学年高二上学期期中考试化学试题
解题方法
6 . 研究发现,大多数化学反应并不是经过简单碰撞就能完成的,而往往经过多个反应步骤才能实现。碘钟反应是一种化学振荡反应,其体现了化学动力学的原理。某小组同学在室温下对某“碘钟实验”的原理进行探究。
资料:该“碘钟实验”反应分A、B两步进行:
反应A: (慢)
(慢)
反应B: (快)
(快)
(1)该“碘钟实验”的总反应是___ 。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向K2S2O8溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入试剂Y溶液,溶液的蓝色褪去。
试剂X是___ 、试剂Y是___ 。
(3)已知A反应的速率方程为: (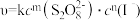 ),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
①表中V1=__ mL,理由是___ ;
②通过数据计算得知:m=___ ,n=___ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验III。(溶液浓度均为0.01mol/L)
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验III未产生颜色变化的原因:___ 。
资料:该“碘钟实验”反应分A、B两步进行:
反应A:
 (慢)
(慢)反应B:
 (快)
(快)(1)该“碘钟实验”的总反应是
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向K2S2O8溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入试剂Y溶液,溶液的蓝色褪去。
试剂X是
(3)已知A反应的速率方程为: (
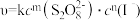 ),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)| 实验 序号 | 试剂体积V/mL | 显色时间 t/s | ||||
| K2S2O8溶液 | KI溶液 | 水 | Na2S2O3溶液 | 淀粉溶液 | ||
| ① | 10 | 10 | 0 | 4 | 1 | 27.0 |
| ② | 5 | 10 | 5 | 4 | 1 | 54.0 |
| ③ | 2.5 | 10 | V1 | 4 | 1 | 108.0 |
| ④ | 10 | 5 | 5 | 4 | 1 | 54.0 |
②通过数据计算得知:m=
(4)为探究其他因素对该“碘钟实验”的影响,进行实验III。(溶液浓度均为0.01mol/L)
| 试剂体积V/mL | ||||
| K2S2O8溶液 | KI溶液 | 水 | Na2S2O3溶液 | 淀粉溶液 |
| 10 | 5 | 3 | 6 | 1 |
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验III未产生颜色变化的原因:
您最近半年使用:0次
7 . 用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)①浸出过程中加入Na2SO3的目的是____ 。
②向浸出液中加入NaClO3的离子反应方程式为____ 。
③为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施____ (答一条即可)。若不慎向“浸出液”中加入NaClO3过量时,可能会生成有毒气体,写出生成该有毒气体的离子方程式____ 。
(2)①“加Na2CO3调pH至a”,过滤所得到的沉淀成分为____ 。
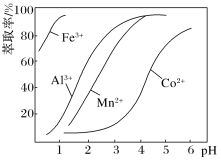
②萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是____ ;其使用的适宜pH范围是____ (填编号)。
A.2.0—2.5 B. 3.0—3.5 C.4.0—4.5 D.5.0—5.5
③“操作1”中包含的基本实验操作,它们依次是_______ 、____ 和过滤、减压烘干。
(3)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤,洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是____ (答一条即可)。

已知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe( OH)3 | Fe(OH)2 | Co(OH)2 | Al( OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
②向浸出液中加入NaClO3的离子反应方程式为
③为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施
(2)①“加Na2CO3调pH至a”,过滤所得到的沉淀成分为
②萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是
A.2.0—2.5 B. 3.0—3.5 C.4.0—4.5 D.5.0—5.5

③“操作1”中包含的基本实验操作,它们依次是
(3)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤,洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近半年使用:0次
2018-02-06更新
|
619次组卷
|
2卷引用:新疆乌鲁木齐地区2018届高三第一次诊断测试化学试题



