名校
1 . I.在恒温2L密闭容器中通入气体X并发生放热反应:2X(g) Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)______ 。
(2)图中c点对应的速率关系是v(正)______ v(逆)(填“>”或“<”或“=”);b曲线与a比改变的条件是______ 。
(3)反应进行到a点时放出的热量______ 反应进行到b点时放出的热量(填“>”或“<”或“=”)。
II.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。______ (计算保留2位有效数字)。
(5)能说明上述反应达到平衡状态的是______ (填字母)。
(6)平衡时CH3OH的体积分数为______ 。平衡混合气体中CO2(g)和H2(g)的质量之比是______ 。
(7)第3分钟时v正(CH3OH)______ 第9分钟时v逆(CH3OH)(填“>”“<”“=”或“无法比较”)。
III.在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如图所示。______ 。
(9)a、b、c、d四个点中,表示化学反应处于平衡状态的点是______ 。
 Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
| A.升高温度 | B.加入适量X |
| C.增大压强 | D.及时分离出Y |
(2)图中c点对应的速率关系是v(正)
(3)反应进行到a点时放出的热量
II.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(5)能说明上述反应达到平衡状态的是
| A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点) |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内生成1molH2,同时生成1molCH3OH |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
(6)平衡时CH3OH的体积分数为
(7)第3分钟时v正(CH3OH)
III.在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如图所示。

(9)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
您最近一年使用:0次
名校
2 . 下列说法正确的是

| A.由气态氨气转化为固态铵盐的过程称为氮的固定 |
| B.用CO2和饱和NaHCO3溶液,使用如图装置可实现喷泉实验 |
| C.密闭容器中充入1molN2和3molH2,充分反应后生成2molNH3 |
| D.燃煤中加入生石灰可以减少SO2的排放 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.标准状况下,11.2LSO3含有的分子数为0.5NA(用NA表示阿伏加德罗常数的值,下同) |
| B.32gCu在足量O2或在足量硫蒸气中完全反应失去的电子数均为NA |
C.H2(g)+I2(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变 |
D.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C可以同时是气体 2C(?)已达平衡,则A、C可以同时是气体 |
您最近一年使用:0次
名校
解题方法
4 . 一定条件下,水气变换反应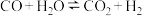 的中间产物是HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:
的中间产物是HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.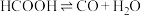 (快) Ⅱ.
(快) Ⅱ. (慢)
(慢)
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。
仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。 温度下,在密封石英管内完全充满
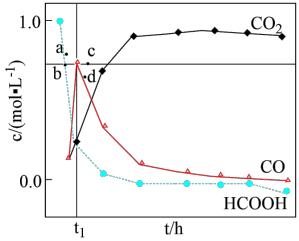
温度下,在密封石英管内完全充满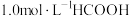 水溶液,使HCOOH分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法不正确的是
水溶液,使HCOOH分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法不正确的是
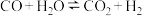 的中间产物是HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:
的中间产物是HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:Ⅰ.
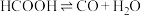 (快) Ⅱ.
(快) Ⅱ. (慢)
(慢)研究发现,在反应Ⅰ、Ⅱ中,
 仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。
仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。 温度下,在密封石英管内完全充满
温度下,在密封石英管内完全充满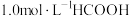 水溶液,使HCOOH分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法不正确的是
水溶液,使HCOOH分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列说法不正确的是
| A.活化能:反应Ⅰ<反应Ⅱ |
B. 时,反应Ⅰ此时已经处于平衡状态 时,反应Ⅰ此时已经处于平衡状态 |
C. 时刻测得CO、 时刻测得CO、 的浓度分别为 的浓度分别为 、 、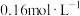 ,反应Ⅱ达平衡时,测得 ,反应Ⅱ达平衡时,测得 的浓度为 的浓度为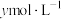 。则反应Ⅱ的平衡常数为 。则反应Ⅱ的平衡常数为 |
D.相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点a、b、c、d中,CO新的浓度峰值点可能是b 盐酸,则图示点a、b、c、d中,CO新的浓度峰值点可能是b |
您最近一年使用:0次
名校
解题方法
5 . 研究NOx、CO、SO2等大气污染气体的治理,对保护环境有重要的意义。回答下列问题:
(1)在一定温度下,向2L的恒容密闭容器中充入4.0molNO2和4.0molCO,在催化剂作用下发生反应:2NO2(g)+4CO(g) N2(g)+4CO2(g),测得相关数据如下:
N2(g)+4CO2(g),测得相关数据如下:
①其他条件不变,若不使用催化剂,则0~5minNO2的转化率将___________ (填“变大”、“变小”或“不变”)。
②以下表述能说明该反应已达到平衡状态的是___________ 。
A.CO的反应速率为N2的4倍 B.气体的颜色不再变化
C.化学平衡常数K不再变化 D.混合气的压强不再变化
③该温度下反应的化学平衡常数K=___________ (保留两位有效数字)。
④在20min时,保持温度不变,继续向容器中再加入2.0molNO2和2.0molN2,则化学平衡___________ 移动(填“正向”、“逆向”或“不”)。
(2)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。CH4还原NO2反应的化学方程式为___________ 。
(1)在一定温度下,向2L的恒容密闭容器中充入4.0molNO2和4.0molCO,在催化剂作用下发生反应:2NO2(g)+4CO(g)
 N2(g)+4CO2(g),测得相关数据如下:
N2(g)+4CO2(g),测得相关数据如下:| 0min | 5min | 10min | 15min | 20min | |
| c(NO2)/mol·L−1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
| c(N2)/mol·L−1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
②以下表述能说明该反应已达到平衡状态的是
A.CO的反应速率为N2的4倍 B.气体的颜色不再变化
C.化学平衡常数K不再变化 D.混合气的压强不再变化
③该温度下反应的化学平衡常数K=
④在20min时,保持温度不变,继续向容器中再加入2.0molNO2和2.0molN2,则化学平衡
(2)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。CH4还原NO2反应的化学方程式为
您最近一年使用:0次
6 . 下列说法符合事实的是
A. 溶液中c(Na+)与c(HSO 溶液中c(Na+)与c(HSO )之比为1:1 )之比为1:1 |
| B.100mL0.1mol·L-1的NaHCO3溶液中含有的氧原子数为0.03NA |
| C.0.1molSO2与足量氧气在一定条件下反应可得到SO3分子的数目为0.1NA |
| D.相同温度和压强下,物质熵的大小比较:1molH2O(s)<1molH2O(g) |
您最近一年使用:0次
名校
解题方法
7 . 一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气( 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
I:
Ⅱ:
Ⅲ:
(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______。(填标号)。
(2)若在恒温恒容容器中仅发生反应Ⅱ,则下列能说明反应达到平衡状态的是_______。
(3)在体积为1L的密闭容器中,充入1 mol 和3 mol
和3 mol  ,一定条件下发生反应Ⅲ。反应过程中测得
,一定条件下发生反应Ⅲ。反应过程中测得 和
和 的浓度随时间变化如图2所示:3 min时的正反应速率
的浓度随时间变化如图2所示:3 min时的正反应速率_______ (填“>”,“=”或“<”)逆反应速率,从反应开始到第10 min,氢气的平均反应速率
_______ 。
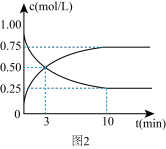
(4)在体积为V L并带有滑动活塞的恒温密闭容器中加入2 mol X和2 mol Y,发生如下反应(X、Y状态未知): 。10分钟后达到平衡,此时X、Y、Z的物质的量之比为
。10分钟后达到平衡,此时X、Y、Z的物质的量之比为 ,且容器的体积不变,则a=
,且容器的体积不变,则a=_______ ;X的状态为_______ (填“气态”或“非气态”)。
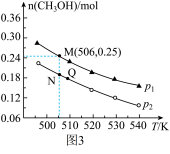
(5)由CO2和H2合成CH3OH 的反应如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH
CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH_______ 0(填“> ”或“<”),判断理由是_______ 。图中压强p1_______ p2( “>”或“<”),N点时,该反应的平衡常数K=_______ (计算结果保留2位小数)。
(6)
(7)
 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:I:

Ⅱ:

Ⅲ:

(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______。(填标号)。
| A.加入焦炭 | B.通入CO | C.升高温度 | D.分离出氢气 |
(2)若在恒温恒容容器中仅发生反应Ⅱ,则下列能说明反应达到平衡状态的是_______。
| A.容器内气体的压强不变 |
| B.容器内气体的总质量不变 |
| C.容器内气体的平均相对分子质量不变 |
D.单位时间内,每有2 mol  键断裂,同时有1 mol 键断裂,同时有1 mol  键断裂 键断裂 |
(3)在体积为1L的密闭容器中,充入1 mol
 和3 mol
和3 mol  ,一定条件下发生反应Ⅲ。反应过程中测得
,一定条件下发生反应Ⅲ。反应过程中测得 和
和 的浓度随时间变化如图2所示:3 min时的正反应速率
的浓度随时间变化如图2所示:3 min时的正反应速率
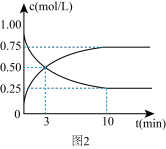
(4)在体积为V L并带有滑动活塞的恒温密闭容器中加入2 mol X和2 mol Y,发生如下反应(X、Y状态未知):
 。10分钟后达到平衡,此时X、Y、Z的物质的量之比为
。10分钟后达到平衡,此时X、Y、Z的物质的量之比为 ,且容器的体积不变,则a=
,且容器的体积不变,则a=(5)由CO2和H2合成CH3OH 的反应如下:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH
CH3OH(g)+H2O(g) ΔH,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,则反应的ΔH(6)
(7)

您最近一年使用:0次
名校
8 . 对利用甲烷消除 污染进行研究,
污染进行研究,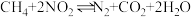 。在
。在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入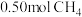 和
和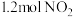 ,测得
,测得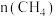 随时间变化的有关实验数据见下表。下列说法正确的是
随时间变化的有关实验数据见下表。下列说法正确的是
 污染进行研究,
污染进行研究,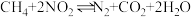 。在
。在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入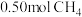 和
和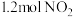 ,测得
,测得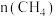 随时间变化的有关实验数据见下表。下列说法正确的是
随时间变化的有关实验数据见下表。下列说法正确的是| 组别 | 温度 | 时间  | 0 | 10 | 20 | 40 | 50 |
| ① |  | 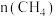 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② |  | 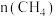 | 0.50 | 0.30 | 0.18 | 0.15 |
A.组别1中, 内, 内, 的降解速率为 的降解速率为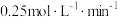 |
B.由实验数据可知实验控制的温度 |
C.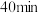 时,表格中 时,表格中 对应反应已经达到平衡状态 对应反应已经达到平衡状态 |
D. 内, 内, 的降解速率①>② 的降解速率①>② |
您最近一年使用:0次
2023-10-02更新
|
155次组卷
|
24卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
黑龙江省牡丹江市第一高级中学2022-2023学年高一下学期5月期中考试化学试题浙江省丽水市四校2018-2019学年高一下学期期中化学试题高一必修第二册(人教2019版)全书综合训练河北省安平中学2020-2021学年高二上学期第一次月考化学试题黑龙江省鹤岗市第一中学2021届高三上学期第二次月考化学试题江苏省海安市2020-2021学年高二上学期期中考试化学试题江西省景德镇市昌江区景德镇一中2020-2021学年高二上学期期中考试化学试题(1班)山东师范大学附属中学2020-2021学年高一下学期期中学分认定考试化学(等级考)试题河北省任丘一中2021-2022学年高二上学期开学考试化学试题江苏省盐城市阜宁中学等四校2021-2022学年高一下学期期中考试化学试题江苏省南京市六校联合体2021-2022高一下学期期中考试化学试题山东省泰安市2021-2022学年高一下学期期末考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高二上学期期中考试化学试题四川省成都市东部新区养马高级中学2022-2023学年高二上学期期中考试化学试题江苏省南通市海安高级中学2022-2023学年高一下学期第一次月考化学试题福建省福州格致中学2022-2023学年高一下学期期中考试化学试题河北省正定中学2022-2023学年高一下学期第二次月考化学试题安徽省亳州市第二完全中学2022-2023学年高一下学期期中考试化学试题(特培班)江西省九江市德安县第一中学2022-2023学年高一下学期5月期中考试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第一次调研考试化学试题云南省下关第一中学2023-2024学年高二上学期9月月考化学试题江苏省常州高级中学2023~2024 学年高二上学期10月阶段检测化学试题湖北省黄州中学(黄冈市外国语学校)2023-2024学年高二上学期9月月考化学试题阶段重点练(四)
名校
解题方法
9 . 一定条件下,容积2L的密闭容器中,将2molL气体和3molM气体混合,发生如下反应: ,10s末,生成2.4molR,测得Q的浓度为0.4mol/L。
,10s末,生成2.4molR,测得Q的浓度为0.4mol/L。
(1)前10s内用M表示的化学反应速率为_______ 。
(2)化学方程式中x值为_______ 。
(3)10s末L的转化率是_______ 。
(4)下列说法可以说明该反应已达平衡的是_______ 。(填序号)
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3molM的同时生成3molR
⑤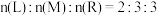
 ,10s末,生成2.4molR,测得Q的浓度为0.4mol/L。
,10s末,生成2.4molR,测得Q的浓度为0.4mol/L。(1)前10s内用M表示的化学反应速率为
(2)化学方程式中x值为
(3)10s末L的转化率是
(4)下列说法可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3molM的同时生成3molR
⑤
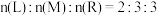
您最近一年使用:0次
名校
10 . 下列实验方案不能 达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去MgO中的Al2O3 | 加入过量的NaOH溶液,过滤、洗涤、干燥 |
| B | 制备 胶体 胶体 | 向NaOH稀溶液中加入饱和FeCl3溶液,然后煮沸 |
| C | 探究乙醇的还原性 | 向盛有2mL酸性重铬酸钾溶液的试管中加入乙醇,观察现象 |
| D | 探究FeCl3与KI溶液反应的可逆性 | 向盛有5mL KI溶液的试管中滴入同浓度的FeCl3溶液5~6滴,然后加入2mLCCl4充分振荡,静置后在上层清液中滴入KSCN溶液,观察现象 KI溶液的试管中滴入同浓度的FeCl3溶液5~6滴,然后加入2mLCCl4充分振荡,静置后在上层清液中滴入KSCN溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次