1 . “绿水青山就是金山银山”,在人们高度重视环境和保护环境的今天,处理和利用氮氧化物、碳氧化物、硫氧化物对改善大气质量具有重要的意义
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物可防止氮氧化物污染,如反应2CO(g)+2NO(g)=2CO2(g)+N2(g) △H=-747 kJ/mol。
已知:ⅰ.2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol
ⅱ.N2(g)+O2(g)=2NO(g) △H=+181 kJ/mol
则表示C(s)燃烧热的热化学方程式为___________ 。
(2)向某恒容绝热密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) △H,下列说法中能够判断该反应处于平衡状态的有
2SO3(g) △H,下列说法中能够判断该反应处于平衡状态的有___________ (填标号)。
A.SO2(g)与SO3(g)的物质的量之比恒定不变
B.SO2(g)与O2(g)的物质的量之比恒定不变
C.容器中温度恒定不变
D.混合物中S元素的质量分数恒定不变
(3)已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H。将1 mol CO2和3 mol H2充入1 L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO2的转化率与温度的对应关系如图所示:
CH3OH(g)+H2O(g) △H。将1 mol CO2和3 mol H2充入1 L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO2的转化率与温度的对应关系如图所示:
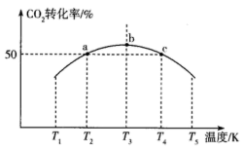
①△H___________ 0(填“>”或“<”)。
②能否根据a点CO2的转化率求出反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)在T2K下的平衡常数?
CH3OH(g)+H2O(g)在T2K下的平衡常数?___________ (填“能”或“不能”),理由是___________ 。
③已知c点时容器内的气体压强为p,在T4K下该反应的平衡常数Kp为___________ (用含p的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物可防止氮氧化物污染,如反应2CO(g)+2NO(g)=2CO2(g)+N2(g) △H=-747 kJ/mol。
已知:ⅰ.2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol
ⅱ.N2(g)+O2(g)=2NO(g) △H=+181 kJ/mol
则表示C(s)燃烧热的热化学方程式为
(2)向某恒容绝热密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g)
 2SO3(g) △H,下列说法中能够判断该反应处于平衡状态的有
2SO3(g) △H,下列说法中能够判断该反应处于平衡状态的有A.SO2(g)与SO3(g)的物质的量之比恒定不变
B.SO2(g)与O2(g)的物质的量之比恒定不变
C.容器中温度恒定不变
D.混合物中S元素的质量分数恒定不变
(3)已知:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H。将1 mol CO2和3 mol H2充入1 L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO2的转化率与温度的对应关系如图所示:
CH3OH(g)+H2O(g) △H。将1 mol CO2和3 mol H2充入1 L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO2的转化率与温度的对应关系如图所示:
①△H
②能否根据a点CO2的转化率求出反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)在T2K下的平衡常数?
CH3OH(g)+H2O(g)在T2K下的平衡常数?③已知c点时容器内的气体压强为p,在T4K下该反应的平衡常数Kp为
您最近一年使用:0次
解题方法
2 . 合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
常温下,大气固氮的倾向______ 工业固氮(填“大于”或“小于”)。
(2)N2(g)与H2(g)反应的能量变化如图所示。
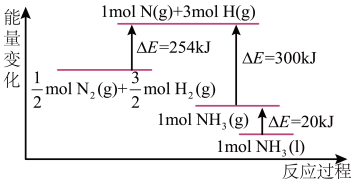
则N2(g)与H2(g)制备NH3(l)的热化学方程式为__________________ 。
(3)T ℃时,在 2 L恒容密闭容器中加入 1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)⇌2NH3(g)],体系中n(NH3)随时间的变化如图。
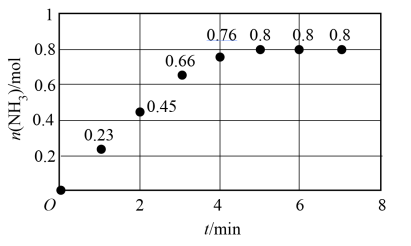
①前2分钟内的平均反应速率v(NH3)=______ mol·L-1·min-1。
②下列情况能说明该反应已达到平衡状态的是______ (选填序号)。
A.混合气体的密度不变
B.单位时间内断裂n mol N—H键的同时形成n mol H—H键
C.容器内的总压强不再变化
D.3v 正(H2)=2v 逆(NH3)
③有关工业固氮的说法正确的是______ (选填序号)。
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
④T ℃时,该反应的平衡常数为______ 。
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol·min-1)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是______ (填化学式)。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
| 反应 | 大气固氮N2(g)+O2(g)⇌2NO(g) | 工业固氮N2(g)+3H2(g)⇌2NH3(g) | ||||
| 温度/℃ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数(K) | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g)反应的能量变化如图所示。

则N2(g)与H2(g)制备NH3(l)的热化学方程式为
(3)T ℃时,在 2 L恒容密闭容器中加入 1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)⇌2NH3(g)],体系中n(NH3)随时间的变化如图。

①前2分钟内的平均反应速率v(NH3)=
②下列情况能说明该反应已达到平衡状态的是
A.混合气体的密度不变
B.单位时间内断裂n mol N—H键的同时形成n mol H—H键
C.容器内的总压强不再变化
D.3v 正(H2)=2v 逆(NH3)
③有关工业固氮的说法正确的是
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
④T ℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol·min-1)与催化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近一年使用:0次
2020-09-28更新
|
173次组卷
|
2卷引用:吉林省长春市北师大附属学校2021-2022学年高三上学期第一次月考化学试题
解题方法
3 . 运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+216.4kJ/mol
CO(g)+3H2(g) ∆H1=+216.4kJ/mol
b. CO(g)+H2O(g) CO2(g)+H2(g) ∆H2= –41.2kJ/mol
CO2(g)+H2(g) ∆H2= –41.2kJ/mol
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= _________ 。
(2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
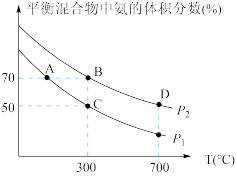
①恒压时,反应一定达到平衡状态的标志是_________ (填序号)
A. 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变
C. 保持不变 D.
保持不变 D.
②P1_________ P2 (填“>” “<”“=”或“不确定”,下同);反应的平衡常数:B点_________ D点。
③C点 的转化率为
的转化率为_________ ;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)_________ υ(B)。
Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。

(3)已知阴极室溶液呈酸性,则阴极的电极反应式为_________ 。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H1=+216.4kJ/mol
CO(g)+3H2(g) ∆H1=+216.4kJ/molb. CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H2= –41.2kJ/mol
CO2(g)+H2(g) ∆H2= –41.2kJ/mol则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= (2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。

①恒压时,反应一定达到平衡状态的标志是
A.
 和
和 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变C.
 保持不变 D.
保持不变 D.
②P1
③C点
 的转化率为
的转化率为Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。

(3)已知阴极室溶液呈酸性,则阴极的电极反应式为
您最近一年使用:0次
解题方法
4 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_______ 。该反应需要在加压下进行,原因是_______ 。
(2)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_______ 。
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应: (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
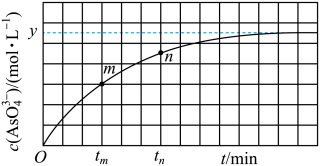
①下列可判断反应达到平衡的是_______ (填标号)。
a.溶液的pH不再变化 b.v(I−)=2v( )
)
c. c( )/c(
)/c( )不再变化 d. c(I−)=y mol·L−1
)不再变化 d. c(I−)=y mol·L−1
②tm时v逆_______ tn时v逆(填“大于”“小于”或“等于”),理由是_______ 。
③tm若平衡时溶液的pH=14,则该反应的平衡常数K为_______ 。
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(2)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH22As(s)+
 O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =
(3)298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应:
 (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I−)=2v(
 )
)c. c(
 )/c(
)/c( )不再变化 d. c(I−)=y mol·L−1
)不再变化 d. c(I−)=y mol·L−1②tm时v逆
③tm若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次
5 . 目前,世界各国相继规划了碳达峰、碳中和。开发CO2利用技术、降低空气中CO2含量成为研究热点。可采用以下方法将CO2进行资源化利用。
(1)CO2催化加氢制甲醇。一定温度下,在某恒容密闭容器中充入一定量的CO2和H2,发生反应:CO2(g)+3H2(g) CH3OH(g) + H2O(g)。下列叙述能说明反应已达到平衡状态的是_______(填标号)
CH3OH(g) + H2O(g)。下列叙述能说明反应已达到平衡状态的是_______(填标号)
(2)CO2催化加氢合成乙烯。在10L某恒容密闭容器中,充入1.4mol CO2和4.2mol H2,发生反应:2CO2(g)+6H2(g) C2 H4(g) + 4H2O(g) ΔH。反应达到平衡后,四种组分的物质的量分数x随温度T的变化如图所示。
C2 H4(g) + 4H2O(g) ΔH。反应达到平衡后,四种组分的物质的量分数x随温度T的变化如图所示。
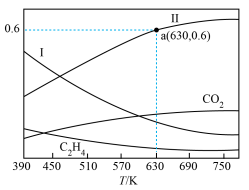
①该反应的ΔH_______ 0(填“>”或“<”),曲线Ⅰ和曲线Ⅱ分别表示_______ (填化学式,下同)和_______ 的变化曲线。
②根据图中a点,计算该温度下平衡时的n(H2O)=_______ mol,c(C2H4)=_______ mol•L-1,CO2 的转化率为_______ %(保留三位有效数字)。
③若平衡时a点容器内气体的总压强为0.25MPa,则该反应平衡常数KP=_______ (MPa)-3(列出计算式即可,分压=总压×物质的量分数,KP就是用分压代替平衡浓度求算的平衡常数)
(3)CO2用途广泛,写出其基于物理性质的一种用途:_______ 。
(1)CO2催化加氢制甲醇。一定温度下,在某恒容密闭容器中充入一定量的CO2和H2,发生反应:CO2(g)+3H2(g)
 CH3OH(g) + H2O(g)。下列叙述能说明反应已达到平衡状态的是_______(填标号)
CH3OH(g) + H2O(g)。下列叙述能说明反应已达到平衡状态的是_______(填标号)| A.混合气体的密度不再随时间变化 |
| B.气体的压强不再随时间变化 |
| C.CH3OH的物质的量分数不再随时间变化 |
| D.单位时间内每形成3mol H—H键,同时断开3mol C—H键。 |
 C2 H4(g) + 4H2O(g) ΔH。反应达到平衡后,四种组分的物质的量分数x随温度T的变化如图所示。
C2 H4(g) + 4H2O(g) ΔH。反应达到平衡后,四种组分的物质的量分数x随温度T的变化如图所示。
①该反应的ΔH
②根据图中a点,计算该温度下平衡时的n(H2O)=
③若平衡时a点容器内气体的总压强为0.25MPa,则该反应平衡常数KP=
(3)CO2用途广泛,写出其基于物理性质的一种用途:
您最近一年使用:0次
2022-11-03更新
|
39次组卷
|
2卷引用:河北省唐山市滦南县第一中学2021-2022学年高二上学期期中考试化学试题
名校
6 . 回答下列问题:
(1)微生物作用下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

1mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(2)高能燃料肼N2H4,俗称联氨。在工业生产中用途广泛。已知N2H4(l)+O2(g)=N2(g)+2H2O(l)ΔH=-622kJ·mol-1,计算16gN2H4(l)燃烧生成氮气和液态水(反应①)时放出的热量为_______ kJ。相同条件下,若生成氮气和水蒸气(反应②),则反应②放出的热量比①_______ (填“多”或“少”)。
(3)甲醇是一种重要的化工原料,CO可用于合成甲醇,发生反应:CO(g)+2H2(g)⇌CH3OH(g)。在一容积可变的密闭容器中充有1molCO与2molH2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(ɑ)与温度(T)、压强(p)的关系如图所示。
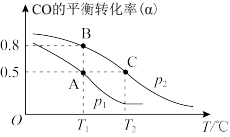
①p1_______ p2(填“>”“<”或“=”)
②A、B、C三点的平衡常数(KA、KB、KC)大小关系为_______ (用“>”“<”或“=”连接,下同)
③A、B、C三点容器内混合气体的平均摩尔质量(MA、MB、MC)大小关系为_______ 。
④下列可作为反应达到化学平衡状态的标志的是_______ (填字母)
A.CO、CH3OH的物质的量之比保持不变
B.生成1molCO的同时生成2molH2
C.CO、H2、CH3OH的物质的量之比为1:2:1
D.CH3OH的体积分数不再变化
(1)微生物作用下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
1mol
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是(2)高能燃料肼N2H4,俗称联氨。在工业生产中用途广泛。已知N2H4(l)+O2(g)=N2(g)+2H2O(l)ΔH=-622kJ·mol-1,计算16gN2H4(l)燃烧生成氮气和液态水(反应①)时放出的热量为
(3)甲醇是一种重要的化工原料,CO可用于合成甲醇,发生反应:CO(g)+2H2(g)⇌CH3OH(g)。在一容积可变的密闭容器中充有1molCO与2molH2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(ɑ)与温度(T)、压强(p)的关系如图所示。

①p1
②A、B、C三点的平衡常数(KA、KB、KC)大小关系为
③A、B、C三点容器内混合气体的平均摩尔质量(MA、MB、MC)大小关系为
④下列可作为反应达到化学平衡状态的标志的是
A.CO、CH3OH的物质的量之比保持不变
B.生成1molCO的同时生成2molH2
C.CO、H2、CH3OH的物质的量之比为1:2:1
D.CH3OH的体积分数不再变化
您最近一年使用:0次
2022-08-18更新
|
132次组卷
|
3卷引用:重庆市石柱中学校2021-2022学年高二上学期第一次月考化学试题
解题方法
7 . 当今,世界各国相继规划了碳达峰、碳中和的时间节点。因此,研发 利用技术、降低空气中
利用技术、降低空气中 含量成为了研究热点。为减少
含量成为了研究热点。为减少 对环境造成的影响,可采用以下方法将其资源化利用。
对环境造成的影响,可采用以下方法将其资源化利用。
(1) 催化加氢制甲醇
催化加氢制甲醇
一定温度下,在某恒容密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: 。下列叙述能说明该反应已达到平衡状态的是___________(填标号)
。下列叙述能说明该反应已达到平衡状态的是___________(填标号)
(2) 催化加氢合成乙烯
催化加氢合成乙烯
在10 L某恒容密闭容器中,充入1.4mol 和4.2mol
和4.2mol  发生反应:
发生反应:
 。反应达到平衡时,四种组分的物质的量分数
。反应达到平衡时,四种组分的物质的量分数 随温度
随温度 的变化如图所示。
的变化如图所示。

①该反应的
___________ (填“>”或“<”)0,曲线Ⅰ和曲线Ⅱ分别表示___________ (填化学式,下同)和___________ 的变化曲线。
②根据图中a点,计算该温度时的
___________ mol,
___________  ,
, 的平衡转化率为
的平衡转化率为___________ %(保留三位有效数字)。
③若平衡时a点的压强为0.25 MPa,则该反应的平衡常数
___________  (列出计算式,用分压表示,分压=总压×物质的量分数)
(列出计算式,用分压表示,分压=总压×物质的量分数)
(3) 用途广泛,写出其基于物理性质的一种用途:
用途广泛,写出其基于物理性质的一种用途:___________ 。
 利用技术、降低空气中
利用技术、降低空气中 含量成为了研究热点。为减少
含量成为了研究热点。为减少 对环境造成的影响,可采用以下方法将其资源化利用。
对环境造成的影响,可采用以下方法将其资源化利用。(1)
 催化加氢制甲醇
催化加氢制甲醇一定温度下,在某恒容密闭容器中充入一定量的
 和
和 ,发生反应:
,发生反应: 。下列叙述能说明该反应已达到平衡状态的是___________(填标号)
。下列叙述能说明该反应已达到平衡状态的是___________(填标号)| A.混合气体的密度不再随时间变化而改变 |
| B.气体的压强不再随时间变化而改变 |
C. 的物质的量分数不再随时间变化而改变 的物质的量分数不再随时间变化而改变 |
| D.单位时间内每形成1.5mol H-H键,同时形成1mol C-H键 |
 催化加氢合成乙烯
催化加氢合成乙烯在10 L某恒容密闭容器中,充入1.4mol
 和4.2mol
和4.2mol  发生反应:
发生反应:
 。反应达到平衡时,四种组分的物质的量分数
。反应达到平衡时,四种组分的物质的量分数 随温度
随温度 的变化如图所示。
的变化如图所示。
①该反应的

②根据图中a点,计算该温度时的


 ,
, 的平衡转化率为
的平衡转化率为③若平衡时a点的压强为0.25 MPa,则该反应的平衡常数

 (列出计算式,用分压表示,分压=总压×物质的量分数)
(列出计算式,用分压表示,分压=总压×物质的量分数)(3)
 用途广泛,写出其基于物理性质的一种用途:
用途广泛,写出其基于物理性质的一种用途:
您最近一年使用:0次
名校
解题方法
8 . 甲醇是一种重要的有机化工原料,在工业上有着重要的用途。
(1)利用CO和H,也可以合成甲醇,其反应为
 ,相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1∶2的CO和
,相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1∶2的CO和 的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图所示。
的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图所示。
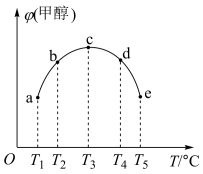
①从a点到c点,温度升高甲醇的体积分数增大的原因是___________ 。
②根据图象判断a___________ (填“>”“<”或“=”)0。
③下列说法能说明反应达到平衡状态的是___________ (填字母)。
A.容器中气体压强不再变化
B.用 和
和 表示的反应速率之比为2∶1
表示的反应速率之比为2∶1
C.混合气体的密度不变
D.单位时间内生成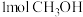 的同时生成
的同时生成
(2)若在 、10MPa条件下,往一密闭容器通入CO和
、10MPa条件下,往一密闭容器通入CO和 合成甲醇[其中
合成甲醇[其中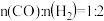 ],测得容器内总压强与反应时间的关系如图所示。
],测得容器内总压强与反应时间的关系如图所示。

①图中A点时,CO的转化率为___________ 。
②在其他条件不变的情况下,测得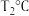 时压强的变化曲线如图所示,则C点的正反应速率
时压强的变化曲线如图所示,则C点的正反应速率 与A点的逆反应速率
与A点的逆反应速率 的大小关系为
的大小关系为
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③图中B点的压强平衡常数
___________ ( 为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(只需要列出计算式即可)
为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(只需要列出计算式即可)
(1)利用CO和H,也可以合成甲醇,其反应为

 ,相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1∶2的CO和
,相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1∶2的CO和 的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图所示。
的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图所示。
①从a点到c点,温度升高甲醇的体积分数增大的原因是
②根据图象判断a
③下列说法能说明反应达到平衡状态的是
A.容器中气体压强不再变化
B.用
 和
和 表示的反应速率之比为2∶1
表示的反应速率之比为2∶1C.混合气体的密度不变
D.单位时间内生成
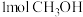 的同时生成
的同时生成
(2)若在
 、10MPa条件下,往一密闭容器通入CO和
、10MPa条件下,往一密闭容器通入CO和 合成甲醇[其中
合成甲醇[其中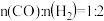 ],测得容器内总压强与反应时间的关系如图所示。
],测得容器内总压强与反应时间的关系如图所示。
①图中A点时,CO的转化率为
②在其他条件不变的情况下,测得
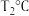 时压强的变化曲线如图所示,则C点的正反应速率
时压强的变化曲线如图所示,则C点的正反应速率 与A点的逆反应速率
与A点的逆反应速率 的大小关系为
的大小关系为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③图中B点的压强平衡常数

 为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(只需要列出计算式即可)
为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(只需要列出计算式即可)
您最近一年使用:0次
2021-11-21更新
|
1012次组卷
|
6卷引用:湖南师范大学附属中学2021-2022学年高三上学期月考试卷(二)化学试题
湖南师范大学附属中学2021-2022学年高三上学期月考试卷(二)化学试题江西省丰城中学2021-2022学年上学期高三创新实验班第四次月考化学试题安徽省宣城中学2021-2022学年高二上学期12月月考化学试题(已下线)2022年广东卷高考真题变式题(17-21)(已下线)模拟卷06-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)四川省泸州市叙永第一中学校2023-2024学年高二上学期1月期末化学试题
解题方法
9 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式___________ 。
(2)已知: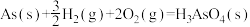

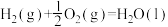

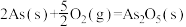
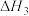
则反应 的
的
___________ ;
(3)298K时,将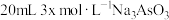 、
、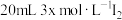 和20mL NaOH溶液混合,发生反应:
和20mL NaOH溶液混合,发生反应: 。溶液中
。溶液中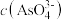 与反应时间(t)的关系如图所示。
与反应时间(t)的关系如图所示。
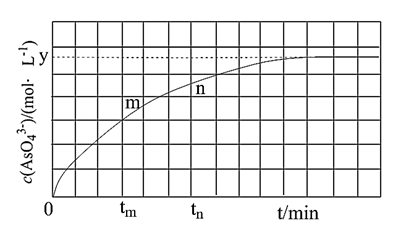
①下列不可判断反应达到平衡的是___________ (填标号);
a.溶液的pH不再变化 b.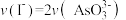
c.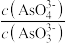 不再变化 d.
不再变化 d.
②tn时v逆___________ tm时v逆(填“>” 、“<”或“=”);
③若平衡时溶液的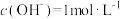 ,则该反应的化学平衡常数K=
,则该反应的化学平衡常数K=___________ 。(用含x、y的式子表示);
(4) H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图1和题图2所示:
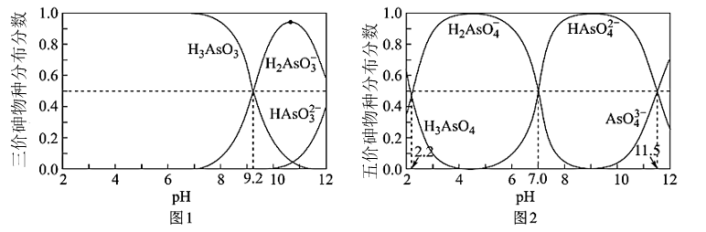
①以酚酞为指示剂(变色范围pH:8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为___________ ;
②H3AsO4第一步电离方程式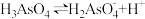 的电离常数为Ka1,则pKa1=
的电离常数为Ka1,则pKa1=___________ ( );
);
(1)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(2)已知:
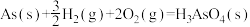

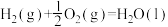

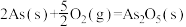
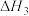
则反应
 的
的
(3)298K时,将
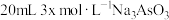 、
、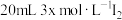 和20mL NaOH溶液混合,发生反应:
和20mL NaOH溶液混合,发生反应: 。溶液中
。溶液中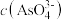 与反应时间(t)的关系如图所示。
与反应时间(t)的关系如图所示。
①下列不可判断反应达到平衡的是
a.溶液的pH不再变化 b.
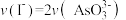
c.
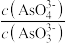 不再变化 d.
不再变化 d.
②tn时v逆
③若平衡时溶液的
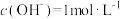 ,则该反应的化学平衡常数K=
,则该反应的化学平衡常数K=(4) H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图1和题图2所示:

①以酚酞为指示剂(变色范围pH:8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
②H3AsO4第一步电离方程式
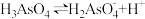 的电离常数为Ka1,则pKa1=
的电离常数为Ka1,则pKa1= );
);
您最近一年使用:0次
名校
解题方法
10 . 甲醇是一种重要的有机化工原料,在工业上有着重要的用途。
(1)用CO和H2可以合成甲醇,其反应为CO(g)+2H2(g) CH3OH(g) △H=akJ/mol。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到tmin时甲醇的体积分数如图1所示。
CH3OH(g) △H=akJ/mol。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到tmin时甲醇的体积分数如图1所示。
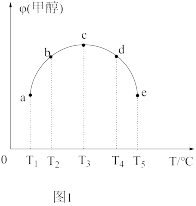
①从a点到c点,温度升高甲醇的体积分数增大的原因是___________ 。
②根据图象判断a___________ 0;(填“>”“<”或“=”)
③下列说法能说明反应达到平衡状态的是___________ (填字母)。
A.容器中气体压强不再变化 B.用H2和CH3OH表示的反应速率之比为2:1
C.混合气体的密度不变 D.单位时间内生成1molCH3OH的同时生成2molH2
(2)若在T1℃、10MPa条件下,往一密闭刚性容器通入CO和H2合成甲醇[n(CO):n(H2)=1:2],测得容器内总压强与反应时间的关系如图2所示。

①图中A点时,CO的转化率为___________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率Vc(正)与A点VA(逆)的逆反应速率的大小关系为Vc(正)___________ VA(逆)(填“>”“<”或“=”)。
③B点加入一定量的CH3OH(g),则再次平衡后CO的体积分数___________ (填“增大”“减小”或“不变”),B点和C点的平衡常数的大小关系为KB___________ KC(填“>”“<”或“=”)。
④图中B点的压强平衡常数Kp=___________ (Kp为压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(只需要列出计算式即可)
(1)用CO和H2可以合成甲醇,其反应为CO(g)+2H2(g)
 CH3OH(g) △H=akJ/mol。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到tmin时甲醇的体积分数如图1所示。
CH3OH(g) △H=akJ/mol。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到tmin时甲醇的体积分数如图1所示。
①从a点到c点,温度升高甲醇的体积分数增大的原因是
②根据图象判断a
③下列说法能说明反应达到平衡状态的是
A.容器中气体压强不再变化 B.用H2和CH3OH表示的反应速率之比为2:1
C.混合气体的密度不变 D.单位时间内生成1molCH3OH的同时生成2molH2
(2)若在T1℃、10MPa条件下,往一密闭刚性容器通入CO和H2合成甲醇[n(CO):n(H2)=1:2],测得容器内总压强与反应时间的关系如图2所示。

①图中A点时,CO的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率Vc(正)与A点VA(逆)的逆反应速率的大小关系为Vc(正)
③B点加入一定量的CH3OH(g),则再次平衡后CO的体积分数
④图中B点的压强平衡常数Kp=
您最近一年使用:0次



