1 . 下列事实能用勒夏特列原理来解释的是
| A.盛有2 mL 5%H2O2溶液的试管中滴入1 mL 0.1 mol·L-1 FeCl3溶液,试管中迅速产生大量气泡 |
B.工业上合成氨反应N2(g)+ 3H2 (g)  2NH3(g) ΔH<0 选择加热到500 ℃ 2NH3(g) ΔH<0 选择加热到500 ℃ |
C.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+ I2(g)  2HI(g) 2HI(g) |
| D.实验室可以采用排饱和食盐水收集氯气 |
您最近一年使用:0次
2022-12-03更新
|
96次组卷
|
2卷引用:甘肃省礼县第一中学2020-2021学年高一上学期期中测试化学试题
名校
解题方法
2 . 下列有关合成氨工业的说法正确的是
| A.合成氨工业的反应温度控制在400~500℃,目的是使化学平衡向正反应方向移动 |
| B.合成氨厂一般采用的压强为10MPa~30MPa,因为该压强下铁触媒的活性最高 |
| C.增大压强,正反应速率和逆反应速率均增大,但对正反应的反应速率影响更大 |
D. 的量越多, 的量越多, 的转化率越大,因此,充入的 的转化率越大,因此,充入的 越多越有利于 越多越有利于 的合成 的合成 |
您最近一年使用:0次
3 . 氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g) 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。

①图中A点时,SO2的转化率为___________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正___________ v(A)逆(填“>”“<”或 “=”)。
③图中B点的压强平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用___________ 法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为___________ 。
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:___________ 。
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为___________
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)
 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正
③图中B点的压强平衡常数Kp=
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为
您最近一年使用:0次
名校
解题方法
4 . 硫酸是一种重要的化工产品,目前的重要生产方法是“接触法”,反应原理为:2SO2+O2 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是
 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.由反应可知,2mol SO2的能量大于2mol SO3的能量 |
| D.工业在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次
2021-12-01更新
|
1074次组卷
|
7卷引用:甘肃省兰州第一中学2020-2021学年高一上学期期中考试化学试题
甘肃省兰州第一中学2020-2021学年高一上学期期中考试化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高一下学期5月期中考试化学试题四川省内江市2021-2022学年高二上学期期末检测题化学试题(已下线)6.2.2 化学反应的限度-2021-2022学年高一化学课后培优练(人教版2019必修第二册)第六章 化学反应与能量(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第六章 化学反应与能量【单元测试A卷】6.2.2 化学反应的限度 课堂例题
5 . 由H、C、N、O、S等元素形成的多种化合物在生产生活中有着重要应用。
Ⅰ.化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+ O2(g)===CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
O2(g)===CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
②CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH2=+216 kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,产生1 mol CO,转移电子的数目为__________ 。
(2)甲醇催化脱氢可制得重要的化工产品——甲醛,制备过程中能量的转化关系如图所示。
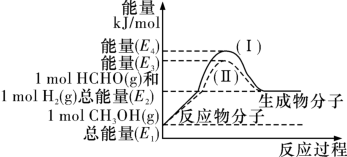
①写出上述反应的热化学方程式_______ 。
②反应热大小比较:过程Ⅰ______ (填“大于”“小于”或“等于”)过程Ⅱ。
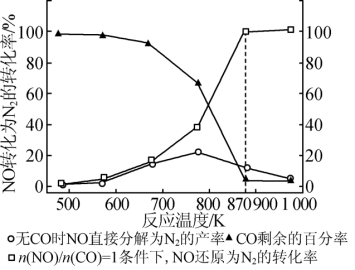
Ⅱ.(3)汽车使用乙醇汽油并不能减少NOx的排放,这使得NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以AgZSM5为催化剂,则得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775 K,发现NO的分解率降低。其可能的原因为_______ ,在n(NO)/n(CO)=1的条件下,为更好地除去NOx物质,应控制的最佳温度在_______ K左右。
Ⅲ.研究表明,在催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
反应Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1;
CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1;
反应Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1,
CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1,
(4)T1时,将1.00 mol CO2和3.00 mol H2充入体积为1.00 L的恒容密闭容器中发生反应Ⅰ,容器起始压强为p0。
①充分反应达到平衡后,若CO2的转化率为a,则容器的压强与起始压强之比为_______ (用含a的代数式表示)。
②若经过3h反应达到平衡,平衡后,混合气体的物质的量为3.00 mol,则该过程中H2的平均反应速率为___________ ;平衡常数K可用反应体系中气体物质分压表示,即用平衡分压代替平衡浓度,分压=总压×物质的量分数。则上述反应的平衡常数Kp=______ (用含p0的代数式表示)。
Ⅰ.化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+
 O2(g)===CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
O2(g)===CO(g)+2H2(g) ΔH1=-36 kJ·mol-1②CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH2=+216 kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,产生1 mol CO,转移电子的数目为
(2)甲醇催化脱氢可制得重要的化工产品——甲醛,制备过程中能量的转化关系如图所示。

①写出上述反应的热化学方程式
②反应热大小比较:过程Ⅰ
Ⅱ.(3)汽车使用乙醇汽油并不能减少NOx的排放,这使得NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以AgZSM5为催化剂,则得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775 K,发现NO的分解率降低。其可能的原因为

Ⅲ.研究表明,在催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
反应Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1;
CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1;反应Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1,
CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1,(4)T1时,将1.00 mol CO2和3.00 mol H2充入体积为1.00 L的恒容密闭容器中发生反应Ⅰ,容器起始压强为p0。
①充分反应达到平衡后,若CO2的转化率为a,则容器的压强与起始压强之比为
②若经过3h反应达到平衡,平衡后,混合气体的物质的量为3.00 mol,则该过程中H2的平均反应速率为
您最近一年使用:0次
2020-11-26更新
|
117次组卷
|
2卷引用:甘肃省庆阳市等3地2022-2023学年高二上学期12月期中化学试题
名校
解题方法
6 . 关于合成氨工业的下列说法正确的是( )
| A.从合成塔出来的气体,其中氨气一般占15%,所以生产氨的工业效率都很低 |
B.由于 易液化, 易液化, 、 、 可循环使用,则总的说来,氨的产率很高 可循环使用,则总的说来,氨的产率很高 |
| C.合成氨工业的反应温度控制在400~500℃左右,目的是使平衡向正反应方向进行 |
D.合成氨工业采用 ,是因为该条件下催化剂的活性最好 ,是因为该条件下催化剂的活性最好 |
您最近一年使用:0次
2020-09-20更新
|
880次组卷
|
8卷引用:甘肃省兰州第一中学2022-2023学年高二上学期期中考试化学试题
甘肃省兰州第一中学2022-2023学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控(已下线)第六章 化学反应与能量(培优提升卷)-2020-2021学年高一化学章末集训必刷卷(人教版2019必修第二册)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)河南省通许县一中2022—2023年高二上学期第一次月考化学试题(已下线)课时5化学反应条件的控制第4节 化学反应条件的优化——工业合成氨
7 . 在加热、催化剤作用下2SO2(g)+O2(g) 2SO3(g)下列说法不正确的是( )
2SO3(g)下列说法不正确的是( )
 2SO3(g)下列说法不正确的是( )
2SO3(g)下列说法不正确的是( )| A.在相同条件下,该反应中分别用SO2和O2表示的v,数值不同,但该反应的快慢程度是一致的 |
| B.该反应加入催化剂的目的是为了加快反应速率 |
| C.为了提高SO2的转化率,减少污染物的排放,常常在实际生产中,O2和SO2的投入量之比大于1:2 |
| D.在密闭容器中,投入2 mol SO2和l mol O2,反应结束时生成的2 mol SO3 |
您最近一年使用:0次
8 . 在下列平衡 (黄色)
(黄色) (橙红色)
(橙红色) 中,溶液介于黄和橙红色之间,现欲增加溶液的橙红色,则要在溶液中加入
中,溶液介于黄和橙红色之间,现欲增加溶液的橙红色,则要在溶液中加入
 (黄色)
(黄色) (橙红色)
(橙红色) 中,溶液介于黄和橙红色之间,现欲增加溶液的橙红色,则要在溶液中加入
中,溶液介于黄和橙红色之间,现欲增加溶液的橙红色,则要在溶液中加入A. | B. | C. | D. |
您最近一年使用:0次
2019-01-16更新
|
303次组卷
|
17卷引用:甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(B卷)试题
甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(B卷)试题甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(A卷)试题(已下线)2011-2012年广东省广雅中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年河北省涿州二中高二上学期期中考试化学试卷(已下线)2011-2012学年江西省兴国县将军中学高二上学期期中考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷2014-2015学年广东省深圳市明珠学校高二上学期期中化学试卷天津市红桥区2017-2018学年高二上学期期中考试化学试题甘肃省武威第五中学2018-2019学年高二上学期期末考试化学试题甘肃省靖远四中2018-2019学年高二第二学期开学检测化学试题2015-2016学年河北省唐山市高二上学期期末考试化学试卷广东省阳东广雅学校2017-2018学年高二10月月考化学试题天津市红桥区2020 届高三期末质量检测化学试题福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题福建省莆田第十五中学2018-2019学年高二上学期期末考试化学试题天津市红桥区2019-2020学年高三上学期期末考试化学试题安徽省太和县第八中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
9 . 碳、氮及其化合物是同学们经常能接触到的重要物质,是科学研究的重要对象。
(1)H2NCOONH4是工业合成尿素的中间产物,该反应的能量变化如图甲所示。用CO2和氨气合成尿素的热化学方程式为________________________________________ 。

(2)合理利用CO2、CH4,抑制温室效应成为科学研究的新热点。一种以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸(ΔH<0)。在不同温度下催化剂的催化效率与乙酸的生成速率分别如图乙所示。250~300 ℃时,温度升高而乙酸的生成速率降低的原因是________________ 。250 ℃和400 ℃时乙酸的生成速率几乎相等,实际生产中应选择的温度为________ ℃。
(3)T ℃时,将等物质的量的NO和CO充入体积为2 L的密闭容器中发生反应2NO+2CO 2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图丙所示。
2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图丙所示。

①平衡时若保持温度不变,再向容器中充入CO、N2各0.8 mol,平衡将________ (填“向左”“向右”或“不”)移动。
②图中a、b分别表示在一定温度下,使用相同质量、不同表面积的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是________ (填“a”或“b”)。
③15 min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是________ (任答一条即可)。
(1)H2NCOONH4是工业合成尿素的中间产物,该反应的能量变化如图甲所示。用CO2和氨气合成尿素的热化学方程式为

(2)合理利用CO2、CH4,抑制温室效应成为科学研究的新热点。一种以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸(ΔH<0)。在不同温度下催化剂的催化效率与乙酸的生成速率分别如图乙所示。250~300 ℃时,温度升高而乙酸的生成速率降低的原因是
(3)T ℃时,将等物质的量的NO和CO充入体积为2 L的密闭容器中发生反应2NO+2CO
 2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图丙所示。
2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图丙所示。
①平衡时若保持温度不变,再向容器中充入CO、N2各0.8 mol,平衡将
②图中a、b分别表示在一定温度下,使用相同质量、不同表面积的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是
③15 min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是
您最近一年使用:0次
名校
10 . 一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应X(g) Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
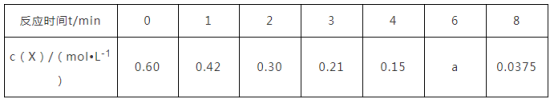
(1)0~3 min用Z表示的平均反应速率v(Z)=____ 。
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是_____________ 。由此规律推出反应在6 min时反应物的浓度a为____ mol·L-1。
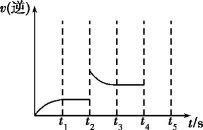
(3)反应的逆反应速率随时间变化的关系如图所示,t2时改变的条件可是______ 、_____ 。
 Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
(1)0~3 min用Z表示的平均反应速率v(Z)=
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是
(3)反应的逆反应速率随时间变化的关系如图所示,t2时改变的条件可是
您最近一年使用:0次



