名校
解题方法
1 . 将 作为弱氧化剂用于乙烷脱氢制备乙烯,具有避免乙烷深度氧化、
作为弱氧化剂用于乙烷脱氢制备乙烯,具有避免乙烷深度氧化、 资源化利用等显著优势。
资源化利用等显著优势。
(1)①查阅资料,计算 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热
i.查阅______ 的燃烧热数据(填化学式)。
ii.查阅水的汽化热:
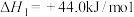 。
。
利用上述数据,得如下热化学方程式:
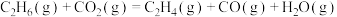
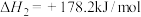
②检验产物有乙烯生成的操作和现象______ 。
(2)结合键能数据分析 氧化
氧化 脱氢反应的挑战和难点
脱氢反应的挑战和难点______ 。
(3)推测 催化
催化 氧化
氧化 脱氢反应过程示意图如下,补全示意图中画框部分(示意图中未使用键线式)。
脱氢反应过程示意图如下,补全示意图中画框部分(示意图中未使用键线式)。
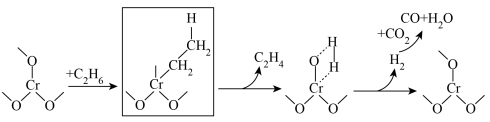
(4)分析投料体积比对反应的影响(650℃,0.1MPa,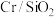 催化剂)
催化剂)
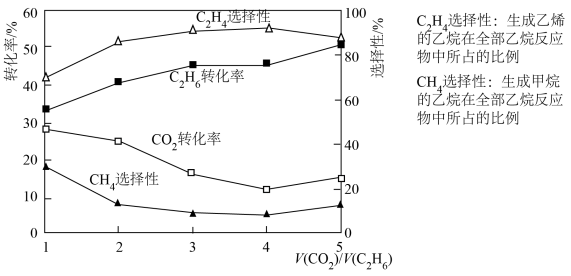
①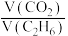 从1提高到5,
从1提高到5, 转化率从33.3%增加到50.5%,简述
转化率从33.3%增加到50.5%,简述 转化率增加的原因
转化率增加的原因______ 。(体积比为3和4时乙烷转化率基本相同)
②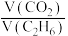 从4提高到5,副反应的化学方程式可能是
从4提高到5,副反应的化学方程式可能是______ 。
 作为弱氧化剂用于乙烷脱氢制备乙烯,具有避免乙烷深度氧化、
作为弱氧化剂用于乙烷脱氢制备乙烯,具有避免乙烷深度氧化、 资源化利用等显著优势。
资源化利用等显著优势。(1)①查阅资料,计算
 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热i.查阅
ii.查阅水的汽化热:

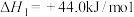 。
。利用上述数据,得如下热化学方程式:
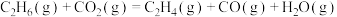
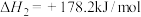
②检验产物有乙烯生成的操作和现象
(2)结合键能数据分析
 氧化
氧化 脱氢反应的挑战和难点
脱氢反应的挑战和难点键 |
|
|
|
键能 | 347.7 | 413.4 | 745 |
(3)推测
 催化
催化 氧化
氧化 脱氢反应过程示意图如下,补全示意图中画框部分(示意图中未使用键线式)。
脱氢反应过程示意图如下,补全示意图中画框部分(示意图中未使用键线式)。
(4)分析投料体积比对反应的影响(650℃,0.1MPa,
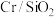 催化剂)
催化剂)
①
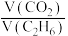 从1提高到5,
从1提高到5, 转化率从33.3%增加到50.5%,简述
转化率从33.3%增加到50.5%,简述 转化率增加的原因
转化率增加的原因②
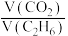 从4提高到5,副反应的化学方程式可能是
从4提高到5,副反应的化学方程式可能是
您最近一年使用:0次
2 .  资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
Ⅰ. 制甲醇,过程如下:
制甲醇,过程如下:
i.催化剂活化: (无活性)
(无活性)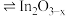 (有活性)
(有活性)
ii. 与
与 在活化后的催化剂表面可逆的发生如下反应:
在活化后的催化剂表面可逆的发生如下反应:
反应①:
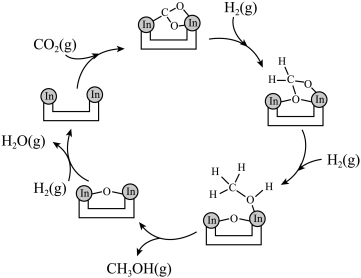
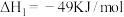 ,其反应历程如图;
,其反应历程如图;
反应②:
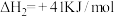 。
。
已知: 选择性
选择性 。
。
(1) 制甲醇的过程中,为同时提高
制甲醇的过程中,为同时提高 平衡转化率和
平衡转化率和 的选择性,可采取的措施为
的选择性,可采取的措施为___________ 。
(2)关于反应①历程,以下描述正确的是___________。(填序号)。
(3) 与
与 混合气体以不同流速通过反应器,气体流速与
混合气体以不同流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图:
选择性的关系如图:

①其他条件不变,气体流速较慢可造成 的积累,使催化剂失活,用化学方程式表示催化剂失活的原因:
的积累,使催化剂失活,用化学方程式表示催化剂失活的原因:___________ 。
②其他条件不变,气体流速加快, 转化率、
转化率、 选择性变化的原因是
选择性变化的原因是___________ 。
Ⅱ.一种以甲醇和二氧化碳为主要原料,利用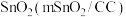 和CuO纳米片(CuONS/CF)作催化电极,电化学法制备甲酸的工作原理如图所示 (已知电解时甲醇难在电极上直接放电):
和CuO纳米片(CuONS/CF)作催化电极,电化学法制备甲酸的工作原理如图所示 (已知电解时甲醇难在电极上直接放电):
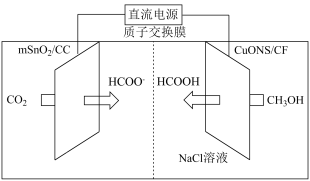
(4)①加入NaCl溶液的作用是___________ 。
②若有4mol 通过质子交换膜,将阴阳极溶液混合并酸化,理论获得HCOOH
通过质子交换膜,将阴阳极溶液混合并酸化,理论获得HCOOH___________ mol。
 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。Ⅰ.
 制甲醇,过程如下:
制甲醇,过程如下:i.催化剂活化:
 (无活性)
(无活性)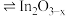 (有活性)
(有活性)ii.
 与
与 在活化后的催化剂表面可逆的发生如下反应:
在活化后的催化剂表面可逆的发生如下反应:反应①:

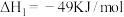 ,其反应历程如图;
,其反应历程如图;反应②:

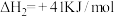 。
。已知:
 选择性
选择性 。
。
(1)
 制甲醇的过程中,为同时提高
制甲醇的过程中,为同时提高 平衡转化率和
平衡转化率和 的选择性,可采取的措施为
的选择性,可采取的措施为(2)关于反应①历程,以下描述正确的是___________。(填序号)。
| A.反应物键能之和大于生成物键能之和 |
| B.以上过程中经历了In—C、In-O键的形成和断裂 |
C. 无活性的可能原因是 无活性的可能原因是 结构中缺少氧空位 结构中缺少氧空位 |
| D.原料气中添加少量CO主要目的是为了抑制反应②进行 |
 与
与 混合气体以不同流速通过反应器,气体流速与
混合气体以不同流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图:
选择性的关系如图:
①其他条件不变,气体流速较慢可造成
 的积累,使催化剂失活,用化学方程式表示催化剂失活的原因:
的积累,使催化剂失活,用化学方程式表示催化剂失活的原因:②其他条件不变,气体流速加快,
 转化率、
转化率、 选择性变化的原因是
选择性变化的原因是Ⅱ.一种以甲醇和二氧化碳为主要原料,利用
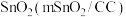 和CuO纳米片(CuONS/CF)作催化电极,电化学法制备甲酸的工作原理如图所示 (已知电解时甲醇难在电极上直接放电):
和CuO纳米片(CuONS/CF)作催化电极,电化学法制备甲酸的工作原理如图所示 (已知电解时甲醇难在电极上直接放电):
(4)①加入NaCl溶液的作用是
②若有4mol
 通过质子交换膜,将阴阳极溶液混合并酸化,理论获得HCOOH
通过质子交换膜,将阴阳极溶液混合并酸化,理论获得HCOOH
您最近一年使用:0次
解题方法
3 . 丙烯是重要的化工原料,目前生产丙烯主要有丙烷脱氢、丙烷与二氧化碳耦合等技术。
方法一:丙烷在催化剂作用下直接脱氢法制丙烯
已知:主反应 Ⅰ:C3H8(g) C3H6(g)+H2(g)ΔH1>0
C3H6(g)+H2(g)ΔH1>0
副反应 Ⅱ:C3H8(g) C2H4(g)+CH4(g)
C2H4(g)+CH4(g)
(1)反应Ⅰ自发进行的条件___________ 。
(2)一定温度下,向1L恒容密闭容器中通入0.6mol C3H8,压强为0.75MPa,反应后测得各组分的平衡压强(即组分的物质的量分数×总压)为:p(C3H8)=0.5MPa、p(CH4)=0.075MPa,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数Kc的数值为___________ 。
(3)下列说法正确的是___________
方法二:丙烷与二氧化碳耦合法制丙烯
(4)以In/Zn作为催化剂,丙烷与二氧化碳可通过耦合法制丙烯,主要发生如下反应:
Ⅰ:C3H8(g) C3H6(g)+H2(g)
C3H6(g)+H2(g)
Ⅱ:C3H8(g) C2H4(g)+CH4(g)
C2H4(g)+CH4(g)
Ⅲ:CO2(g)+9H2(g) C3H6(g)+6H2O(g)
C3H6(g)+6H2O(g)
Ⅳ:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
在580℃时,将C3H8和CO2按体积比1:1充入一恒压密闭容器中进行反应,实验测得体系中C3H8(g)、CO2(g)的转化率和C3H6(g)的选择性随催化剂组成变化如图甲,体系中C3H8(g)、CO2(g)的平衡转化率和C3H6(g)的平衡产率随压强变化如图乙。
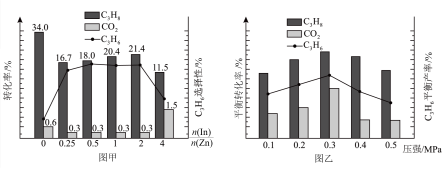
已知:C3H6(g)的选择性越高,副产物的含量越低。
耦合法制丙烯适宜选择的生产条件为___________ ,随压强增大C3H6(g)的平衡产率先增大后减小的原因为___________ 。
方法一:丙烷在催化剂作用下直接脱氢法制丙烯
已知:主反应 Ⅰ:C3H8(g)
 C3H6(g)+H2(g)ΔH1>0
C3H6(g)+H2(g)ΔH1>0副反应 Ⅱ:C3H8(g)
 C2H4(g)+CH4(g)
C2H4(g)+CH4(g)(1)反应Ⅰ自发进行的条件
(2)一定温度下,向1L恒容密闭容器中通入0.6mol C3H8,压强为0.75MPa,反应后测得各组分的平衡压强(即组分的物质的量分数×总压)为:p(C3H8)=0.5MPa、p(CH4)=0.075MPa,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数Kc的数值为
(3)下列说法正确的是___________
| A.通过充入惰性气体增大压强,不改变反应Ⅰ的反应速率 |
| B.恒温恒压条件下,ΔH1保持不变,说明反应Ⅰ达到平衡状态 |
| C.若只发生反应Ⅰ,恒压条件下,向原料气中掺入水蒸气,可增大反应的平衡常数,提高丙烯的产率 |
| D.已知高温条件下,C-C键比C-H键更易断裂,则制备丙烯应选择较低温度下的高效催化剂 |
方法二:丙烷与二氧化碳耦合法制丙烯
(4)以In/Zn作为催化剂,丙烷与二氧化碳可通过耦合法制丙烯,主要发生如下反应:
Ⅰ:C3H8(g)
 C3H6(g)+H2(g)
C3H6(g)+H2(g) Ⅱ:C3H8(g)
 C2H4(g)+CH4(g)
C2H4(g)+CH4(g)Ⅲ:CO2(g)+9H2(g)
 C3H6(g)+6H2O(g)
C3H6(g)+6H2O(g) Ⅳ:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)在580℃时,将C3H8和CO2按体积比1:1充入一恒压密闭容器中进行反应,实验测得体系中C3H8(g)、CO2(g)的转化率和C3H6(g)的选择性随催化剂组成变化如图甲,体系中C3H8(g)、CO2(g)的平衡转化率和C3H6(g)的平衡产率随压强变化如图乙。

已知:C3H6(g)的选择性越高,副产物的含量越低。
耦合法制丙烯适宜选择的生产条件为
您最近一年使用:0次
名校
解题方法
4 . 五氧化二钒(V2O5)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备V2O5的一种流程如下:
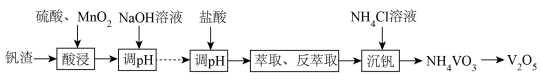
已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
(1)“酸浸”时,MnO2将VO+转化为 的离子反应方程式为
的离子反应方程式为___________ 。
(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知 能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为: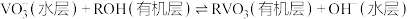 。
。
①萃取前,加盐酸调节溶液的pH为7的目的是___________ 。
②反萃取中, 反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
反萃取率随着pH的升高呈现先增大后减小的趋势的原因是___________ 。
(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是___________ 。
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知: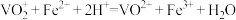 ;
;
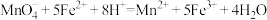 。
。
计算V2O5样品的纯度(写出计算过程)。___________ 。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:___________ 。


已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
| pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 主要存在形式 |  | V2O5 | 多钒酸根 |  | 多钒酸根 |  |
| 备注 | 多钒酸盐在水中溶解度较小 | |||||
 的离子反应方程式为
的离子反应方程式为(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知
 能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为: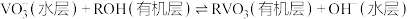 。
。①萃取前,加盐酸调节溶液的pH为7的目的是
②反萃取中,
 反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
反萃取率随着pH的升高呈现先增大后减小的趋势的原因是(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知:
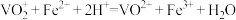 ;
;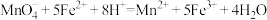 。
。计算V2O5样品的纯度(写出计算过程)。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:

您最近一年使用:0次
2023-09-09更新
|
473次组卷
|
2卷引用:江苏省苏州市2023-2024学年高三上学期期初调研测试化学试题
解题方法
5 . 以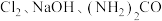 (尿素)和
(尿素)和 为原料可制备
为原料可制备 (水合肼)和无水
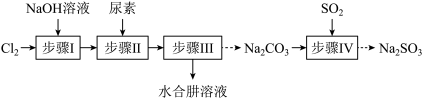
(水合肼)和无水 ,其主要实验流程如下:
,其主要实验流程如下:
已知:①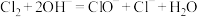 是放热反应。
是放热反应。
② 沸点约118℃,具有强还原性,高温易分解,能与
沸点约118℃,具有强还原性,高温易分解,能与 溶液剧烈反应。
溶液剧烈反应。
(1)步骤I制备 溶液时,若温度超过40℃,
溶液时,若温度超过40℃, 与
与 溶液反应生成
溶液反应生成 和
和 ,其离子方程式为
,其离子方程式为___________ ;实验中为防止温度过高,可采取的措施是___________ (任填一项)。
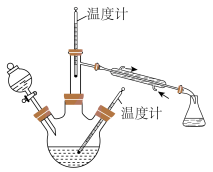
(2)步骤II合成 的装置如图所示。控制反应温度。将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集
的装置如图所示。控制反应温度。将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集 馏分。分液漏斗中的溶液是
馏分。分液漏斗中的溶液是___________ (填标号)。
A. 溶液 B.
溶液 B. 和
和 混合溶液
混合溶液
选择该项的理由是___________ 。蒸馏时需要减压,原因是___________ 。
(3)步骤IV用步骤III得到的副产品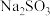 制备无水
制备无水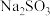 (水溶液中
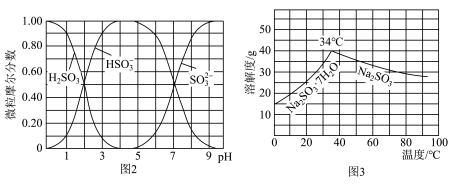
(水溶液中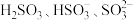 随
随 的分布如图2所示,
的分布如图2所示,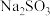 的溶解度曲线如图3所示)。
的溶解度曲线如图3所示)。
①边搅拌边向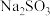 溶液中通入
溶液中通入 制备
制备 溶液。实验中确定停止通
溶液。实验中确定停止通 的操作为
的操作为___________ 。
②请补充完整由 溶液制备无水
溶液制备无水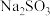 的实验方案:
的实验方案:___________ ,干燥,密封包装。
(实验中须使用的试剂: 、无水乙醇)
、无水乙醇)
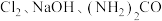 (尿素)和
(尿素)和 为原料可制备
为原料可制备 (水合肼)和无水
(水合肼)和无水 ,其主要实验流程如下:
,其主要实验流程如下:
已知:①
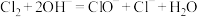 是放热反应。
是放热反应。②
 沸点约118℃,具有强还原性,高温易分解,能与
沸点约118℃,具有强还原性,高温易分解,能与 溶液剧烈反应。
溶液剧烈反应。(1)步骤I制备
 溶液时,若温度超过40℃,
溶液时,若温度超过40℃, 与
与 溶液反应生成
溶液反应生成 和
和 ,其离子方程式为
,其离子方程式为(2)步骤II合成
 的装置如图所示。控制反应温度。将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集
的装置如图所示。控制反应温度。将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集 馏分。分液漏斗中的溶液是
馏分。分液漏斗中的溶液是A.
 溶液 B.
溶液 B. 和
和 混合溶液
混合溶液选择该项的理由是

(3)步骤IV用步骤III得到的副产品
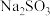 制备无水
制备无水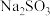 (水溶液中
(水溶液中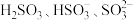 随
随 的分布如图2所示,
的分布如图2所示,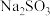 的溶解度曲线如图3所示)。
的溶解度曲线如图3所示)。
①边搅拌边向
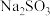 溶液中通入
溶液中通入 制备
制备 溶液。实验中确定停止通
溶液。实验中确定停止通 的操作为
的操作为②请补充完整由
 溶液制备无水
溶液制备无水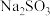 的实验方案:
的实验方案:(实验中须使用的试剂:
 、无水乙醇)
、无水乙醇)
您最近一年使用:0次
名校
解题方法
6 . 工业生产无铁硫酸铝,以硫酸浸取铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)得含铁(Fe3+)的硫酸铝溶液,加热到一定温度,搅拌,加入一定量高锰酸钾溶液和硫酸锰溶液,在溶液中生成活性二氧化锰,调节溶液的pH,反应一段时间,二氧化锰和Fe(OH)3发生吸附共沉作用,最终得到无铁硫酸铝产品。
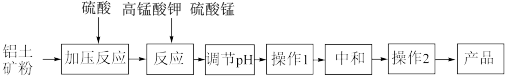
(1)硫酸浸取铝土矿时主要反应的离子方程式为___________ 。
(2)完成高锰酸钾溶液和硫酸锰溶液反应的化学方程式:KMnO4+MnSO4+H2O=___________ 。
(3)调节pH的作用是___________ 。
(4)操作1的名称为___________ ,实验室进行操作2用到的陶瓷质 仪器有___________ 。
(5)下列有关工艺的说法正确的是___________(填字母)。
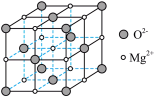
(6)氧化镁熔沸点高,可制造耐火、耐高温器材,其晶胞结构如图所示。该晶体中每个 周围与它最近且距离相等的
周围与它最近且距离相等的 数为
数为___________ ;若该立方晶胞参数为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
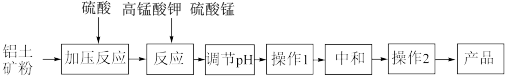
(1)硫酸浸取铝土矿时主要反应的离子方程式为
(2)完成高锰酸钾溶液和硫酸锰溶液反应的化学方程式:KMnO4+MnSO4+H2O=
(3)调节pH的作用是
(4)操作1的名称为
(5)下列有关工艺的说法正确的是___________(填字母)。
| A.可以向溶液中再加入铝土矿粉等调节pH |
| B.溶液的碱性越强,则除铁效果越好,而且不会影响硫酸铝的产率 |
| C.活性二氧化锰生成量应适宜,不足时铁的去除率较低,过量时会增加成本 |
| D.可以直接向溶液中加入二氧化锰粉末以除去Fe(OH)3 |
(6)氧化镁熔沸点高,可制造耐火、耐高温器材,其晶胞结构如图所示。该晶体中每个
 周围与它最近且距离相等的
周围与它最近且距离相等的 数为
数为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
7 . 以煤为原料,经由甲醇可制取甲醚,也可以制取烯烃并可以此取代传统的以石油为原料制取烯烃的路线。
(1)已知:在25℃和101kPa条件下,甲醇的燃烧热为-726.5 ,乙烯的燃烧热为-1411
,乙烯的燃烧热为-1411  ,
,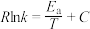 (
( 为活化能,R、C为常数,k为平衡常数)。则:
为活化能,R、C为常数,k为平衡常数)。则:
① 脱水生成
脱水生成 的热化学方程式是
的热化学方程式是___________ ,该反应自发进行的条件是___________ (填“较低”、“较高”或“任意”)温度。
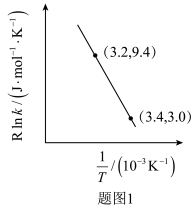
②甲醇脱水生成乙烯的温度与平衡常数的实验数据图如图1所示,该反应的正反应的活化能为___________  。
。
(2)以煤为原料气化产生的原料气可以用来合成 和
和 ,合成气平衡转化率随氢碳比 (
,合成气平衡转化率随氢碳比 (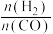 )的变化如图2所示:甲醇制取烃的过程中,会发生多种反应,可以生成
)的变化如图2所示:甲醇制取烃的过程中,会发生多种反应,可以生成 、
、 、
、 等,一定条件下,测得各烃的质量分数、
等,一定条件下,测得各烃的质量分数、 转化率随温度变化情况如图3所示。
转化率随温度变化情况如图3所示。
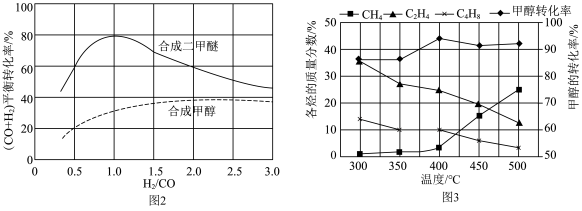
①下列叙述不正确 的是___________ 。
A.合成 的最佳氢碳比为1.0
的最佳氢碳比为1.0
B.甲醇制取烃的过程中,相同条件下,温度越高越有利于 的生成
的生成
C.甲醇制取乙烯的过程中,一般控制在350℃~400℃比较合适
D.甲醇制取烃的过程中, 的平衡转化率随温度升高先增大后减少
的平衡转化率随温度升高先增大后减少
②原料气合成 、
、 过程有如下反应发生:
过程有如下反应发生:
反应Ⅰ
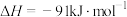
反应Ⅱ

反应Ⅲ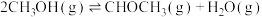

图2中原料气合成 的转化率高于
的转化率高于 的原因
的原因___________ 。
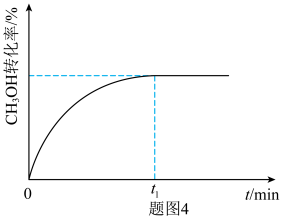
③在350℃,1MPa下,甲醇制取乙烯的转化率随时间的变化曲线如图4所示( 为该条件下的平衡时刻)。画出在相同条件下,向容器中添加氮气作稀释剂时甲醇的转化率随时间的变化曲线。
为该条件下的平衡时刻)。画出在相同条件下,向容器中添加氮气作稀释剂时甲醇的转化率随时间的变化曲线。_________
(1)已知:在25℃和101kPa条件下,甲醇的燃烧热为-726.5
 ,乙烯的燃烧热为-1411
,乙烯的燃烧热为-1411  ,
,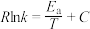 (
( 为活化能,R、C为常数,k为平衡常数)。则:
为活化能,R、C为常数,k为平衡常数)。则:①
 脱水生成
脱水生成 的热化学方程式是
的热化学方程式是②甲醇脱水生成乙烯的温度与平衡常数的实验数据图如图1所示,该反应的正反应的活化能为
 。
。
(2)以煤为原料气化产生的原料气可以用来合成
 和
和 ,合成气平衡转化率随氢碳比 (
,合成气平衡转化率随氢碳比 (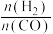 )的变化如图2所示:甲醇制取烃的过程中,会发生多种反应,可以生成
)的变化如图2所示:甲醇制取烃的过程中,会发生多种反应,可以生成 、
、 、
、 等,一定条件下,测得各烃的质量分数、
等,一定条件下,测得各烃的质量分数、 转化率随温度变化情况如图3所示。
转化率随温度变化情况如图3所示。
①下列叙述
A.合成
 的最佳氢碳比为1.0
的最佳氢碳比为1.0B.甲醇制取烃的过程中,相同条件下,温度越高越有利于
 的生成
的生成C.甲醇制取乙烯的过程中,一般控制在350℃~400℃比较合适
D.甲醇制取烃的过程中,
 的平衡转化率随温度升高先增大后减少
的平衡转化率随温度升高先增大后减少②原料气合成
 、
、 过程有如下反应发生:
过程有如下反应发生:反应Ⅰ

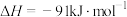
反应Ⅱ


反应Ⅲ
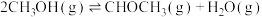

图2中原料气合成
 的转化率高于
的转化率高于 的原因
的原因③在350℃,1MPa下,甲醇制取乙烯的转化率随时间的变化曲线如图4所示(
 为该条件下的平衡时刻)。画出在相同条件下,向容器中添加氮气作稀释剂时甲醇的转化率随时间的变化曲线。
为该条件下的平衡时刻)。画出在相同条件下,向容器中添加氮气作稀释剂时甲醇的转化率随时间的变化曲线。
您最近一年使用:0次
名校
解题方法
8 . 有催化剂的条件下,将 和
和 混合加热可制备
混合加热可制备 。主要的反应有:
。主要的反应有:
Ⅰ.
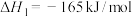
Ⅱ.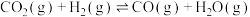

Ⅲ.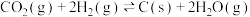
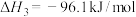
(1) 、
、 、
、 的沸点由高到低的顺序是
的沸点由高到低的顺序是__________ 。
(2)由燃烧热求 。已知
。已知 (g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
(g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
①要计算 至少还需要一个过程的热效应(该热效应记为
至少还需要一个过程的热效应(该热效应记为 ),则此过程的热化学方程式是
),则此过程的热化学方程式是___________ 。
②
____________ (用含有 的代数式表示)。
的代数式表示)。
(3) 的电子式是
的电子式是__________ ,其中C=O键的键能是799kJ/mol, 中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差
中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差__________ kJ/mol。
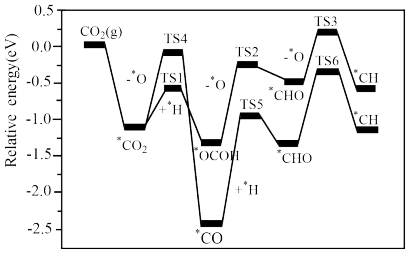
(4) 甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是___________________ 。
(5)将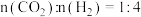 混合气持续以一定的流速通过含催化剂的恒容反应器,测定
混合气持续以一定的流速通过含催化剂的恒容反应器,测定 的转化率和
的转化率和 的选择性随温度的变化关系如图所示。温度高于500℃后,
的选择性随温度的变化关系如图所示。温度高于500℃后, 的转化率几乎保持不变但
的转化率几乎保持不变但 的选择性下降的可能原因是
的选择性下降的可能原因是________________________ 。

(6)不同压强下,保持相同的投料比,测定反应体系中 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。
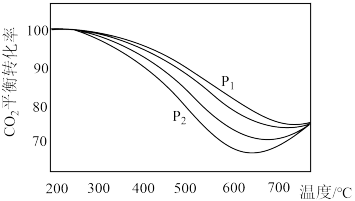
 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的,原因是
时的,原因是___________________________ 。
 和
和 混合加热可制备
混合加热可制备 。主要的反应有:
。主要的反应有:Ⅰ.

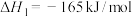
Ⅱ.
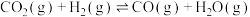

Ⅲ.
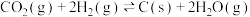
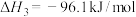
(1)
 、
、 、
、 的沸点由高到低的顺序是
的沸点由高到低的顺序是(2)由燃烧热求
 。已知
。已知 (g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
(g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。①要计算
 至少还需要一个过程的热效应(该热效应记为
至少还需要一个过程的热效应(该热效应记为 ),则此过程的热化学方程式是
),则此过程的热化学方程式是②

 的代数式表示)。
的代数式表示)。(3)
 的电子式是
的电子式是 中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差
中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差(4)
 甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
(5)将
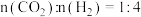 混合气持续以一定的流速通过含催化剂的恒容反应器,测定
混合气持续以一定的流速通过含催化剂的恒容反应器,测定 的转化率和
的转化率和 的选择性随温度的变化关系如图所示。温度高于500℃后,
的选择性随温度的变化关系如图所示。温度高于500℃后, 的转化率几乎保持不变但
的转化率几乎保持不变但 的选择性下降的可能原因是
的选择性下降的可能原因是
(6)不同压强下,保持相同的投料比,测定反应体系中
 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。
 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的,原因是
时的,原因是
您最近一年使用:0次
解题方法
9 . 某小组设计制备补铁剂甘氨酸亚铁的实验步骤和装置图(夹持装置省略)如图:
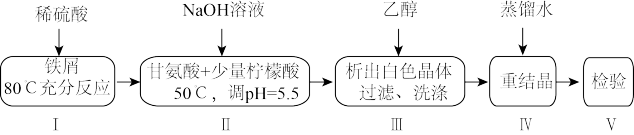
合成反应为:2H2NCH2COOH+FeSO4+2NaOH=(H2NCH2COO)2Fe+Na2SO4+2H2O。
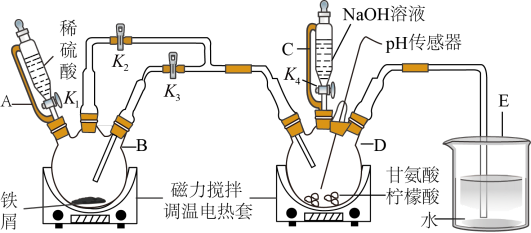
有关物质性质如表所示:
回答下列问题:
(1)步骤I制备FeSO4,先打开K1、K2,关闭K3,充分反应后(仍有气泡),将B中溶液转移到D中的操作是______ 。
(2)步骤I、II中,为了防止Fe2+被氧化,采取的措施有______ 、______ (填2种)。
(3)步骤II,D中反应液pH过高或过低均会导致产率降低,原因是______ 。
(4)下列说法不正确 的是______ 。
(5)步骤V,检测产品中铁元素的含量,需要用到如图电子天平,以差量法 准确称量样品。操作的正确排序为:电子天平开机预热→A→B→______→______→______→______→F。______

A.调水平(使水平仪气泡归中)
B.利用标准码进行校准
C.往称量瓶中加入一定量样品,放回秤盘
D.将称量瓶置于秤盘中间,待示数不变时,按TAR键去皮
E.从称量瓶中倒出一定量样品,放回秤盘
F.关闭侧门,待示数不变时读数记录

合成反应为:2H2NCH2COOH+FeSO4+2NaOH=(H2NCH2COO)2Fe+Na2SO4+2H2O。
有关物质性质如表所示:
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,微溶于乙醇 |
| 具有两性 | 酸性和还原性 | 常温不易,氧化变质 |

回答下列问题:
(1)步骤I制备FeSO4,先打开K1、K2,关闭K3,充分反应后(仍有气泡),将B中溶液转移到D中的操作是
(2)步骤I、II中,为了防止Fe2+被氧化,采取的措施有
(3)步骤II,D中反应液pH过高或过低均会导致产率降低,原因是
(4)下列说法
| A.步骤I、II使用滴液漏斗A或C滴入液体时,无需取下上口玻璃塞 |
| B.步骤III加入乙醇的作用是降低甘氨酸亚铁的溶解度,促使其结晶析出 |
| C.步骤III过滤后洗涤,往漏斗中加水浸没沉淀,小心搅拌以加快过滤 |
| D.步骤IV重结晶,将粗产品溶解于适量水中,蒸发浓缩至出现大量晶体,趁热过滤 |

A.调水平(使水平仪气泡归中)
B.利用标准码进行校准
C.往称量瓶中加入一定量样品,放回秤盘
D.将称量瓶置于秤盘中间,待示数不变时,按TAR键去皮
E.从称量瓶中倒出一定量样品,放回秤盘
F.关闭侧门,待示数不变时读数记录
您最近一年使用:0次
名校
解题方法
10 . 以废银(主要含Ag,以及少量SiO2、α-Al2O3杂质)为原料提取高纯度银的流程如图1所示,其他条件相同,浸出率与温度、时间的关系分别如图2和图3所示:
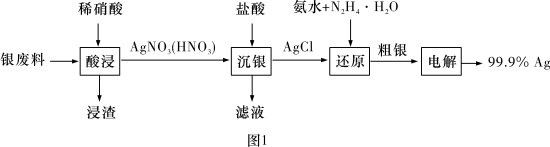
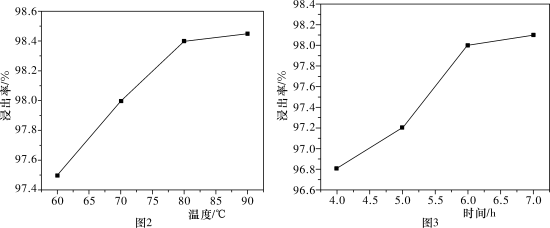
| A.最佳生产条件是温度为80℃、时间为6.0 h |
| B.浸渣的主要成分是SiO2 |
| C.“电解”中向AgNO3溶液中添加少量NaNO3能增强导电性 |
| D.理论上制备21.6 g Ag需要消耗2.5gN2H4·H2O |
您最近一年使用:0次
2023-08-16更新
|
173次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高三上学期入学考试(暑假作业检测)化学试题