1 . 在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌ N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
 N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
您最近一年使用:0次
2021-10-26更新
|
470次组卷
|
14卷引用:重庆市沙坪坝实验中学校2021-2022学年高二上学期10月月考化学试题
重庆市沙坪坝实验中学校2021-2022学年高二上学期10月月考化学试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题浙江省磐安县第二中学2021-2022学年高二10月份竞赛化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题西藏林芝市第二高级中学2021-2022学年高二上学期期中考试理综化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期第一次月考化学试题广东省广州市第二中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高二上学期第一次月考化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题河南省新教材2022-2023学年高二上学期第三次阶段性模拟测试化学试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题浙江省宁波市奉化区2023-2024学年高二上学期期末检测化学试题
名校
2 . 下列关于化学平衡的叙述,正确的是
A.2NO2(g)  N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 |
B.H2(g)+I2(g)  2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 |
C.FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 |
D.N2(g)+3H2(g)  2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 |
您最近一年使用:0次
2021-10-13更新
|
746次组卷
|
10卷引用:重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题
重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题四川省成都外国语学校2021-2022学年高二上学期10月月考化学试题2021年辽宁高考化学试题变式题11-19江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题四川省成都市第七中学2020-2021学年高二上学期十月阶段性考试化学试题安徽省池州市第一中学2020-2021学年高二上学期期中考试化学试题江西省南昌市八一中学2020-2021学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题黑龙江省牡丹江穆棱市第二中学2021-2022学年高二上学期期末考试化学试题
名校
3 . 在一定条件下,取一定量的A和B在恒容密闭容器中发生反应:aA(g)+bB(s) mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
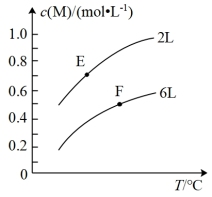
 mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
mM(g)+nN(g) △H=QkJ·mol-1,达到平衡时,M的浓度与温度和容器容积的关系如图所示。下列有关判断一定正确的是
| A.a>m+n | B.达到平衡后,增大B的量将会提高A的转化率 |
| C.E点的平衡常数小于F点的平衡常数 | D.Q>0 |
您最近一年使用:0次
2021-09-27更新
|
994次组卷
|
8卷引用:重庆市朝阳中学2021-2022学年高二12月月考化学试题
名校
4 . 已知反应X(g)+2Y(g) XY2(g) ΔH>0,下列说法错误的是
XY2(g) ΔH>0,下列说法错误的是
 XY2(g) ΔH>0,下列说法错误的是
XY2(g) ΔH>0,下列说法错误的是| A.充入X(g),平衡正向移动,X的转化率降低 |
| B.减小容器体积,正反应与逆反应速率均增大,平衡正移 |
| C.加入正催化剂,反应活化能降低,正反应与逆反应速率均增大 |
| D.升高温度,正反应速率加快,逆反应速率减缓,平衡正向移动 |
您最近一年使用:0次
2021-08-02更新
|
225次组卷
|
2卷引用:重庆市第八中学2020-2021学年高一下学期期末考试化学试题
名校
5 . 二甲醚(DME)正逐渐替代化石燃料。有多种方法制备二甲醚,回答下列问题。
(1)合成气制二甲醚:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH=-204.7 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-204.7 kJ·mol-1
①已知:H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1,H2(g)的燃烧热ΔH=-285.8 kJ·mol-1,CO(g)的燃烧热ΔH=-283.0 kJ·mol-1。则二甲醚的燃烧热ΔH=________ kJ·mol-1。
②300 ℃,1 L恒容密闭容器中充入4 mol H2和2 mol CO,测得容器内压强变化如下:
反应进行到20 min时,H2的转化率为________ ,CO的平均反应速率v(CO)=________ mol·L-1·min-1。该温度下的平衡常数K=________ (mol·L)-4。
(2)CO2催化加氢制二甲醚,可以实现CO2的再利用。该过程主要发生如下反应:
Ⅰ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.7 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.7 kJ·mol-1
Ⅱ.2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol-1
恒压条件下,CO2、H2起始量相等时,CO2的平衡转化率和CH3OCH3的选择性随温度变化如图。已知:CH3OCH3的选择性

①300 ℃时,通入CO2、H2各1 mol,平衡时CH3OCH3的选择性、CO2的平衡转化率都为30%,平衡时生成CH3OCH3的物质的量=________ mol。温度高于300 ℃,CO2的平衡转化率随温度升高而上升的原因是________ 。
②220 ℃时,CO2和H2反应一段时间后,测得A点CH3OCH3的选择性为48%,不改变反应时间和温度,一定能提高CH3OCH3的选择性的措施有________ 。
(1)合成气制二甲醚:4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) ΔH=-204.7 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-204.7 kJ·mol-1①已知:H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1,H2(g)的燃烧热ΔH=-285.8 kJ·mol-1,CO(g)的燃烧热ΔH=-283.0 kJ·mol-1。则二甲醚的燃烧热ΔH=
②300 ℃,1 L恒容密闭容器中充入4 mol H2和2 mol CO,测得容器内压强变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
(2)CO2催化加氢制二甲醚,可以实现CO2的再利用。该过程主要发生如下反应:
Ⅰ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.7 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.7 kJ·mol-1Ⅱ.2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol-1恒压条件下,CO2、H2起始量相等时,CO2的平衡转化率和CH3OCH3的选择性随温度变化如图。已知:CH3OCH3的选择性


①300 ℃时,通入CO2、H2各1 mol,平衡时CH3OCH3的选择性、CO2的平衡转化率都为30%,平衡时生成CH3OCH3的物质的量=
②220 ℃时,CO2和H2反应一段时间后,测得A点CH3OCH3的选择性为48%,不改变反应时间和温度,一定能提高CH3OCH3的选择性的措施有
您最近一年使用:0次
2021-07-20更新
|
721次组卷
|
4卷引用:重庆市第十一中学校2021届高三下学期4月二诊化学试题
重庆市第十一中学校2021届高三下学期4月二诊化学试题2021年河北省高考化学试卷变式题10-18题湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题(已下线)第12讲 化学反应的调控-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
6 . 能源开发和利用是科学研究的热点课题。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
II.2CH3OH(g) CH3OCH3(g)+H2O(g) △H2
CH3OCH3(g)+H2O(g) △H2
III.CO(g)+H2O(g) CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
则3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H=
CH3OCH3(g)+CO2(g) △H=___________ (用含△H1、△H2、△H3的代数表示)。
(2)在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
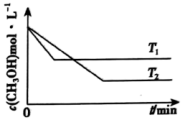
①△H___________ (填“>”“<”或“=”)0,说明理由___________ 。
②在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率___________ (填“增大”“减小”或“不变”)。
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g) CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为___________ 。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡___________ (填“向左移动”、“向右移动”或“不移动”)。
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
II.CO(g)+2H2(g) CH3OH(g) △H2=-90.4 kJ·mol-1
CH3OH(g) △H2=-90.4 kJ·mol-1
III.CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为___________ mol·L-1(用含a、b、V的代数式表示,下同),反应III的平衡常数为___________ 。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1II.2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2
CH3OCH3(g)+H2O(g) △H2III.CO(g)+H2O(g)
 CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3则3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g) △H=
CH3OCH3(g)+CO2(g) △H=(2)在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
①△H
②在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)
 CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.5 kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) △H2=-90.4 kJ·mol-1
CH3OH(g) △H2=-90.4 kJ·mol-1III.CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol,此时H2O(g)的浓度为
您最近一年使用:0次
2021-07-02更新
|
1679次组卷
|
7卷引用:重庆市缙云教育联盟2021-2022学年高三10月质量检测化学试题
重庆市缙云教育联盟2021-2022学年高三10月质量检测化学试题广西河池市九校2020-2021学年高二下学期第二次联考化学试题(已下线)第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)2.2.3 影响化学平衡的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河南宏力学校2021-2022学年高二上学期期中考试化学试题(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)浙江省杭师大附中2022-2023学年高二上学期期中考试 化学试题
名校
7 . 催化加氢生成乙烯和水是综合利用 CO2的热点研究领域。理论计算表明,在某刚性容器内,原料初始组成 n(CO2)∶n(H2)=1∶3,反应达到平衡时,四种组分的物质的量浓度 c 随温度 T 的变化如图所示。下列说法不正确的是


| A.曲线a 代表 H2 |
| B.该反应为放热反应 |
| C.E 点的正反应速率大于 F点的逆反应速率 |
D.450K 时,该反应平衡常数的数值为  |
您最近一年使用:0次
名校
8 . 在容积不变的密闭容器中,一定条件下进行如下反应:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-373.2kJ·mol-1。如图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是
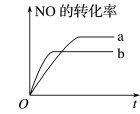
| A.降低温度 |
| B.向密闭容器中通入氩气 |
| C.加催化剂 |
| D.增大反应物中NO的浓度 |
您最近一年使用:0次
2021-03-24更新
|
268次组卷
|
9卷引用:重庆市天星桥中学2021-2022学年高二上学期第二次月考化学试题
重庆市天星桥中学2021-2022学年高二上学期第二次月考化学试题新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二上学期期末考试化学试题广西南宁市第三中学2017-2018学年高二上学期期末考试化学试题甘肃省临泽县第一中学2018-2019学年高二上学期期中考试化学试题2020届高三化学知识点强化训练—化学平衡的移动及影响因素鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时2 反应条件对化学平衡的影响章末检测卷(二)化学反应的方向、限度与速率陕西省渭南市蒲城县蒲城中学2023-2024学年高二上学期期中考试化学试题上海市进才中学2023-2024学年高一下学期期中考试化学试卷(等级)
名校
9 . NH3、NOx、SO2处理不当易造成环境污染,如果对这些气体加以利用就可以变废为宝,既减少了对环境的污染,又解决了部分能源危机问题。
(l)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l)∆H=-890.3kJ mol-1
mol-1
②N2(g)+2O2(g)=2NO2(g) ∆H=+67.7kJ mol-1
mol-1
则反应CH4(g)+2NO2(g)= CO2(g)+N2+2H2O(l)ΔH=_______ 。
(2)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g)⇌HCN(g)+3H2(g) ΔH>0
①保持其他条件一定,达到平衡时NH3转化率随X变化的关系如图1所示,X表示的外界条件可以为_______ (填字母代号)。

A.温度 B.压强 C.原料中CH4与NH3的物质的量之比
②在一定温度下,向2L恒容密闭容器中加入CH4和NH3各2mol,此时容器内压强为4×105Pa,平衡时,NH3体积分数为30%,所用时间为10min,则该时间段内用CH4的浓度变化表示的反应速率为_______ mol·L-l·min-1,该温度下平衡常数Kp=_______ Pa2(Kp是用分压来表示平衡常数,分压=总压×物质的量分数)。若保持温度不变,再向容器中加入1molH2,则再次平衡时HCN的体积分数 _______ (填“增大”、“不变”或“减小”)。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3进行电解生产硫酸,其中阴、阳膜组合电解装置如图2所示,电极材料为石墨,A-E分别代表生产中的原料或产品,a表示_______ (填“阴”或“阳”)离子交换膜。阳极的电极反应式为_______ 。

(l)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l)∆H=-890.3kJ
 mol-1
mol-1②N2(g)+2O2(g)=2NO2(g) ∆H=+67.7kJ
 mol-1
mol-1则反应CH4(g)+2NO2(g)= CO2(g)+N2+2H2O(l)ΔH=
(2)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g)⇌HCN(g)+3H2(g) ΔH>0
①保持其他条件一定,达到平衡时NH3转化率随X变化的关系如图1所示,X表示的外界条件可以为

A.温度 B.压强 C.原料中CH4与NH3的物质的量之比
②在一定温度下,向2L恒容密闭容器中加入CH4和NH3各2mol,此时容器内压强为4×105Pa,平衡时,NH3体积分数为30%,所用时间为10min,则该时间段内用CH4的浓度变化表示的反应速率为
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3进行电解生产硫酸,其中阴、阳膜组合电解装置如图2所示,电极材料为石墨,A-E分别代表生产中的原料或产品,a表示

您最近一年使用:0次
名校
解题方法
10 . 为探究Na2SO3溶液和铬(VI)盐溶液的反应规律,某同学进行实验如下:
已知: (橙色) +H2O
(橙色) +H2O
 (黄色) + 2H+
(黄色) + 2H+
(1)进行实验ⅰ和ⅱ:
①用离子方程式表示饱和Na2SO3溶液pH约为9的原因:______________________ 。
②用离子方程式解释i中现象:______________________ 。
(2)继续进行实验ⅲ:
为了说明产生上述现象的原因,补充实验ⅳ:
向2 mL蒸馏水中滴加pH=2的0.05 mol/L K2Cr2O7橙色溶液3滴,溶液变成浅橙色。
①补充实验ⅳ的目的是______________________ 。
②用化学平衡移动原理解释iii中现象:______________________ 。
③根据实验ⅰ~ⅲ,可推测:Na2SO3溶液和铬( VI)盐溶液的反应与溶液酸碱性有关。
a.碱性条件下,Na2SO3溶液和铬( VI)盐溶液不发生氧化还原反应;
b.______________________ 。
④向实验ⅲ所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是______________ 。
已知:
 (橙色) +H2O
(橙色) +H2O
 (黄色) + 2H+
(黄色) + 2H+(1)进行实验ⅰ和ⅱ:
| 序号 | 操作 | 现象 |
| ⅰ | 向2 mLpH=2的0.05 mol/LK2Cr2O7的橙色溶液中滴加饱和Na2SO3溶液(pH约为9)3滴 | 溶液变绿色(含Cr3+) |
| ⅱ | 向2 mLpH=8的0.1 mol/L的K2CrO4黄色溶液中滴加饱和Na2SO3溶液3滴 | 溶液没有明显变化 |
②用离子方程式解释i中现象:
(2)继续进行实验ⅲ:
| 序号 | 操作 | 现象 |
| ⅲ | 向2 mL饱和Na2SO3溶液中滴加pH=2的0.05 mol/LK2Cr2O7的橙色溶液3滴 | 溶液变黄色 |
向2 mL蒸馏水中滴加pH=2的0.05 mol/L K2Cr2O7橙色溶液3滴,溶液变成浅橙色。
①补充实验ⅳ的目的是
②用化学平衡移动原理解释iii中现象:
③根据实验ⅰ~ⅲ,可推测:Na2SO3溶液和铬( VI)盐溶液的反应与溶液酸碱性有关。
a.碱性条件下,Na2SO3溶液和铬( VI)盐溶液不发生氧化还原反应;
b.
④向实验ⅲ所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是
您最近一年使用:0次
2020-12-29更新
|
469次组卷
|
5卷引用:重庆市第三十二中学2020-2021学年高二上学期期末考试化学试题



