10-11高二下·浙江杭州·期中
1 . 对已经达到化学平衡的反应: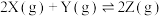 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是
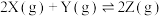 ,减小压强时,对反应产生的影响是
,减小压强时,对反应产生的影响是| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
2022-11-02更新
|
741次组卷
|
97卷引用:辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题
辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷辽宁省大连渤海高级中学2018-2019学年高二下学期期中考试化学试题黑龙江漠河市高级中学2020-2021学年高二上学期期末考试化学试题湖北省十堰市2020-2021学年高二上学期期末考试化学试题广东省惠州市2020-2021学年高二上学期期末考试化学试题广东省惠州市2020-2021学年高二上学期期末质量监测化学试题河南省开封市五县2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题2第三单元 化学平衡的移动山东省山大附中卧龙学校2021-2022学年高二上学期第一次月考化学试题甘肃省庆阳市第六中学2021-2022学年高二上学期期中考试化学(理)试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题广东省揭阳市惠来县第一中学2021-2022学年高二上学期第二次阶段考试化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高二上学期期中考试化学试题内蒙古乌兰察布市部分学校2021-2022学年高二上学期期中联考化学试题甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(B卷)试题福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题(已下线)2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷(已下线)2011-2012学年山东省鲁北中学高二上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市邹城二中高二上学期期中质量检测化学试卷(已下线)2011-2012学年云南省玉溪一中高二下学期期中考试化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年昆明三中、滇池中学(滇中)高二下期中考试化学卷(已下线)2012-2013学年江苏省南京三中高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2013-2014学年河南省漯河市高二上学期期中考试化学试卷(已下线)2014-2015学年河南周口市沈丘县县直高级中学高二上第一次月考化学(已下线)2014-2015学年山东安丘市实验中学期中考试高二化学模拟(B)卷(已下线)2014秋安徽省淮北师范大学附属实验中学高二上学期期中化学试卷2015-2016学年陕西省西安第七十中学高二上学期期中测试化学试卷2015-2016学年宁夏育才中学高二上学期期中测试化学试卷2015-2016学年青海西宁第十四中学高二上期中考试化学卷2015-2016学年陕西省澄城县寺前中学高一下学期期中考试化学试卷(已下线)同步君 人教版 选修4 第2章 第3节 化学平衡状态2016-2017学年湖北省襄阳五中高二上开学考试化学试卷2016-2017学年河北省博野中学高二上学期第二次月考化学试卷2016-2017学年宁夏育才中学高二上第一次月考化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷2016-2017学年河北省张家口万全中学高二上第一次月考化学试卷2016-2017学年湖南省浏阳市第一中学高二上阶段性测试化学试卷2016-2017学年甘肃省民乐一中高二上10月月考化学试卷2016-2017学年山东省桓台二中高二12月检测化学试卷甘肃省会宁县第四中学2017-2018学年高二上学期期中考试化学试题云南省德宏州芒市第一中学2017-2018学年高二上学期期中考试化学试题山东省济南第一中学2017-2018学年高二上学期期中考试化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第二课时(化学平衡状态)【全国省级联考】广东省蓝精灵中学2017-2018 学年度高二上学期期末联考化学试题【全国百强校】河北省石家庄市辛集中学2018-2019学年高二上学期第一次月考化学试题甘肃省岷县一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期期中考试化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题甘肃省高台县第一中学2018-2019学年高二上学期期中考试化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题甘肃省宁县二中2018-2019学年高二上学期期中考试化学试题四川省宜宾市第四中学2018-2019学年高二上学期期中考试理科综合化学试题高二人教版选修4 第二章 第三节 化学平衡河北省承德市第一中学2018-2019学年高二上学期第三次月考化学试题甘肃省镇原县孟坝中学2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区沙雅县第二中学2018-2019学年高二上学期期中考试化学试题河南省永城市实验高级中学2018-2019学年高二上学期期中考试化学试题上海市华东师范大学附属天山学校2018-2019学年高一第二学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高二10月月考化学试题湖南省永州市东安县第一中学2019-2020学年高二上学期第一次月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题甘肃省张掖市山丹县第一中学2019-2020学年上学期9月月考--高二化学江西省宜春九中(外国语学校)2019-2020学年高二上学期期中考试化学试题吉林省蛟河市朝鲜族中学校2019-2020学年高二上学期期中考试化学试题河北省石家庄市普通高中2019-2020学年高二10月月考化学(高考)试题新疆沙雅县第二中学2019-2020学年高二上学期期中考试化学试题贵州省毕节市实验高级中学2018-2019学年高二上学期期末考试化学试题湖南省邵阳市洞口县第四中学2019-2020学年高二上学期期中考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二上学期期末考试化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题黑龙江桦南二中2019-2020学年高二上学期期中考试化学试题广西桂林市第十八中学2019-2020学年高二下学期期中考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题陕西省延安市吴起高级中学2019-2020学年高一下学期第四次质量检测(期末)化学试题黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题海南省海口市第四中学2020-2021学年高二上学期第一次月考化学试题吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题新疆生产建设兵团第四师第一中学2020-2021学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素河北省唐山市河北唐山外国语学校2020-2021学年高二上学期期中考试(理科)化学试题宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试题河北省张家口宣化一中2020-2021学年高二上学期12月月考化学试题福建省莆田第十五中学2018-2019学年高二上学期期末考试化学试题华中师范大学海南附属中学2019-2020学年高二上学期第三次月考化学试题吉林长春市榆树高级中学2019-2020学年高二下学期期末考试化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题青海省西宁市大通回族土族自治县2021-2022学年高二上学期期末考试化学试题(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)湖北省随州市洛平许济四市联盟2022-2023学年高三上学期第一次质量检测化学试题湖北省黄州中学2022--2023学年高二上学期10月月考化学试题河南省灵宝市第五高级中学2021-2022学年高二下学期第一次月考化学试题广东省阳江市高新区2022-2023学年高二上学期1月期末考试化学试题作业(十二) 压强对化学平衡的影响 勒·夏特列原理
2 . 下列事实中不能用平衡移动原理解释的是
| A.合成氨使用高温条件 |
| B.往氢硫酸溶液中加入碱,有利于S2-增多 |
| C.硫化亚铁不溶于水,但是能溶于稀盐酸中 |
| D.用水洗涤硫酸钡造成的损失量大于用稀硫酸造成的损失量 |
您最近一年使用:0次
2021-12-15更新
|
529次组卷
|
3卷引用:辽宁省实验中学2021-2022学年高二上学期第二次(12月)月考化学试题
辽宁省实验中学2021-2022学年高二上学期第二次(12月)月考化学试题湖北省新高考联考协作体2021-2022学年高二3月考试化学试题(已下线)押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)
3 . 在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌ N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
 N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
您最近一年使用:0次
2021-10-26更新
|
470次组卷
|
14卷引用:辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题
辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题浙江省磐安县第二中学2021-2022学年高二10月份竞赛化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题重庆市沙坪坝实验中学校2021-2022学年高二上学期10月月考化学试题西藏林芝市第二高级中学2021-2022学年高二上学期期中考试理综化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期第一次月考化学试题广东省广州市第二中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高二上学期第一次月考化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题河南省新教材2022-2023学年高二上学期第三次阶段性模拟测试化学试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题浙江省宁波市奉化区2023-2024学年高二上学期期末检测化学试题
4 . 甲醇是一种重要的有机化工原料,可用于制取甲醚。一定温度下,在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)。
(1)容器I中的反应达到平衡时所需的时间_____ (填“大于”“小于”或等于)容器III中的。
(2)a=___________
(3)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
(4)已知下面两个反应(m、n均大于0):
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
则下列m与n的关系中,正确的是___________(填字母)。
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| II | 387 | 0.40 | a | b |
| III | 207 | 0.20 | 0.090 | 0.090 |
(1)容器I中的反应达到平衡时所需的时间
(2)a=
(3)下列说法中能说明该反应达到平衡状态的是___________。(填字母)
| A.容器中压强不变 |
| B.混合气体中c(CH3OCH3)不变 |
| C.混合气体的密度不变 |
| D.单位时间内生成1mol CH3OCH3同时消耗2mol CH3OH |
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-mkJ·mol-1
反应②:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=-nkJ·mol-1
则下列m与n的关系中,正确的是___________(填字母)。
| A.n﹥2m | B.m﹥2n | C.2m﹥n | D.m﹥3n |
您最近一年使用:0次
名校
5 . 下列关于化学平衡的叙述,正确的是
A.2NO2(g)  N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 |
B.H2(g)+I2(g)  2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 |
C.FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 |
D.N2(g)+3H2(g)  2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 |
您最近一年使用:0次
2021-10-13更新
|
746次组卷
|
10卷引用:2021年辽宁高考化学试题变式题11-19
2021年辽宁高考化学试题变式题11-19重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题四川省成都外国语学校2021-2022学年高二上学期10月月考化学试题江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题四川省成都市第七中学2020-2021学年高二上学期十月阶段性考试化学试题安徽省池州市第一中学2020-2021学年高二上学期期中考试化学试题江西省南昌市八一中学2020-2021学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题黑龙江省牡丹江穆棱市第二中学2021-2022学年高二上学期期末考试化学试题
6 . 下列实验装置设计完全正确且能达到目的的是
| A | B | C | D |
 | 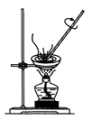 | 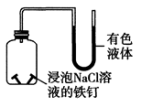 |  |
| 铁件上镀铜 | 蒸发 溶液制备 溶液制备 晶体 晶体 | 探究铁的吸氧腐蚀 | 测定 溶液生成 溶液生成 的反应速率 的反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-12更新
|
254次组卷
|
2卷引用:辽宁省铁岭市调兵山市第二高级中学2020-2021学年度高二下学期期末考试化学试题
7 . 甲醇是重要的化工原料,又可作为燃料。以CO2和H2为原料生产甲醇时,同时发生下列两个反应,反应的热化学方程式如下:
I.
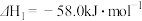
II.
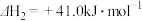
(1)上述两个反应中,在热力学上趋势较大的是____ (填反应代号)。
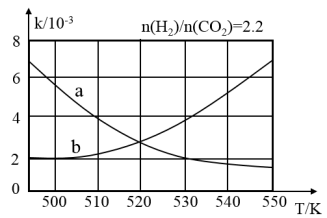
(2)下图中表示反应II平衡常数K随温度变化关系的曲线为__ (填曲线标记字母),其判断依据是___ 。
(3)CO和H2反应也可生成气态甲醇。相关的化学键键能数据如下:
①则x=______ 。
②CO和H2生成甲醇的反应,体系总压强为P MPa恒定,在温度T时,起始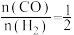 ,若到达平衡时,CO的转化率为50%,则平衡常数Kp=
,若到达平衡时,CO的转化率为50%,则平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)某实验室控制CO2和H2初始投料比为1:2.2。在相同压强下,发生I、II两个反应,经过相同反应时间测得如下实验数据如图A、图B所示:
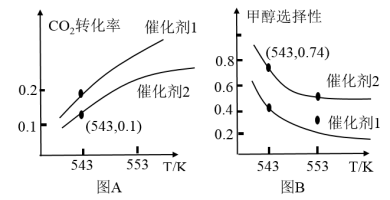
①有利于提高CO2转化为CH3OH平衡转化率的措施有_______ 。
A.使用催化剂1
B.增大CO2和H2的初始投料比
C.使用催化剂2
D.投料比不变,增加反应物的浓度
②在催化剂2的作用下,543 K时,CO的选择性(CO2转化为CO的体积百分比)为____ ,H2的转化率为____ (保留两位有效数字)。
I.

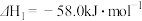
II.

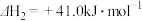
(1)上述两个反应中,在热力学上趋势较大的是
(2)下图中表示反应II平衡常数K随温度变化关系的曲线为

(3)CO和H2反应也可生成气态甲醇。相关的化学键键能数据如下:
| 化学键 |  |  |  |  |  |
 | 436 | 343 | 1076 | 465 |  |
①则x=
②CO和H2生成甲醇的反应,体系总压强为P MPa恒定,在温度T时,起始
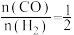 ,若到达平衡时,CO的转化率为50%,则平衡常数Kp=
,若到达平衡时,CO的转化率为50%,则平衡常数Kp=(4)某实验室控制CO2和H2初始投料比为1:2.2。在相同压强下,发生I、II两个反应,经过相同反应时间测得如下实验数据如图A、图B所示:

①有利于提高CO2转化为CH3OH平衡转化率的措施有
A.使用催化剂1
B.增大CO2和H2的初始投料比
C.使用催化剂2
D.投料比不变,增加反应物的浓度
②在催化剂2的作用下,543 K时,CO的选择性(CO2转化为CO的体积百分比)为
您最近一年使用:0次
2021-06-28更新
|
474次组卷
|
2卷引用:2021年辽宁高考化学试题变式题11-19
8 . 对于反应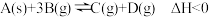 ,下列说法正确的是
,下列说法正确的是
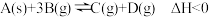 ,下列说法正确的是
,下列说法正确的是| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.该反应△S>0,△H<0,在任何条件下能自发进行 |
| C.恒温恒容条件下,混合气体密度不变达到化学平衡状态 |
| D.达到平衡状态后,若增加A的量,平衡向正反应方向移动 |
您最近一年使用:0次
2021-06-28更新
|
917次组卷
|
6卷引用:辽宁省葫芦岛市第八高级中学2021-2022学年高二上学期实验班第一次月考化学试题
辽宁省葫芦岛市第八高级中学2021-2022学年高二上学期实验班第一次月考化学试题浙江省嘉兴市2020-2021学年高二下学期期末检测化学试题(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)专题2.3 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)浙江省天台中学2021-2022学年高二上学期返校考试化学试题(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)
9 . “加大力度保护自然,实现可持续发展”是第五届联合国环境大会会议主题。工业生产产生的含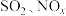 的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
(1)在一定条件下,肼( )与
)与 反应能生成
反应能生成 和
和 。
。
已知:①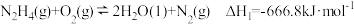 ;
;
②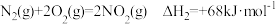 ;
;
③ ;
;
则反应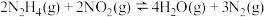 的
的
_______  。
。
(2)在一恒容密闭容器中发生反应: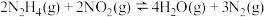 。当温度高于250℃时,正、逆反应速率分别为
。当温度高于250℃时,正、逆反应速率分别为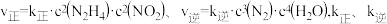 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 、
、 与该反应的平衡常数
与该反应的平衡常数 之间的关系为
之间的关系为_______ 。速率常数 随温度的升高而增大,则达到平衡后,仅升高温度,
随温度的升高而增大,则达到平衡后,仅升高温度, 增大的倍数
增大的倍数_______ (填“>”、“<”或“=”) 增大的倍数。
增大的倍数。
(3)在一定条件下,利用催化净化技术,CO可将NO2转化为无毒物质反应为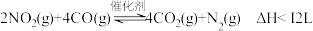 。向两个容积均为2L的恒容密闭容器中均分别充入
。向两个容积均为2L的恒容密闭容器中均分别充入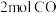 和
和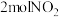 ,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为
,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为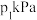 ,曲线II代表的体系平衡后气体的总压强为
,曲线II代表的体系平衡后气体的总压强为 。
。
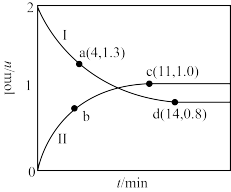
①代表220℃条件下的变化曲线为___ (填“I”或“II”);ad段 的平均反应速率为
的平均反应速率为__  。
。
②下列有关曲线II条件下的反应的说法正确的是_______ (填标号)。
A.当体系中 与
与 的物质的量之比不随时间变化时,反应达到平衡状态
的物质的量之比不随时间变化时,反应达到平衡状态
B.当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,混合气体的平均相对分子质量增大
D.使用高效催化剂可提高 的转化率
的转化率
③图中a、c、d三点对应的逆反应速率由大到小的顺序为_______ (用a、c、d表示);在曲线II代表的温度下,该反应的平衡常数Kp=_______  (Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
(Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
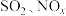 的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。(1)在一定条件下,肼(
 )与
)与 反应能生成
反应能生成 和
和 。
。已知:①
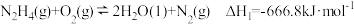 ;
;②
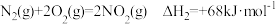 ;
;③
 ;
;则反应
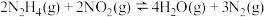 的
的
 。
。(2)在一恒容密闭容器中发生反应:
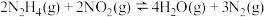 。当温度高于250℃时,正、逆反应速率分别为
。当温度高于250℃时,正、逆反应速率分别为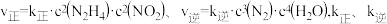 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 、
、 与该反应的平衡常数
与该反应的平衡常数 之间的关系为
之间的关系为 随温度的升高而增大,则达到平衡后,仅升高温度,
随温度的升高而增大,则达到平衡后,仅升高温度, 增大的倍数
增大的倍数 增大的倍数。
增大的倍数。(3)在一定条件下,利用催化净化技术,CO可将NO2转化为无毒物质反应为
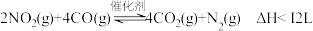 。向两个容积均为2L的恒容密闭容器中均分别充入
。向两个容积均为2L的恒容密闭容器中均分别充入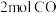 和
和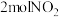 ,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为
,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为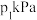 ,曲线II代表的体系平衡后气体的总压强为
,曲线II代表的体系平衡后气体的总压强为 。
。
①代表220℃条件下的变化曲线为
 的平均反应速率为
的平均反应速率为 。
。②下列有关曲线II条件下的反应的说法正确的是
A.当体系中
 与
与 的物质的量之比不随时间变化时,反应达到平衡状态
的物质的量之比不随时间变化时,反应达到平衡状态B.当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,混合气体的平均相对分子质量增大
D.使用高效催化剂可提高
 的转化率
的转化率③图中a、c、d三点对应的逆反应速率由大到小的顺序为
 (Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
(Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
2021-05-27更新
|
408次组卷
|
6卷引用:辽宁省沈阳郊联体2021届高三5月四模化学试题
10 . 氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。
(1)NO在空气中存在如下反应:2NO(g) + O2(g) ⇌2NO2(g) ∆H;该反应分两步完成,其反应历程如图所示:
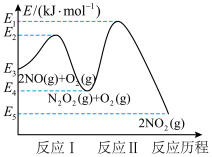
回答下列问题:
①写出反应I的热化学方程式_______ 。
②反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)⇌2NO2(g)反应速率的是_______ (填“反应I”或“反应Ⅱ”);对该反应体系升高温度,发现总反应速率反而变慢,其原因可能是_______ (反应未使用催化剂)。
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及10min和20min各物质平衡浓度如表所示:
①T℃时,该反应的平衡常数为_______ (保留两位有效数字)。
②在10min时,若只改变某一条件使平衡发生移动,20min时重新达到平衡,则改变的条件是_______ 。
(3)NO2存在如下平衡:2NO2(g)⇌N2O4(g) ∆H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=_______ ;在图中标出点中,指出能表示反应达到平衡状态的点是_______ 。

(1)NO在空气中存在如下反应:2NO(g) + O2(g) ⇌2NO2(g) ∆H;该反应分两步完成,其反应历程如图所示:

回答下列问题:
①写出反应I的热化学方程式
②反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)⇌2NO2(g)反应速率的是
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及10min和20min各物质平衡浓度如表所示:
浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.040 | 0.03 | 0.030 |
| 20 | 0.032 | 0.034 | 0.017 |
①T℃时,该反应的平衡常数为
②在10min时,若只改变某一条件使平衡发生移动,20min时重新达到平衡,则改变的条件是
(3)NO2存在如下平衡:2NO2(g)⇌N2O4(g) ∆H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。一定温度下,k1、k2与平衡常数kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=

您最近一年使用:0次



