名校
1 . 下列事实,不能用勒夏特列原理解释的是
A. 溶液中加入 溶液中加入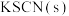 后颜色变深 后颜色变深 |
| B.开启啤酒瓶后,瓶中立刻泛起大量泡 |
C.对 ,增大平衡体系的压强(压缩体积)可使体系颜色变深 ,增大平衡体系的压强(压缩体积)可使体系颜色变深 |
D.红棕色气体 加压后颜色先变深后变浅 加压后颜色先变深后变浅 |
您最近一年使用:0次
名校
2 . 下列实验方法或方案能达到目的的是
| 目的 | 实验方法或方案 | |
| A | 探究压强对化学平衡的影响 | 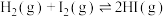  |
| B | 证明碳酸钠水解能力比碳酸氢钠强 | 分别向盛有 饱和 饱和 溶液和饱和 溶液和饱和 溶液的试管中滴加3滴酚酞溶液,观察颜色变化 溶液的试管中滴加3滴酚酞溶液,观察颜色变化 |
| C | 探究浓度对化学平衡移动的影响 | 向两支盛有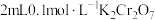 溶液的试管中分别滴入3滴浓硫酸和3滴浓 溶液的试管中分别滴入3滴浓硫酸和3滴浓 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有 溶液的试管中分别加入 溶液的试管中分别加入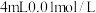 和 和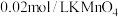 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列操作能达到相应实验目的的是

A.除去乙烯中的少量 | B.研究浓度对化学平衡的影响 |
| C.除去二氧化锰中的少量氯酸钾 | D.用氢氧化钠溶液滴定盐酸 |
您最近一年使用:0次
4 . 一定温度下,向2L恒温密闭容器中加入足量活性炭和 ,发生反应
,发生反应 ,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
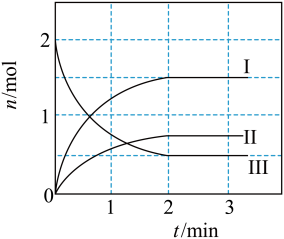
 ,发生反应
,发生反应 ,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
A.曲线I表示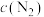 随t的变化 随t的变化 |
B.0~2min内, |
C.3min时,加入催化剂可提高 的平衡转化率 的平衡转化率 |
D.3min时,充入 增大压强,该容器的气体颜色不变 增大压强,该容器的气体颜色不变 |
您最近一年使用:0次
名校
5 . 回答下列问题:
(1)在 和
和 溶液中存在如下平衡:
溶液中存在如下平衡: (黄色)
(黄色) (无色)
(无色)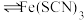 (红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和
(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和 溶液,溶液颜色变
溶液,溶液颜色变___________ (填“深”或“浅”);向另一支试管中滴加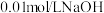 溶液,平衡向
溶液,平衡向___________ (填“正”或“逆”)方向移动。
(2)已知: (
( ,橙色)
,橙色) (
( ,黄色)
,黄色)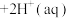
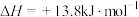 某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下:
某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下: 中颜色不变后与试管
中颜色不变后与试管 比较,溶液颜色变浅;②快速滴入浓硫酸,试管
比较,溶液颜色变浅;②快速滴入浓硫酸,试管 温度略有升高,溶液颜色与试管
温度略有升高,溶液颜色与试管 相比溶液颜色变深。下列说法正确的是___________。
相比溶液颜色变深。下列说法正确的是___________。
(3)某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如表(见表格),请结合表中信息,回答有关问题:
已知:该反应的化学方程式:
①写出上述反应的离子方程式___________ 。
②根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是___________ (填实验序号)。
③在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:1和2、1和3的组合比较,所研究的问题是___________ 。找出哪种组合是温度对化学反应速率的影响___________ 。
④教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:___________ 。
(1)在
 和
和 溶液中存在如下平衡:
溶液中存在如下平衡: (黄色)
(黄色) (无色)
(无色)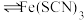 (红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和
(红色)。将上述溶液均分置于两支试管中;向其中一支试管中加入饱和 溶液,溶液颜色变
溶液,溶液颜色变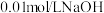 溶液,平衡向
溶液,平衡向(2)已知:
 (
( ,橙色)
,橙色) (
( ,黄色)
,黄色)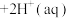
 某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下:
某同学利用以上可逆反应研究浓度对化学平衡的影响,现象如下: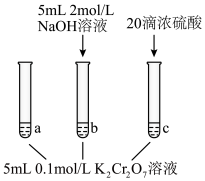
 中颜色不变后与试管
中颜色不变后与试管 比较,溶液颜色变浅;②快速滴入浓硫酸,试管
比较,溶液颜色变浅;②快速滴入浓硫酸,试管 温度略有升高,溶液颜色与试管
温度略有升高,溶液颜色与试管 相比溶液颜色变深。下列说法正确的是___________。
相比溶液颜色变深。下列说法正确的是___________。| A.该反应为氧化还原反应 |
B.待试管 中溶液颜色不变的目的是使 中溶液颜色不变的目的是使 完全反应 完全反应 |
C.试管 中的现象说明影响平衡的主要因素是温度 中的现象说明影响平衡的主要因素是温度 |
| D.该实验不能证明减小生成物浓度,平衡正向移动 |
(3)某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如表(见表格),请结合表中信息,回答有关问题:
| 实验编号 | 实验温度 | 参加反应的物质 | ||||
 |  |  | ||||
 |  |  |  |  | ||
| 1 | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| 2 | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| 3 | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| 4 | 40 | 5 | 0.1 | 10 | 0.1 | 5 |

①写出上述反应的离子方程式
②根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是
③在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:1和2、1和3的组合比较,所研究的问题是
④教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:
您最近一年使用:0次
名校
6 . 一定条件下,某容积为 的密闭容器中发生反应:
的密闭容器中发生反应: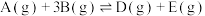
 ,反应过程中正、逆反应速率随着时间的变化如图所示,下列说法正确的是
,反应过程中正、逆反应速率随着时间的变化如图所示,下列说法正确的是
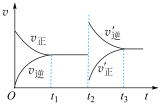
A. 时间段内, 时间段内, |
| B.若容器内气体的密度不再发生变化,则说明达到平衡状态 |
C. 时间段内平衡向正反应方向移动 时间段内平衡向正反应方向移动 |
D. 时刻改变的条件为向容器中加入生成物的同时分离出反应物 时刻改变的条件为向容器中加入生成物的同时分离出反应物 |
您最近一年使用:0次
7 . 下列叙述中,不能用勒夏特列原理解释的是
| A.用饱和食盐水洗气除去氯气中的氯化氢 |
B.将 的乙酸溶液稀释10倍后溶液 的乙酸溶液稀释10倍后溶液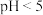 |
| C.合成氨反应常在高压条件下进行 |
D.对 平衡体系压缩容器体积后可使气体颜色变深 平衡体系压缩容器体积后可使气体颜色变深 |
您最近一年使用:0次
23-24高二上·广东深圳·期末
名校
8 . 合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
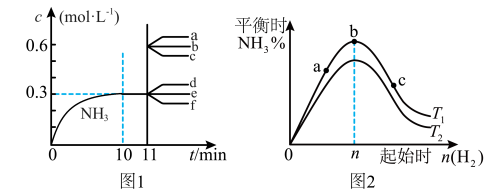
 2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
2NH3(g) ΔH<0。图1表示在2L恒容密闭容器中NH3的物质的量浓度随时间的变化曲线。图2表示在其他条件不变时,平衡时NH3的体积分数随起始时H2的物质的量的变化曲线。下列说法正确的是
| A.图1中,其他条件不变,第11min改用更为高效的催化剂,则c(NH3)-t的变化趋势为曲线b所示 |
| B.图1中,其他条件不变,第11min迅速压缩容器体积为1L,则c(NH3)-t的变化趋势为曲线a所示 |
| C.图2中,反应物N2的平衡转化率:b>a>c |
| D.图2中,T1、T2表示温度,则T1>T2 |
您最近一年使用:0次
名校
解题方法
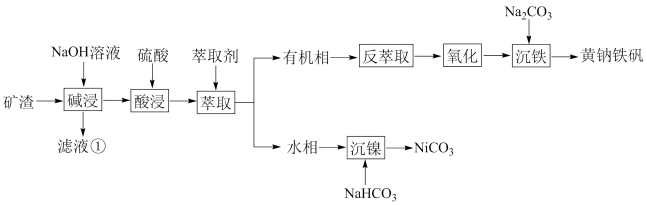
9 . 某废矿渣的主要成分有 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
已知:i.黄钠铁矾 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
ii.常温下,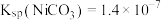 ;
;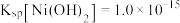 。
。
回答下列问题:
(1)滤液①中,主要存在的钠盐有_____________________ 。
(2)“萃取”可将金属离子进行富集与分离,原理如下:
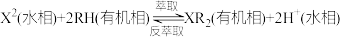 。
。
则“反萃取”应控制在____________________ (填“碱性”、“酸性”或“中性”)环境进行。
(3)“氧化”中加入 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为____________________ 。
(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为_________________________ ,“沉镍”时若溶液 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是__________________________ 。
(5)“沉铁”过程反应的离子方程式为_________________________ 。
(6)定量分析:
测定“酸漫”后的溶液中 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用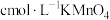 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
已知:i.黄钠铁矾
 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;ii.常温下,
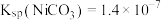 ;
;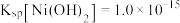 。
。回答下列问题:
(1)滤液①中,主要存在的钠盐有
(2)“萃取”可将金属离子进行富集与分离,原理如下:
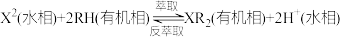 。
。则“反萃取”应控制在
(3)“氧化”中加入
 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为
 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是(5)“沉铁”过程反应的离子方程式为
(6)定量分析:
测定“酸漫”后的溶液中
 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用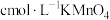 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
10 . Ⅰ.将CO2转化为CO、CH3OH等燃料,可以有效的缓解能源危机,同时可以减少温室气体,实现“双碳目标”。
800℃时,H2还原CO2反应的热化学方程式及其平衡常数如下:
ⅰ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
(1)反应CO(g)+2H2(g) CH3OH(g) ΔH3=
CH3OH(g) ΔH3=___________ kJ·mol-1,K3=___________ 。
Ⅱ.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
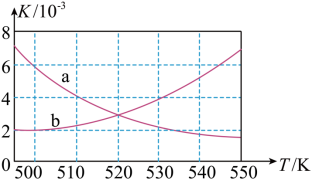
(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为___________ (填曲线标记字母),其判断理由是___________ 。
(3)在一定温度下,向2.0L固定容积的密闭容器中充入2mol H2和1mol CO,经过一段时间后,反应4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
①0~20min的平均反应速率v(CO)=___________ mol·L−1·min−1。
②达到平衡时,H2的转化率为___________ 。
③能表明该反应达到平衡状态的是___________ (填字母)。
A.容器中二甲醚的浓度不变 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
800℃时,H2还原CO2反应的热化学方程式及其平衡常数如下:
ⅰ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104ⅱ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3(1)反应CO(g)+2H2(g)
 CH3OH(g) ΔH3=
CH3OH(g) ΔH3=Ⅱ.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为

(3)在一定温度下,向2.0L固定容积的密闭容器中充入2mol H2和1mol CO,经过一段时间后,反应4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | — |
| n(CO)/mol | 1.0 | — | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | — | — | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
②达到平衡时,H2的转化率为
③能表明该反应达到平衡状态的是
A.容器中二甲醚的浓度不变 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
您最近一年使用:0次



