名校
1 . 恒容密闭容器中发生反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.室温下能自发进行,表明该反应的 |
| B.保持温度一定,充入氩气使反应速率加快 |
| C.加入合适的催化剂,既能改变反应历程又能降低活化能 |
D.其他条件一定,再通入适量 , , 和 和 的转化率都将增大 的转化率都将增大 |
您最近一年使用:0次
2024-02-29更新
|
80次组卷
|
2卷引用:四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题
名校
解题方法
2 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 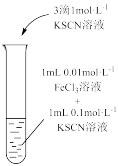 | 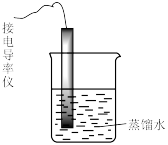 分别测定20℃和80℃蒸馏水的电导率 | 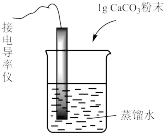 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在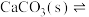  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-06更新
|
933次组卷
|
13卷引用:四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题
四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题河南省濮阳市第一高级中学2022-2023学年高二下学期期中质量检测化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷北京市第五十中学2023-2024学年高二上学期12月月考化学试题天津市部分区2023-2024学年高二上学期期末练习化学试题北京交通大学附属中学第二分校2023-2024学年高二上学期12月月考化学试题
名校
3 . 已知:[Cu(H2O)4]2+ (蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O;浓度较小时[Cu(H2O)4]2+用Cu2+表示。CuCl2溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓HCl,溶液变为黄色(溶液②)。取以上溶液进行如下实验,对实验现象分析正确的是
[CuCl4]2-(黄色)+4H2O;浓度较小时[Cu(H2O)4]2+用Cu2+表示。CuCl2溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓HCl,溶液变为黄色(溶液②)。取以上溶液进行如下实验,对实验现象分析正确的是
 [CuCl4]2-(黄色)+4H2O;浓度较小时[Cu(H2O)4]2+用Cu2+表示。CuCl2溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓HCl,溶液变为黄色(溶液②)。取以上溶液进行如下实验,对实验现象分析正确的是
[CuCl4]2-(黄色)+4H2O;浓度较小时[Cu(H2O)4]2+用Cu2+表示。CuCl2溶于一定量水中,溶液呈蓝色(溶液①)。加入少量浓HCl,溶液变为黄色(溶液②)。取以上溶液进行如下实验,对实验现象分析正确的是| A.向溶液①加入少量浓HCl,使平衡逆向移动 |
| B.将溶液①置于水浴中加热,颜色变为黄色,说明加热能促进[CuCl4]2-生成 |
| C.加入浓HCl,H+与Cl-对溶液颜色变化、Cu2+浓度大小的影响是一致的 |
| D.向溶液②中加入AgNO3后,黄色褪去,说明Ag+能抑制Cu2+水解 |
您最近一年使用:0次
2022-12-15更新
|
265次组卷
|
2卷引用:四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
4 . 对于可逆反应2A(?)+B(g) 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:

(1)物质A的状态是_________ (填“气体”、“液体”或“固体”);
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是_____ ;
(3)v(a)、v(b)、v(c)按由大到小排序_________________ ;
(4)对于2SO2(g)+O2(g) 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是___________ ;如果在恒容容器中,仅把另外82%的其他气体“抽出来”,是否会减小SO2的转化率__________ (填“会”或“不会”)。
 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
(1)物质A的状态是
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是
(3)v(a)、v(b)、v(c)按由大到小排序
(4)对于2SO2(g)+O2(g)
 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是
您最近一年使用:0次
名校
5 . 下列事实不能用勒夏特列原理解释的是
A.氯水中存在平衡:Cl2 + H2O H++ Cl- + HClO,当加入适量 NaHCO (s)后,溶液颜色变浅 H++ Cl- + HClO,当加入适量 NaHCO (s)后,溶液颜色变浅 |
B.在 K2Cr2O7溶液中存在如下平衡:Cr2O72- + H2O 2CrO42- + 2H+,若向 K2Cr2O7溶液中滴入 5~15 滴浓硫酸,溶液颜色加深 2CrO42- + 2H+,若向 K2Cr2O7溶液中滴入 5~15 滴浓硫酸,溶液颜色加深 |
C.对于反应体系 CO(g) + NO2(g) NO(g) + CO2(g),给平衡体系增大压强可使颜色变深 NO(g) + CO2(g),给平衡体系增大压强可使颜色变深 |
D.对于反应 2NO2(g) N2O4(g)△H < 0,平衡体系升高温度颜色变深 N2O4(g)△H < 0,平衡体系升高温度颜色变深 |
您最近一年使用:0次
2018-11-13更新
|
379次组卷
|
3卷引用:四川省德阳市第五中学2018-2019学年高二上学期第四次(12月)月考化学试题
6 . 下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+H2O HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 |
| B.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 |
| C.高压比常压有利于合成SO3的反应 |
D.对CO(g) + NO2 (g) CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深 CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深 |
您最近一年使用:0次
2016-12-09更新
|
381次组卷
|
4卷引用:2015届四川省德阳市高三4月模拟练习化学试卷



