名校
解题方法
1 . 下列有关实验现象和解释或结论都正确的组合是
| 选项 | 实验操作 | 现象 | 解释或结论 |
A | 相同条件下,分别测量0.1molL1和0.01molL1醋酸溶液的导电性 | 前者的导电性强 | 醋酸浓度越大,电离程度越大 |
B | 向FeCl3和KSCN的混合溶液中加入KCl固体 | 血红色溶液变浅 | 增大KCl的浓度,使得平衡逆向移动 |
C | 两支试管各盛4mL0.1mol/L酸性高锰酸钾溶液,分别加入2mL0.1mol/L草酸溶液和2mL0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
D | 把充有NO2和N2O4的平衡球装置分别放入热水和冷水中 | 热水中颜色更深 | 其他条件不变时,温度升高,平衡向吸热反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-04更新
|
597次组卷
|
4卷引用:广西玉林市2023-2024学年高二上学期11月期中考试化学试题
2 . 二氯异氰尿酸钠(NaC3N3O3Cl2,摩尔质量为220g/mol)是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水,可用次氯酸钠与氰尿酸(C3H3N3O3)制得,其制备原理为:2NaClO+C3H3N3O3=NaC3N3O3Cl2+NaOH+H2O。某小组选择下列部分装置制备二氯异氰尿酸钠并测定产品纯度。
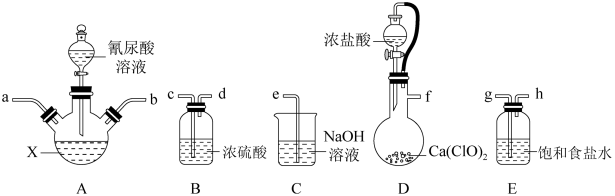
回答下列问题:
(1)A装置中盛装X试剂的仪器名称是___________ ,D中软导管的作用是___________ 。
(2)请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为___________ (填小写字母)。
(3)D中发生反应的离子方程式为___________ 。
(4)X试剂为饱和NaOH溶液。实验时先向A中通入氯气,生成高浓度的NaClO溶液后,再加入氰尿酸溶液。在加入氰尿酸溶液后还要继续通入一定量的氯气,其原因是___________ 。
(5)反应结束后,A中浊液经过滤、___________ 、干燥得到粗产品。该系列操作需要用到如图所示的玻璃仪器有___________ (填字母)。

(6)粗产品中NaC3N3O3Cl2含量测定。称取ag粗产品溶于无氧蒸馏水中配制成250mL溶液,取25.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用cmol/LNa2S2O3标准溶液进行滴定,加入淀粉指示剂,滴定至终点,平均消耗VmLNa2S2O3溶液。(假设杂质不与KI反应,过程中涉及的反应为: +3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2
+3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2 =2I-+
=2I-+ )。则NaC3N3O3Cl2的含量为
)。则NaC3N3O3Cl2的含量为___________ %(用含a、c、V的代数式表示)。

回答下列问题:
(1)A装置中盛装X试剂的仪器名称是
(2)请选择合适的装置,按气流从左至右方向组装,则导管连接顺序为
(3)D中发生反应的离子方程式为
(4)X试剂为饱和NaOH溶液。实验时先向A中通入氯气,生成高浓度的NaClO溶液后,再加入氰尿酸溶液。在加入氰尿酸溶液后还要继续通入一定量的氯气,其原因是
(5)反应结束后,A中浊液经过滤、

(6)粗产品中NaC3N3O3Cl2含量测定。称取ag粗产品溶于无氧蒸馏水中配制成250mL溶液,取25.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用cmol/LNa2S2O3标准溶液进行滴定,加入淀粉指示剂,滴定至终点,平均消耗VmLNa2S2O3溶液。(假设杂质不与KI反应,过程中涉及的反应为:
 +3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2
+3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2 =2I-+
=2I-+ )。则NaC3N3O3Cl2的含量为
)。则NaC3N3O3Cl2的含量为
您最近一年使用:0次
名校
3 . 近几年科学家提出了“绿色自由”的构想。把空气中的CO2进行转化,并使之与H2反应生成可再生能源甲醇。
(1)已知4.4kg CO2与足量H2恰好完全反应,生成气态的水和气态的甲醇,可放出4947kJ的热量,试写出该反应的热化学方程式___________ 。
(2) 一定条件下,往2L恒容密闭容器中充入1mol CO2和3 mol H2在不同催化剂作用下发生反应I、反应II与反应Ⅲ,相同时间内CO2的转化率随温度变化如图(图中c点的转化率为66.67%,即转化了2/3)所示:
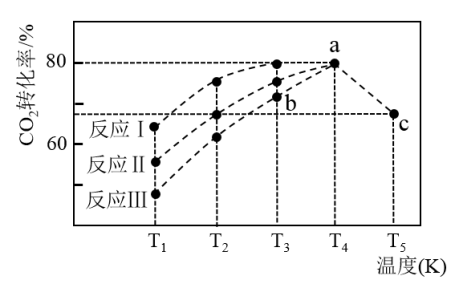
①催化剂效果最佳的反应是___________ (填“反应I”、“反应II”、“反应Ⅲ”)。
②b点v(正)___________ v(逆) (填“>”,“<", “=”) 。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是___________ 。若其他条件不变,将a点容器的体积压缩至原来的一半,一段时间后反应再达平衡时,与原平衡比较下列说法正确的是___________ 。
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比为1:3 D. CH3OH的体积分数增大
④c点时该反应的平衡常数K =___________ 。
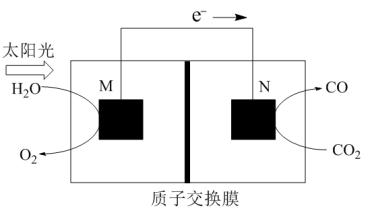
(3)科学家还研究了其它转化温室气体的方法,利用如图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为___________ 。
(1)已知4.4kg CO2与足量H2恰好完全反应,生成气态的水和气态的甲醇,可放出4947kJ的热量,试写出该反应的热化学方程式
(2) 一定条件下,往2L恒容密闭容器中充入1mol CO2和3 mol H2在不同催化剂作用下发生反应I、反应II与反应Ⅲ,相同时间内CO2的转化率随温度变化如图(图中c点的转化率为66.67%,即转化了2/3)所示:

①催化剂效果最佳的反应是
②b点v(正)
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比为1:3 D. CH3OH的体积分数增大
④c点时该反应的平衡常数K =
(3)科学家还研究了其它转化温室气体的方法,利用如图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为

您最近一年使用:0次
名校
4 . 一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
| 平衡v正(SO2)/mol/(L·s) | v1 | v2 | v3 |
| 平衡c(SO3)mol/L | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率/α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 | B.K1>K3,p2>2p3 |
| C.v1>v3,α1(SO2)>α3(SO2) | D.c2>2c3,α2(SO3)+α3(SO2)<1 |
您最近一年使用:0次
2021-08-14更新
|
1550次组卷
|
25卷引用:广西浦北中学2021-2022学年高二上学期第一次月考化学试题
广西浦北中学2021-2022学年高二上学期第一次月考化学试题天津市静海区第一中学2020届高三下学期第六周周末训练化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 高考帮人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关浙江省诸暨市2019-2020学年高二上学期期末考试化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题(已下线)【绍兴新东方】绍兴高中化学00008(已下线)【浙江新东方】高中化学20210304-010(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)吉林省长春市第二中学2021-2022学年高二上学期第一次月考化学试题江西省吉安一中2021-2022学年高二上学期第一次段考化学试题江西省九江市第一中学2021-2022学年高二上学期期中考试化学试题江西省宜春市八校2022-2023学年高二上学期12月联考化学试题河北省部分学校2023-2024学年高二上学期10月联考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题
解题方法
5 . 某电子厂排放的酸性废液中含有Fe3+、Cu2+、Fe2+、Cl-等离子,以这种废液为原料设计制备高纯Fe2O3的工艺流程如图(部分操作和条件略):

已知:①HCl(浓)+FeCl3 HFeCl4(易溶于有机溶剂);
HFeCl4(易溶于有机溶剂);
②Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3。
回答下列问题:
(1)工厂废液浓缩的目的是_______ ,通入氯气发生的氧化还原反应离子方程式为_______ 。
(2)萃取剂要求:①被萃取物在其中的溶解度要大、②与原溶剂不互溶、③_______ ,加水反萃取能发生的原因是_______ (从化学平衡的角度进行解释)。
(3)加入氨水得到的沉淀常用冰水洗涤,目的是_______ ,检验洗涤是否干净的操作为:取最后一次洗出液,向其中滴加_______ ,观察是否有沉淀生成。
(4)加入氨水使溶液中的Fe3+沉淀完全(浓度小于1×10-5 mol·L-1),需调节溶液pH范围为_______ 。

已知:①HCl(浓)+FeCl3
 HFeCl4(易溶于有机溶剂);
HFeCl4(易溶于有机溶剂);②Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3。
回答下列问题:
(1)工厂废液浓缩的目的是
(2)萃取剂要求:①被萃取物在其中的溶解度要大、②与原溶剂不互溶、③
(3)加入氨水得到的沉淀常用冰水洗涤,目的是
(4)加入氨水使溶液中的Fe3+沉淀完全(浓度小于1×10-5 mol·L-1),需调节溶液pH范围为
您最近一年使用:0次
2021-03-18更新
|
213次组卷
|
2卷引用:广西河池市九校2020-2021学年高二下学期第二次联考化学试题
10-11高三上·江苏盐城·期中
名校
6 . 重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O

试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:___________ 。
(2)操作③的目的是什么,用简要的文字说明:____________________________ 。
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:_______ 。
(4)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是:________________ ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度(设整个过程中其它杂质不参与反应)____________ 。
 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
(2)操作③的目的是什么,用简要的文字说明:
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
(4)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是:
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度(设整个过程中其它杂质不参与反应)
您最近一年使用:0次
7 . 氮的固定对工农业及人类生存具有重大意义。
合成氨是最重要的人工固氮:N2(g)+3H2(g) 2NH3(g) △H<0。
2NH3(g) △H<0。
(1)下列关于该反应的说法中,正确的是___________ (填正确选项字母编号)。
A.反应达到平衡状态时,N2、H2、NH3的体积比为1∶3∶2
B.加催化剂可以加快正反应速率,减慢逆反应速率
C.高温既有利于加快反应速率也有利于提高氨气的产率
D.高压既有利于加快反应速率也有利于提高氨气的产率
(2)一定温度下,在容积为1L的密闭容器中,加入lmolN2和3mol H2,反应达到平衡时H2的转化率为60%,此时反应消耗N2物质的量为___________ mol;保持容器体积不变,再向容器中加入1molN2,3mol H2,反应再次达到平衡时,氢气的转化率将___________ (填“增大”或“减小”或“不变”)。
(3)标准状况下,将22.4 mL的氨气通入100 mL 0.01 mol·L-1的盐酸中,充分反应后,溶液中各离子浓度由大到小的顺序是________________________ 。
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入适量的CO2气体,充分反应后,过滤所得滤液为(NH4)2SO4溶液,该过程的化学反应方程式为____________________ 。
(5)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递 H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现常压、570℃高温的电解法合成氨,提高了反应物的转化率,其实验简图如图所示,写出阴极的电极反应式____________________ 。

合成氨是最重要的人工固氮:N2(g)+3H2(g)
 2NH3(g) △H<0。
2NH3(g) △H<0。(1)下列关于该反应的说法中,正确的是
A.反应达到平衡状态时,N2、H2、NH3的体积比为1∶3∶2
B.加催化剂可以加快正反应速率,减慢逆反应速率
C.高温既有利于加快反应速率也有利于提高氨气的产率
D.高压既有利于加快反应速率也有利于提高氨气的产率
(2)一定温度下,在容积为1L的密闭容器中,加入lmolN2和3mol H2,反应达到平衡时H2的转化率为60%,此时反应消耗N2物质的量为
(3)标准状况下,将22.4 mL的氨气通入100 mL 0.01 mol·L-1的盐酸中,充分反应后,溶液中各离子浓度由大到小的顺序是
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入适量的CO2气体,充分反应后,过滤所得滤液为(NH4)2SO4溶液,该过程的化学反应方程式为
(5)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递 H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现常压、570℃高温的电解法合成氨,提高了反应物的转化率,其实验简图如图所示,写出阴极的电极反应式

您最近一年使用:0次



