名校
解题方法
1 . 逆水煤气变换体系中存在以下两个反应:
反应Ⅰ: 反应Ⅱ:
反应Ⅱ:
在恒容条件下,按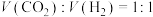 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
反应Ⅰ:
 反应Ⅱ:
反应Ⅱ:
在恒容条件下,按
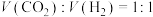 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是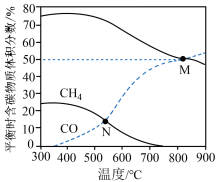
A.反应Ⅰ的 ,反应Ⅱ的 ,反应Ⅱ的 |
B.M点反应Ⅰ的平衡常数 |
C.N点 的物质的量是 的物质的量是 的3倍 的3倍 |
D.若按 投料,则曲线之间交点位置不变 投料,则曲线之间交点位置不变 |
您最近一年使用:0次
名校
解题方法
2 . 资料显示,I2-KI溶液可以清洗银镜。某小组同学设计实验探究银镜在I2-KI溶液中的溶解情况。
已知:I2微溶于水,易溶于KI溶液,并发生反应I2+I− I
I (棕色),I2和I
(棕色),I2和I 氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
探究1:I2-KI溶液(向1mol·L−1KI溶液中加入I2至饱和)溶解银镜
【实验i】_____ 。
(2)能证明②中Ag已全部反应、未被包裹在黄色固体内的实验证据是_____ 。
探究2:I2-KI溶液能快速溶解银镜的原因
【实验ii~iv】向附着银镜的试管中加入相应试剂至浸没银镜,记录如下:
(3)ⅰi中,搅拌后银镜继续溶解的原因是_____ 。
(4)由i、iii可得到的结论是_____ 。
(5)设计iv的目的是_____ 。
探究3:I−的作用
【实验v】
说明:本实验中,检流计读数越大,说明氧化剂氧化性(或还原剂还原性)越强。
(6)步骤1接通电路后,正极的电极反应物为_____ 。
(7)补全步骤3的操作及现象:_____ ,_____ 。
(8)综合上述探究,从反应速率和物质性质的角度分析i中I2-KI溶液能快速全部溶解银镜的原因:_____ 。
已知:I2微溶于水,易溶于KI溶液,并发生反应I2+I−
 I
I (棕色),I2和I
(棕色),I2和I 氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。
氧化性几乎相同;[Ag(S2O3)2]3−在水溶液中无色。探究1:I2-KI溶液(向1mol·L−1KI溶液中加入I2至饱和)溶解银镜
【实验i】
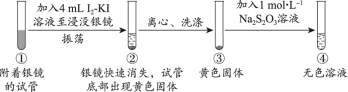
(2)能证明②中Ag已全部反应、未被包裹在黄色固体内的实验证据是
探究2:I2-KI溶液能快速溶解银镜的原因
【实验ii~iv】向附着银镜的试管中加入相应试剂至浸没银镜,记录如下:
| 序号 | 加入试剂 | 实验现象 |
| ⅰi | 4mL饱和碘水(向水中加入I2至饱和, | 30min后,银镜少部分溶解,溶液棕黄色变浅;放置24h后,与紫黑色固体接触部分银镜消失,紫黑色固体表面上有黄色固体,上层溶液接近无色;搅拌后,银镜继续溶解 |
| ⅱi | 4mL饱和碘水和0.66gKI固体(溶液中KI约1mol·L−1) | 15min后银镜部分溶解,溶液棕黄色变浅;放置24h后,试管壁上仍有未溶解的银镜,溶液无色 |
| iv | 4mL1mol·L−1KI溶液 | 放置24h,银镜不溶解,溶液无明显变化 |
(4)由i、iii可得到的结论是
(5)设计iv的目的是
探究3:I−的作用
【实验v】
| 实验装置 | 实验步骤及现象 |
| 1.按左图搭好装置,接通电路,检流计指针向 右微弱偏转,检流计读数为amA; 2.向石墨电极附近滴加饱和碘水,指针继续向 右偏转,检流计读数为bmA(b>a); 3.向左侧烧杯中加入_____,指针继续向右偏转,检流计读数cmA(c>b),有_____生成。 |
(6)步骤1接通电路后,正极的电极反应物为
(7)补全步骤3的操作及现象:
(8)综合上述探究,从反应速率和物质性质的角度分析i中I2-KI溶液能快速全部溶解银镜的原因:
您最近一年使用:0次
2024-04-13更新
|
434次组卷
|
3卷引用:北京市海淀区2023-2024学年高三下学期期中练习化学试题
3 . 对SO2、NOx、CO2和CO进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入NO2、SO2发生反应:NO2(g)+SO2(g)⇌SO3(g)+NO(g)。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是___________ (填序号)。
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是___________ (填字母)。
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为 密闭容器中充入
密闭容器中充入 和
和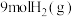 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
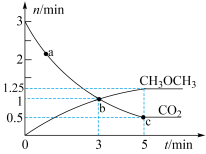
①反应到达3min时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②0~5min内,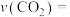
___________  。
。
③反应达到平衡状态时, 的体积分数为
的体积分数为___________ %(保留1位小数)。
④a、b、c三点中代表达到平衡的是___________ ,a点的正反应速率___________ (填>、<或=)b点的逆反应速率。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为
 密闭容器中充入
密闭容器中充入 和
和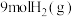 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
①反应到达3min时,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②0~5min内,
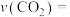
 。
。③反应达到平衡状态时,
 的体积分数为
的体积分数为④a、b、c三点中代表达到平衡的是
您最近一年使用:0次
解题方法
4 . 某学习小组欲利用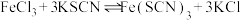 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变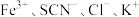 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是___________ (填A或B)。原因是:___________ 。
(2)取 溶液X,加入5滴
溶液X,加入5滴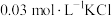 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:①___________ 对平衡产生了影响;②不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.为了探究KCl对 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
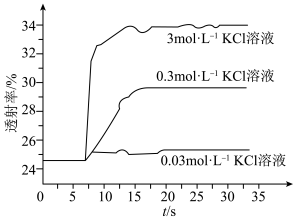
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响___________ 移动(填“正向、逆向或不”)。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:___________ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:
a.溶液中的 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②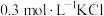 溶液、③
溶液、③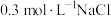 溶液、④
溶液、④ 溶液、⑤
溶液、⑤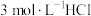 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
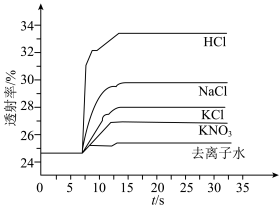
上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是___________ 。盐效应影响较大的阳离子是___________ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)已知 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:___________ 。
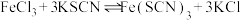 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
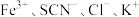 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取
 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是(2)取
 溶液X,加入5滴
溶液X,加入5滴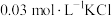 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:① 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.为了探究KCl对
 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。 猜想②:
 产生的影响。
产生的影响。 猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:a.溶液中的
 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取
 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②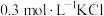 溶液、③
溶液、③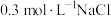 溶液、④
溶液、④ 溶液、⑤
溶液、⑤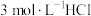 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)已知
 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:
您最近一年使用:0次
名校
5 . 下列事实中,不能用勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
| A.①②⑥⑧ | B.①③⑥⑧ | C.②⑤⑥⑦ | D.②③⑦⑧ |
您最近一年使用:0次
名校
解题方法
6 . I、II、III三个容积均为2L的恒容密闭容器中均投入1mol CO2 和3mol H2 ,在不同温度下发生反应:CO2(g) + 3H2⇌CH3OH(g) + H2O(g) 。反应10min,测得各容器内CO2的物质的量分别如图所示。下列说法正确的是
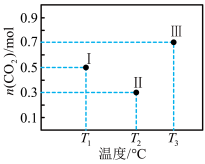

| A.升高温度、增大压强均有利于提高 H2的平衡转化率 |
| B.10min后,向容器Ⅲ中再加入1mol CO2 (g)和1mol H2O (g),此时反应逆向进行 |
| C.容器Ⅱ中的平均速率:v(CO2) =0.07 mol·L-1·min-1 |
| D.10min时,容器Ⅰ中 v(正) = v(逆) |
您最近一年使用:0次
名校
解题方法
7 . 某废矿渣的主要成分有 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
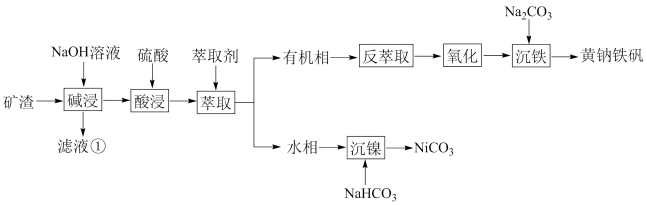
已知:i.黄钠铁矾 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
ii.常温下,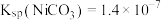 ;
;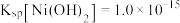 。
。
回答下列问题:
(1)滤液①中,主要存在的钠盐有_____________________ 。
(2)“萃取”可将金属离子进行富集与分离,原理如下:
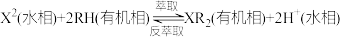 。
。
则“反萃取”应控制在____________________ (填“碱性”、“酸性”或“中性”)环境进行。
(3)“氧化”中加入 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为____________________ 。
(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为_________________________ ,“沉镍”时若溶液 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是__________________________ 。
(5)“沉铁”过程反应的离子方程式为_________________________ 。
(6)定量分析:
测定“酸漫”后的溶液中 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用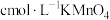 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
已知:i.黄钠铁矾
 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;ii.常温下,
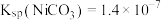 ;
;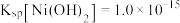 。
。回答下列问题:
(1)滤液①中,主要存在的钠盐有
(2)“萃取”可将金属离子进行富集与分离,原理如下:
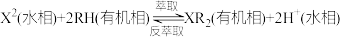 。
。则“反萃取”应控制在
(3)“氧化”中加入
 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为
 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是(5)“沉铁”过程反应的离子方程式为
(6)定量分析:
测定“酸漫”后的溶液中
 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用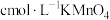 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
8 . 某兴趣小组以重铬酸钾( )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。
已知:在水溶液中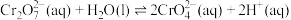
查阅资料:①含铬元素的离子在溶液中的颜色: (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);
② 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
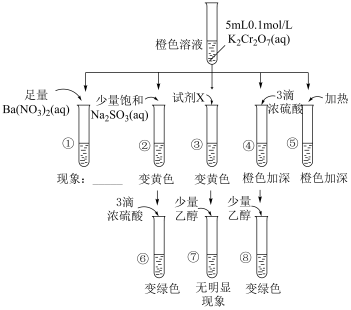
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为___________ ,试剂X是___________ (填化学式)。
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是___________ ,实验⑥中发生反应的离子方程式为___________ 。
(3)结合③、④、⑦、⑧可得出结论为___________ 。
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?___________ (填“能”或“否”)。
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:
 正反应的焓变
正反应的焓变
_______ 0(填“>”、“<”或“=”)。
 )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。已知:在水溶液中
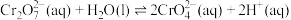
查阅资料:①含铬元素的离子在溶液中的颜色:
 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);②
 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是
(3)结合③、④、⑦、⑧可得出结论为
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:

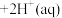 正反应的焓变
正反应的焓变
您最近一年使用:0次
2024-01-09更新
|
55次组卷
|
2卷引用:安徽省安庆市田家炳中学(安庆市第十中学)2023-2024学年高二上学期期中考试化学试题
解题方法
9 . “碳达峰、碳中和”是我国社会发展重大战略之一, 的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用
的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用 的方法。
的方法。
方法I: 加氢制备合成气
加氢制备合成气
在一定温度、压强为 条件下,
条件下, 和
和 按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
相关化学键的键能数据如下表:
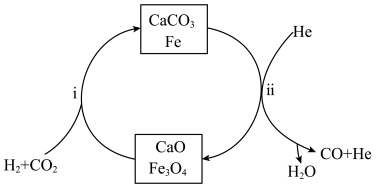
(1)该反应的热化学方程式为
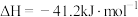 ,则
,则
______ 。
(2)有关该反应的说法错误的是_______(填标号)。
(3)反应i达到平衡后通入 ,有利于反应ii的进行,结合平衡移动原理,解释原因
,有利于反应ii的进行,结合平衡移动原理,解释原因_____________________________________________ 。
方法II: 重整制备合成气
重整制备合成气
 重整制备合成气时发生的反应主要有:
重整制备合成气时发生的反应主要有:
主反应:

副反应: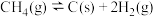
(4)在一定条件下,向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
__________ 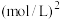 。
。
(5)主反应的反应速率 ,
, ,
, 符合阿伦尼乌斯公式
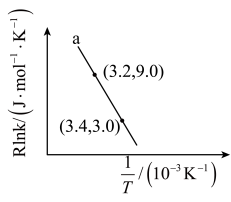
符合阿伦尼乌斯公式 (Ea为活化能、T为温度,R、C为常数),实验测得
(Ea为活化能、T为温度,R、C为常数),实验测得 的实验数据如图所示,则该反应正反应的活化能为
的实验数据如图所示,则该反应正反应的活化能为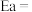
________  ,升高温度时,
,升高温度时,
_____ (填“增大”、“减小”或“不变”)。
(6)一定条件下重整反应中会因发生副反应产生积碳而导致催化剂活性降低,若向容器中通入过量水蒸气可以清除积碳,反应的化学方程式为__________ , 的值
的值__________ (填“增大”、“减小”或“不变”)。
 的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用
的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用 的方法。
的方法。方法I:
 加氢制备合成气
加氢制备合成气在一定温度、压强为
 条件下,
条件下, 和
和 按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。相关化学键的键能数据如下表:

化学键 |
|
|
|
|
键能E/( | 745 | a | 1046 | 436 |
(1)该反应的热化学方程式为

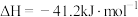 ,则
,则
(2)有关该反应的说法错误的是_______(填标号)。
| A.当装置内的气体压强不变时,反应达到平衡状态 |
B.若在反应中能及时分离出 ,可以提高 ,可以提高 的转化率 的转化率 |
C.反应ii的总反应为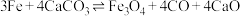 |
D.选择合适的催化剂会提高平衡时 的产率 的产率 |
(3)反应i达到平衡后通入
 ,有利于反应ii的进行,结合平衡移动原理,解释原因
,有利于反应ii的进行,结合平衡移动原理,解释原因方法II:
 重整制备合成气
重整制备合成气 重整制备合成气时发生的反应主要有:
重整制备合成气时发生的反应主要有:主反应:


副反应:
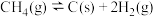
(4)在一定条件下,向
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
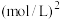 。
。(5)主反应的反应速率
 ,
, ,
, 符合阿伦尼乌斯公式
符合阿伦尼乌斯公式 (Ea为活化能、T为温度,R、C为常数),实验测得
(Ea为活化能、T为温度,R、C为常数),实验测得 的实验数据如图所示,则该反应正反应的活化能为
的实验数据如图所示,则该反应正反应的活化能为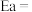
 ,升高温度时,
,升高温度时,

(6)一定条件下重整反应中会因发生副反应产生积碳而导致催化剂活性降低,若向容器中通入过量水蒸气可以清除积碳,反应的化学方程式为
 的值
的值
您最近一年使用:0次
名校
10 . 根据实验目的,下列实验及现象、结论正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 探究温度对平衡移动的影响 | 向试管中加入2mL CuCl2溶液,CuCl2溶液存在 CuCl2溶液,CuCl2溶液存在   ,加热试管,溶液由蓝绿色变为黄绿色 ,加热试管,溶液由蓝绿色变为黄绿色 | 其他条件不变时,升高温度,平衡向吸热反应方向移动 |
| B | 探究氢离子浓度对 、 、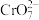 相互转化的影响 相互转化的影响 | 向2mL K2Cr2O7溶液中滴加5~10滴 K2Cr2O7溶液中滴加5~10滴 NaOH溶液,溶液变为黄色 NaOH溶液,溶液变为黄色 | 其他条件不变时,减小氢离子浓度,平衡向生成 的方向移动 的方向移动 |
| C | 探究压强对平衡移动的影响 | 用注射器吸入20mLNO2和N2O4混合气体,向内推动注射器,混合气体颜色加深 | 其他条件不变时,加压,平衡向生成NO2的方向移动 |
| D | 验证CH3COOH和H2CO3的酸性 | 向盛有2mL1mol/L的Na2CO3溶液中,逐滴加入同体积同浓度的CH3COOH溶液,无气泡产生 | 酸性强弱: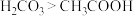 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次






 )
)

