1 . 下列事实能用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 |
B.铁钉放入浓 中不再变化后,加热能产生大量红棕色气体 中不再变化后,加热能产生大量红棕色气体 |
C.氯碱工业中阳极区的溶液用盐酸调pH为2~3,促进 的产生 的产生 |
D.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
您最近一年使用:0次
名校
解题方法
2 . 下列实验能达到实验目的的是
| A | B |
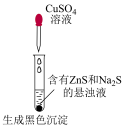 | 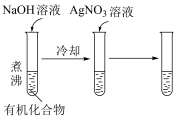 |
比较相同温度下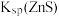 和 和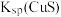 的大小 的大小 | 检验有机化合物中含溴原子 |
| C | D |
 | 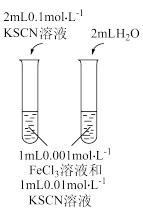 |
| 探究干燥的氯气是否具有漂白性 | 研究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 某兴趣小组将4g铁钉放入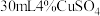 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
①CuSCN:白色固体,不溶于水;
②室温下,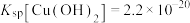 ,
, ,
, 。
。
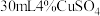 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是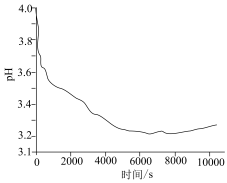
①CuSCN:白色固体,不溶于水;
②室温下,
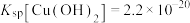 ,
, ,
, 。
。A. 溶液 溶液 的原因是 的原因是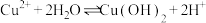 |
B.0~6000s,随着反应进行,溶液pH下降的原因可能是 被 被 氧化为 氧化为 |
C.反应后期溶液pH略有上升的可能原因是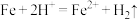 |
D.溶液先变红后又褪色的可能原因是 的反应速率快, 的反应速率快,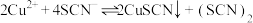 的反应限度大 的反应限度大 |
您最近一年使用:0次
2024-02-29更新
|
115次组卷
|
3卷引用:北京市第一七一中学2023-2024学年高三下学期开学考试化学试题
23-24高三下·北京·开学考试
名校
解题方法
4 . 下列方程式不正确 的是
A.用稀 清洗银镜: 清洗银镜: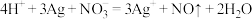 |
B.氢氧化亚铁露置在空气中变为红褐色: |
C.向苯酚钠溶液中通入 ,溶液变浑浊:2 ,溶液变浑浊:2  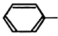 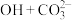 |
D.向 溶液中滴加少量硫酸,溶液橙色加深: 溶液中滴加少量硫酸,溶液橙色加深: |
您最近一年使用:0次
名校
解题方法
5 . 某化学小组通过测定溶液pH,计算K2Cr2O7溶液中“Cr2O (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:
下列说法不合理的是
 (橙色)+H2O=2CrO
(橙色)+H2O=2CrO (黄色)+2H+”的平衡常数,结果如下:
(黄色)+2H+”的平衡常数,结果如下:| 实验序号 | 温度(°C) | K2Cr2O7溶液浓度(mol/L) | pH | 平衡常数 |
| ① | 26.3 | 0.1000 | a | 2.5×10-15 |
| ② | 26.3 | 0.3000 | 3.78 | b |
| ③ | 50.0 | 0.1000 | 3.75 | 1.01×10-14 |
| A.a大于3.78 |
| B.b等于2.5×10-15 |
| C.由实验①③结果可说明该反应为吸热反应 |
| D.向实验①2mL溶液中加入6滴6mol/LNaOH溶液,溶液橙色加深;恢复原温度,平衡常数不变 |
您最近一年使用:0次
名校
6 . I.某小组对Cu与浓HNO3的反应进行研究。记录如下:
(1)Cu与浓HNO3反应的化学方程式是___________ 。
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是___________ 。
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是___________ 、___________ 。
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii. 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)
据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了 使溶液呈绿色。
使溶液呈绿色。
丙进行如下实验:
①亚硝酸分解的化学方程式是___________ 。
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:___________ 。
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是___________ 。请依据实验现象阐述理由:___________ 。
| 装置 | 药品 | 现象 | |
| 实验1 | 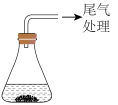 | 0.64gCu片(0.01mol) Cu片和20.0 mL浓HNO3 | Cu片消失,得到绿色溶液A,放置较长时间后得到蓝色溶 液B,…… |
(1)Cu与浓HNO3反应的化学方程式是
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii.
 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了
 使溶液呈绿色。
使溶液呈绿色。丙进行如下实验:
| 操作 | 现象 | |
| 实验3 | i.配制与溶液A的c(H+)相同的HNO3溶液,取20.0mL,通入NO2气体 | 溶液呈黄色 |
| ii.再加0.01molCu(NO3)2固体搅拌至完全溶解 | 溶液变为绿色 | |
| iii.加水稀释 | 溶液立即变蓝 | |
| 实验4 | i.向20.0mL0.5mol/L Cu(NO3)2蓝色溶液中通入少量NO2 | 溶液呈绿色 |
| ii.加入稀H2SO4 | 有无色气体放出,遇空气变红棕色,溶液很快变为蓝色 |
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是
您最近一年使用:0次
名校
7 . 手机主板中含有贵金属单质Au(金)、Ag和Pd(钯)。如图方法可从侤旧手机主板中回收贵金属。

已知:i.Au+3 +6H+
+6H+ Au3++3NO2↑+3H2O K<10-5
Au3++3NO2↑+3H2O K<10-5
Au+ +4H+
+4H+ Au3++NO↑+2H2O K<10-5
Au3++NO↑+2H2O K<10-5
Au3++4Cl- [AuCl4]- K>105
[AuCl4]- K>105
ii.HAuCl4=H++[AuCl4]-
(1)酸浸前,将废旧手机主板粉碎的目的是_______ 。
(2)已知:王水[V(浓硝酸):V(浓盐酸)=1:3]溶金反应时产生NO。
①写出该反应的离子方程式:________ 。
②从反应原理的角度解释浓盐酸的作用________ 。
(3)若用Zn粉将溶液中的1molHAuCl4完全还原,则参加反应的Zn的物质的量是________ mol。
(4)AgCl溶于氨水的离子方程式为________ 。
(5)水合肼(N2H4•H2O)是一种液态还原剂,能直接与AgCl反应生成单质Ag。上述工艺中,先将氯化银溶于氨水,再与水合肼反应,除了“碱性条件下水合肼的还原性增强”,还具有的优点可能有________ (写出一条即可)。
(6)Pd(NH3)2Cl2难溶于水,溶于氨水,是一种电镀试剂,是制备钯及其化合物的重要原料。加入氨水,[PdCl4]2-转化为[Pd(NH3)4]2+,则该条件下配位能力:Cl-_______ NH3(填“>”或“<”)。

已知:i.Au+3
 +6H+
+6H+ Au3++3NO2↑+3H2O K<10-5
Au3++3NO2↑+3H2O K<10-5Au+
 +4H+
+4H+ Au3++NO↑+2H2O K<10-5
Au3++NO↑+2H2O K<10-5Au3++4Cl-
 [AuCl4]- K>105
[AuCl4]- K>105ii.HAuCl4=H++[AuCl4]-
(1)酸浸前,将废旧手机主板粉碎的目的是
(2)已知:王水[V(浓硝酸):V(浓盐酸)=1:3]溶金反应时产生NO。
①写出该反应的离子方程式:
②从反应原理的角度解释浓盐酸的作用
(3)若用Zn粉将溶液中的1molHAuCl4完全还原,则参加反应的Zn的物质的量是
(4)AgCl溶于氨水的离子方程式为
(5)水合肼(N2H4•H2O)是一种液态还原剂,能直接与AgCl反应生成单质Ag。上述工艺中,先将氯化银溶于氨水,再与水合肼反应,除了“碱性条件下水合肼的还原性增强”,还具有的优点可能有
(6)Pd(NH3)2Cl2难溶于水,溶于氨水,是一种电镀试剂,是制备钯及其化合物的重要原料。加入氨水,[PdCl4]2-转化为[Pd(NH3)4]2+,则该条件下配位能力:Cl-
您最近一年使用:0次
2023-08-31更新
|
155次组卷
|
2卷引用:北京市清华大学附属中学2023-2024学年高三上学期开学考试化学(A)试题
名校
解题方法
8 . 用下列仪器或装置(部分夹持装置略)进行相应实验,能够达到实验目的的是
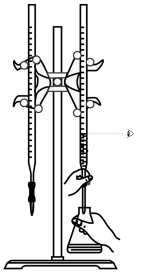 | 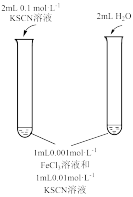 | 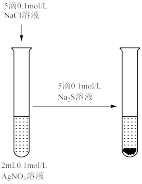 |  |
| A.用标准NaOH溶液滴定锥形瓶中的盐酸 | B.研究浓度对化学平衡的影响 | C.验证沉淀转化:AgCl转化为 | D.检验 溶液是否变质 溶液是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-04更新
|
204次组卷
|
2卷引用:北京市第九中学2023-2024学年高二下学期2月开学考化学试题
名校
9 . CuCl2溶液中存在如下平衡:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
[CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
 [CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
[CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是| A.升温 | B.加NaCl(s) | C.加压 | D.加AgNO3(s) |
您最近一年使用:0次
2022-11-17更新
|
204次组卷
|
18卷引用:北京市八十中2020-2021学年高二下学期开学考试化学试题
北京市八十中2020-2021学年高二下学期开学考试化学试题北京市西城区2020-2021学年高二上学期期末考试化学试题北京市回民学校2021-2022学年高二上学期期中考试化学试题北京师范大学第二附属中学未来科技城学校2021-2022学年高二上学期期中考试化学试题北京市石景山区第九中学2021-2022学年高二上学期期中考试化学试题北京市师范大学亚太实验学校2021-2022学年高二上学期期中考试化学试题北京市中国农业大学附属中学2021-2022学年高二上学期期中学业水平调研化学试题北京市第七中学2022-2023学年高二上学期期中化学试题北京师范大学第二附属中学2022-2023学年高二上学期期中考试化学试题北京市第四十三中学2021-2022学年高二上学期期中考试化学试题北京市北京医学院附属中学2022-2023学年高二上学期期中考试化学试题北京市中国人民大学附属中学通州校区2023-2024学年高二上学期10月月考化学试题北京市第十一中学2022-2023学年高二上学期期中考试化学试卷黑龙江省大庆市第二中学2022-2023学年高二上学期第一次月考化学试题天津市南开大学附属中学2022-2023学年高二上学期期中阶段检测化学试题天津市南开区2022-2023学年高二上学期阶段性质量监测化学试题山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期11月月考化学试题
名校
10 . 若反应:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
 N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是
N2(g)+2CO2(g) ΔH=-373.4kJ·mol-1(汽车尾气净化反应之一)在恒容密闭容器中达到平衡状态,以下说法不正确的是| A.及时分离出 CO2,使 Q 减小,Q<K,因此平衡正向移动 |
| B.及时分离出 N2,使 Q 减小,Q<K,因此平衡正向移动 |
| C.降低温度,使 Q 减小,Q<K,因此平衡正向移动 |
| D.加入催化剂可增大反应速率,从而增大一段时间内的反应物转化率 |
您最近一年使用:0次
2021-02-20更新
|
240次组卷
|
4卷引用:北京市八十中2020-2021学年高二下学期开学考试化学试题



