1 . 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
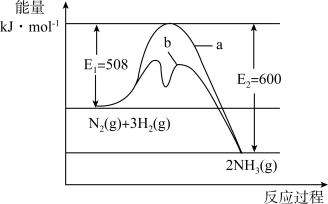
(1)根据图提供的信息,写出该反应的热化学方程式___________ ,在图中曲线___________ (填“a”或“b”)表示加入铁触媒的能量变化曲线,判断理由是___________ 。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=___________ ,该温度下的平衡常数K=___________ 。(小数点后保留3位有效数字)
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正___________ v逆(填“大于”、“小于”或“等于”)。

(1)根据图提供的信息,写出该反应的热化学方程式
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
| A.3v(H2)正=2v(NH3)逆 |
| B.单位时间内生成n mol N2的同时生成2n mol NH3 |
| C.混合气体的密度不再改变 |
| D.容器内压强不随时间的变化而变化 |
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正
您最近一年使用:0次
2023-11-04更新
|
80次组卷
|
2卷引用:甘肃省兰州市教育局第四片区联考2023-2024学年高二上学期期中考试化学试题
名校
解题方法
2 . 元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子,原子核外有_______ 种不同能量的电子,写出其最外层电子的轨道表示式_______ ;碘元素在元素周期表中的位置是_______ ;液溴的保存通常采取的方法是_______ 。
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
(3) 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是_______ 。
(4)已知: 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_______
(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_______
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是_______ (填字母)。
a.海盐提纯:

b.海水提镁:
c.海带提碘: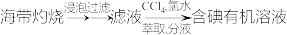

d.海水提溴:
(1)与氯元素同族的短周期元素的原子,原子核外有
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
A. 、 、 、 、 的氧化性 的氧化性 | B. 、 、 、 、 的熔点 的熔点 |
| C.HCl、HBr、HI的热稳定性 | D.HCl、HBr、HI的酸性 |
 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是(4)已知:
 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是
a.海盐提纯:


b.海水提镁:

c.海带提碘:
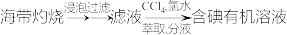

d.海水提溴:

您最近一年使用:0次
2022-11-11更新
|
173次组卷
|
2卷引用:上海市宝山区行知中学2022-2023学年高三上学期期中测试化学试题
名校
解题方法
3 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺技术是国内外研究的热点。研究表明,氮氧化物(NOx)和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如下图所示。
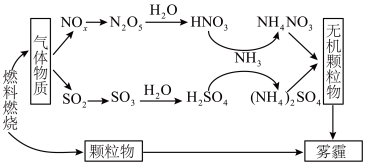
(1)NH4NO3溶液中的离子浓度由大到小顺序是_______ 。
(2)① 已知:SO2生成SO3总反应方程式是:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ/mol
2SO3(g) ΔH=-196.6 kJ/mol
此反应可通过如下两步完成:
2NO(g)+O2 (g ) 2NO2(g) ΔH1=-113 kJ/mol
2NO2(g) ΔH1=-113 kJ/mol
NO2(g)+SO2(g) SO3(g)+NO(g) ΔH2=
SO3(g)+NO(g) ΔH2=_______ 。
② 一定温度下,向2 L恒容密闭容器中充入NO2和SO2各1 mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是_______ 。
(3)SO2属于酸性氧化物,将其通入NaOH溶液中,得到NaHSO3溶液。
①NaHSO3溶液呈酸性,其原因是_______
② 向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因是_______
(4)某同学用中和滴定法测定某烧碱样品的纯度,实验步骤如下:
Ⅰ、配制待测液:称量5.0 g烧碱样品(杂质不与硫酸反应),配成1000 mL溶液;
Ⅱ、滴定:取20.00mL所配待测液,用0.05mol·L-1的H2SO4标准溶液进行滴定,达到滴定终点后,重复此操作两次;记录数据如下表:
计算烧碱样品的纯度是_______ (计算结果保留三位有效数字)
下列实验操作,会使测定结果偏高的是_______ 。
A.酸式滴定管未润洗就装H2SO4标准溶液滴定
B.锥形瓶在蒸馏水洗净后未用待测液润洗
C.读取H2SO4标准溶液读数时,滴定前仰视,滴定到终点后俯视
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失

(1)NH4NO3溶液中的离子浓度由大到小顺序是
(2)① 已知:SO2生成SO3总反应方程式是:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ/mol
2SO3(g) ΔH=-196.6 kJ/mol此反应可通过如下两步完成:
2NO(g)+O2 (g )
 2NO2(g) ΔH1=-113 kJ/mol
2NO2(g) ΔH1=-113 kJ/molNO2(g)+SO2(g)
 SO3(g)+NO(g) ΔH2=
SO3(g)+NO(g) ΔH2=② 一定温度下,向2 L恒容密闭容器中充入NO2和SO2各1 mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是
(3)SO2属于酸性氧化物,将其通入NaOH溶液中,得到NaHSO3溶液。
①NaHSO3溶液呈酸性,其原因是
② 向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因是
(4)某同学用中和滴定法测定某烧碱样品的纯度,实验步骤如下:
Ⅰ、配制待测液:称量5.0 g烧碱样品(杂质不与硫酸反应),配成1000 mL溶液;
Ⅱ、滴定:取20.00mL所配待测液,用0.05mol·L-1的H2SO4标准溶液进行滴定,达到滴定终点后,重复此操作两次;记录数据如下表:
| 测定序号 | 待测溶液体积(mL) | 所耗H2SO4标准溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
| 3 | 20.00 | 1.30 | 21.50 |
计算烧碱样品的纯度是
下列实验操作,会使测定结果偏高的是
A.酸式滴定管未润洗就装H2SO4标准溶液滴定
B.锥形瓶在蒸馏水洗净后未用待测液润洗
C.读取H2SO4标准溶液读数时,滴定前仰视,滴定到终点后俯视
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失
您最近一年使用:0次
名校
解题方法
4 . 由γ-丁酸生成γ-丁内酯的反应如下:HOCH2CH2CH2COOH
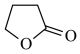 +H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
+H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
(1)该反应在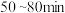 内的平均反应速率为
内的平均反应速率为_______  。
。
(2)该反应化学平衡常数K的表达式是_______ ,298K时该反应的平衡常数K=_______ 。
(3)求120min时γ-羟基丁酸的转化率为_______ (请写出计算过程,注意格式规范)
(4)为提高γ-羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是_______

 +H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
+H2O,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180mol/L,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题: | 21 | 50 | 80 | 100 | 120 | 160 | 220 |  |
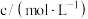 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
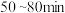 内的平均反应速率为
内的平均反应速率为 。
。(2)该反应化学平衡常数K的表达式是
(3)求120min时γ-羟基丁酸的转化率为
(4)为提高γ-羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是
您最近一年使用:0次
解题方法
5 . 砷酸 、亚砷酸
、亚砷酸 是两种弱酸。回答下列问题:
是两种弱酸。回答下列问题:
(1)已知:①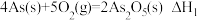
②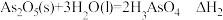
③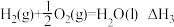
则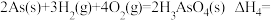
___________ (用 、
、 、
、 的代数式表示)。
的代数式表示)。
(2) 下,向某容器中加入一定量的
下,向某容器中加入一定量的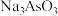 、
、 和
和 溶液,发生反应:
溶液,发生反应: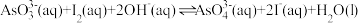 ,
, 的转化率
的转化率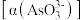 与时间的关系如图所示,测得F点达到平衡,此时对应溶液中
与时间的关系如图所示,测得F点达到平衡,此时对应溶液中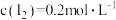 、
、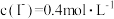 ,且溶液
,且溶液 。
。

①该反应的平衡常数表达式为
___________ 。
②E点的
___________ F点的 (填“>”“<”或“=”),
(填“>”“<”或“=”), 时间段
时间段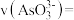
___________  (用含t的代数式表示)。
(用含t的代数式表示)。
③不能表明该反应达到平衡状态的是___________ (填字母)
a.溶液颜色不再变化 b.溶液的 不再变化
不再变化
c.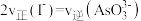 d.溶液中
d.溶液中
④常温下,向平衡后溶液中加入少量 固体,混合溶液中
固体,混合溶液中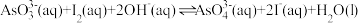 平衡向
平衡向___________ (填“正向”、“逆向”或“无影响”)移动。
 、亚砷酸
、亚砷酸 是两种弱酸。回答下列问题:
是两种弱酸。回答下列问题:(1)已知:①
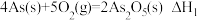
②
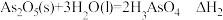
③
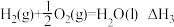
则
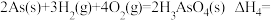
 、
、 、
、 的代数式表示)。
的代数式表示)。(2)
 下,向某容器中加入一定量的
下,向某容器中加入一定量的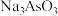 、
、 和
和 溶液,发生反应:
溶液,发生反应: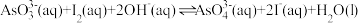 ,
, 的转化率
的转化率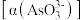 与时间的关系如图所示,测得F点达到平衡,此时对应溶液中
与时间的关系如图所示,测得F点达到平衡,此时对应溶液中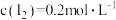 、
、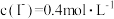 ,且溶液
,且溶液 。
。
①该反应的平衡常数表达式为

②E点的

 (填“>”“<”或“=”),
(填“>”“<”或“=”), 时间段
时间段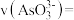
 (用含t的代数式表示)。
(用含t的代数式表示)。③不能表明该反应达到平衡状态的是
a.溶液颜色不再变化 b.溶液的
 不再变化
不再变化c.
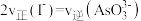 d.溶液中
d.溶液中
④常温下,向平衡后溶液中加入少量
 固体,混合溶液中
固体,混合溶液中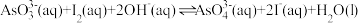 平衡向
平衡向
您最近一年使用:0次
名校
6 .  温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。

(1)写出容器中发生反应的方程式___________ ;正反应为___________ 反应(填“放热”或“吸热”)。
(2)当 时,该反应
时,该反应___________ 达到平衡状态(填“已”或“未”);由图Ⅰ,若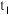 为10min,则
为10min,则 时间内,
时间内,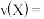
___________ ; 时平衡常数K=
时平衡常数K=___________ (保留小数点后一位)。
(3)其它条件不变,再充入一定量X,平衡___________ 移动(填“正向”、“逆向”、或“不”),X的转化率___________ (填“增大”、“减小”、或“不变”)。
 温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为
温度时,在容积为1L的密闭容器中,X、Y、Z三种气体的浓度随时间变化如图Ⅰ。其它条件不变,当温度分别为 和
和 时,Y的体积分数与时间关系如图Ⅱ。
时,Y的体积分数与时间关系如图Ⅱ。
(1)写出容器中发生反应的方程式
(2)当
 时,该反应
时,该反应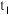 为10min,则
为10min,则 时间内,
时间内,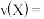
 时平衡常数K=
时平衡常数K=(3)其它条件不变,再充入一定量X,平衡
您最近一年使用:0次
2021-12-18更新
|
226次组卷
|
4卷引用:安徽省黄山市屯溪第一中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
7 . 近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(1)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+ Cl2(g) ΔH1=+83 kJ∙mol−1
Cl2(g) ΔH1=+83 kJ∙mol−1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=−20 kJ∙mol−1
Cl2(g) ΔH2=−20 kJ∙mol−1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=−121 kJ∙mol−1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=___________ kJ∙mol−1
(2)Deacon发明的直接氧化法原理为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g),在刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系如图所示:

据图象分析可知:反应平衡常数K(300 ℃)___________ K(400 ℃)(填“大于”或“小于”)。
(3)设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据,计算K(400 ℃)=___________ (列出计算式)。
(4)按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是___________ 、___________ 。在一定温度的条件下,进一步提高HCl的转化率的方法是___________ 。(写出2种)
(1)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=+83 kJ∙mol−1
Cl2(g) ΔH1=+83 kJ∙mol−1CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=−20 kJ∙mol−1
Cl2(g) ΔH2=−20 kJ∙mol−1CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=−121 kJ∙mol−1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=
(2)Deacon发明的直接氧化法原理为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g),在刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系如图所示:

据图象分析可知:反应平衡常数K(300 ℃)
(3)设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据,计算K(400 ℃)=
(4)按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是
您最近一年使用:0次
2021-05-18更新
|
301次组卷
|
2卷引用:海南省海口市2021年高三高考调研测试化学试题
名校
解题方法
8 . SO2随意排放会造成严重的大气污染。下列是某小组同学设计处理烟气(主要含SO2、N2、O2、粉尘)中SO2的方法。
(1)方法一:利用氯碱工业产品处理含SO2的烟气,流程如下:
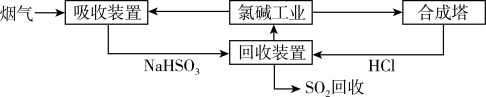
①“吸收装置”中发生反应的离子方程式是___________ 。
②合成塔中每合成1 mol气体放出热量92.3 kJ(25 ℃、101 kPa),反应的热化学方程式是___________ 。
③上述流程中循环利用的物质是___________ 。
(2)方法二:利用FeCl3溶液的氧化性吸收烟气中的SO2。
①该反应的离子方程式是___________ (反应a)。为验证该反应,同学们将SO2通入0.05 mol·L-1 FeCl3溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色。
关于红褐色液体,以下是同学们的分析推测与实验。
②利用胶体的___________ (填性质)可以检验步骤ⅰ中是否得到了Fe(OH)3胶体。
③根据反应b,说明步骤ⅱ中液体颜色变化的原因是___________ (用离子方程式及必要的文字说明)。
(3)制备Cl2反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,可采用酸碱中和滴定法。用___________ (填“酸式”或“碱式”)滴定管量取试样20.00 mL,用0.10 mol·L-1 NaOH标准溶液滴定,消耗22.00 mL,该次滴定测得试样中盐酸浓度为___________ mol·L-1。
(1)方法一:利用氯碱工业产品处理含SO2的烟气,流程如下:

①“吸收装置”中发生反应的离子方程式是
②合成塔中每合成1 mol气体放出热量92.3 kJ(25 ℃、101 kPa),反应的热化学方程式是
③上述流程中循环利用的物质是
(2)方法二:利用FeCl3溶液的氧化性吸收烟气中的SO2。
①该反应的离子方程式是
关于红褐色液体,以下是同学们的分析推测与实验。
| 分析推测 | 实验步骤及现象 |
| 甲:生成了Fe(OH)3胶体 乙:经查阅资料,可能发生反应:Fe3++6SO2  Fe(SO2) Fe(SO2)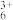 (反应b) (反应b) | ⅰ。制备Fe(OH)3胶体并检验 ⅱ。分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
③根据反应b,说明步骤ⅱ中液体颜色变化的原因是
(3)制备Cl2反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,可采用酸碱中和滴定法。用
您最近一年使用:0次
解答题-原理综合题
|
较易(0.85)
|
9 . 已知在容积为2.0L的恒容密闭容器中存在可逆反应:M(g)+N(g) P(g)+W(g)。该可逆反应的平衡常数与温度的关系如表:
P(g)+W(g)。该可逆反应的平衡常数与温度的关系如表:
回答下列问题:
(1)温度为300℃时,在容器中加入0.5molM和0.5molN,4min时反应达到平衡。
①平衡时气体的总物质的量为___ mol。
②N的转化率为___ %。
③若保持温度不变,再向容器中充入0.25molM和0.25molN,平衡将___ (填“正向”逆向”或“不”)移动。
(2)某温度下,将一定量的M和N充入该容器中,测得不同条件下反应过程中部分物质的物质的量变化情况如图所示。

①生成物W在4~6min内的平均反应速率 (W)=
(W)=___ mol·L-1·min-1。
②第8min时改变的反应条件可能是___ (填标号)。
A.增大压强 B.减小压强 C.升高温度 D.降低温度
③若反应在第8min时,改变了反应的温度,则反应在第12min时,反应体系的温度为___ (填范围或数值)。
 P(g)+W(g)。该可逆反应的平衡常数与温度的关系如表:
P(g)+W(g)。该可逆反应的平衡常数与温度的关系如表:| 温度/℃ | 300 | 500 | 700 | 900 |
| 平衡常数 |  | 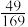 |  |  |
回答下列问题:
(1)温度为300℃时,在容器中加入0.5molM和0.5molN,4min时反应达到平衡。
①平衡时气体的总物质的量为
②N的转化率为
③若保持温度不变,再向容器中充入0.25molM和0.25molN,平衡将
(2)某温度下,将一定量的M和N充入该容器中,测得不同条件下反应过程中部分物质的物质的量变化情况如图所示。

①生成物W在4~6min内的平均反应速率
 (W)=
(W)=②第8min时改变的反应条件可能是
A.增大压强 B.减小压强 C.升高温度 D.降低温度
③若反应在第8min时,改变了反应的温度,则反应在第12min时,反应体系的温度为
您最近一年使用:0次
名校
解题方法
10 . 甲酸钠是一种重要的化工原料。在0.5L真空密闭耐压容器中,将预先用95%乙醇水溶液配制的0.2LNaOH溶液加入上述耐压容器中,加热并搅拌,达到60℃恒温时,通入CO至一定压强,开始反应后记录容器内压强随时间的变化,直到压强不再变化后,冷却,泄压,取出反应物,抽滤、烘干并称量。其反应如下:
I:CO(g)+H2O(l)⇌HCOOH(aq) K1 ΔH1
II:HCOOH(aq)+NaOH(aq)⇌HCOONa(s)+H2O(l) K2 ΔH2
III:CO(g)+NaOH(aq)⇌HCOONa(s) K ΔH
回答下列问题:
(1)K=______ (用含K1、K2的代数式表示),ΔH=_____ (用含ΔH1、ΔH2的代数式表示)。
(2)若需加快反应III的速率,下列措施可行的是______ (填字母)。
A.增大CO的初始压强 B.适当升高温度 C.减少乙醇浓度 D.降低搅拌转速
(3)CO的压强转化率可以反映羧基化进程。CO的压强转化率可以表示为X(CO)=(1-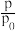 )×100%,p0为CO初始压强,p为CO某时刻分压。HCOONa产率可表示为Y(HCOONa)=
)×100%,p0为CO初始压强,p为CO某时刻分压。HCOONa产率可表示为Y(HCOONa)= ×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成的HCOONa的物质的量。投料比r=
×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成的HCOONa的物质的量。投料比r= ,n0(CO)表示投料CO的物质的量,保持60℃恒温,以投料比r=0.7时,CO初始压强分别为0.5MPa、1.5MPa和2.0MPa,测得X(CO)与时间t的关系如下图所示。
,n0(CO)表示投料CO的物质的量,保持60℃恒温,以投料比r=0.7时,CO初始压强分别为0.5MPa、1.5MPa和2.0MPa,测得X(CO)与时间t的关系如下图所示。

①上图中表示2.0MPa的曲线为_________ (填字母)。
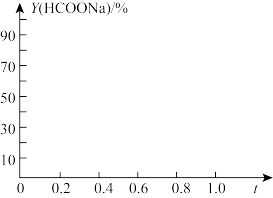
②若1.5MPa时,Y(HCOONa)=87%,则NaOH的转化率为____ 。当CO的初始压强为1.5MPa,保持60℃恒温,不计HCOONa在乙醇中的溶解。在下图中画出Y(HCOONa)与r的关系示意图_____ 。
I:CO(g)+H2O(l)⇌HCOOH(aq) K1 ΔH1
II:HCOOH(aq)+NaOH(aq)⇌HCOONa(s)+H2O(l) K2 ΔH2
III:CO(g)+NaOH(aq)⇌HCOONa(s) K ΔH
回答下列问题:
(1)K=
(2)若需加快反应III的速率,下列措施可行的是
A.增大CO的初始压强 B.适当升高温度 C.减少乙醇浓度 D.降低搅拌转速
(3)CO的压强转化率可以反映羧基化进程。CO的压强转化率可以表示为X(CO)=(1-
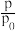 )×100%,p0为CO初始压强,p为CO某时刻分压。HCOONa产率可表示为Y(HCOONa)=
)×100%,p0为CO初始压强,p为CO某时刻分压。HCOONa产率可表示为Y(HCOONa)= ×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成的HCOONa的物质的量。投料比r=
×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成的HCOONa的物质的量。投料比r= ,n0(CO)表示投料CO的物质的量,保持60℃恒温,以投料比r=0.7时,CO初始压强分别为0.5MPa、1.5MPa和2.0MPa,测得X(CO)与时间t的关系如下图所示。
,n0(CO)表示投料CO的物质的量,保持60℃恒温,以投料比r=0.7时,CO初始压强分别为0.5MPa、1.5MPa和2.0MPa,测得X(CO)与时间t的关系如下图所示。
①上图中表示2.0MPa的曲线为
②若1.5MPa时,Y(HCOONa)=87%,则NaOH的转化率为

您最近一年使用:0次



