名校
1 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。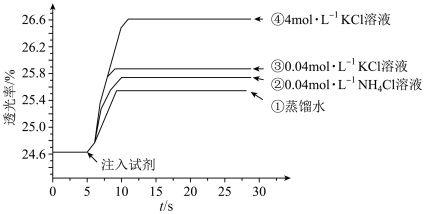
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近一年使用:0次
2023-11-21更新
|
364次组卷
|
7卷引用:北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
名校
2 . 某同学为探究浓度对化学平衡的影响设计了如下实验:已知:
反应i:
反应ii: (黄色)
(黄色)不正确 的是
反应i:

反应ii:
 (黄色)
(黄色)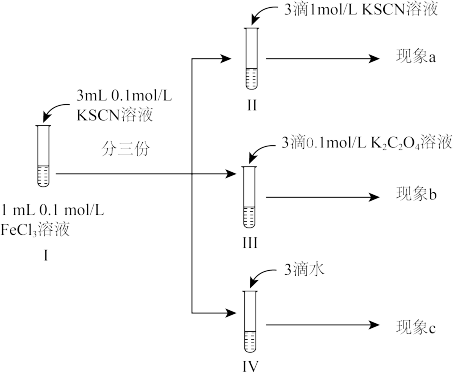
| A.观察到现象a比现象c中红色更深,即可证明增加反应物浓度,反应i平衡正向移动 |
| B.观察到现象b比现象c中红色浅,即可说明反应i平衡逆向移动,反应ⅱ平衡正向移动 |
| C.进行IV对比实验的主要目的是防止出于溶液体积变化引起各离子浓度变化而干扰实验结论得出 |
D.III中溶液一开始无 ,12小时后检出 ,12小时后检出 ,可能的原因是 ,可能的原因是 还原 还原 的速率较慢,反应ⅱ速率较快 的速率较慢,反应ⅱ速率较快 |
您最近一年使用:0次
2023-01-06更新
|
351次组卷
|
4卷引用:北京市昌平区2022-2023学年高二上学期期末考试化学试题
3 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 检验铜和浓硫酸反应之后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入盐酸和BaCl2溶液 | 若出现白色沉淀,则硫酸剩余 |
| B | 探究淀粉在酸性条件下的水解程度 | 取少量淀粉溶液,加入适量稀硫酸加热5min后,再加NaOH中和硫酸,最后滴加碘水 | 溶液无明显现象,则淀粉完全水解 |
| C | 比较CH3COOH和HClO的酸性强弱 | 相同条件下分别用pH试纸测定0.1mol•L-1CH3COONa溶液、0.1mol•L-1NaClO溶液的pH | NaClO溶液pH>CH3COONa溶液的pH,证明CH3COOH的酸性比HClO的酸性强 |
| D | 探究浓度对化学平衡的影响 | 在4mL0.1mol•L-1K2Cr2O7溶液中加入数滴1mol•L-1NaOH溶液 | 若溶液由橙色变为黄色,则H+浓度减小,Cr2O +H2O +H2O 2CrO 2CrO +2H+平衡正移 +2H+平衡正移 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究食用盐是否含碘 | 取粥汤,加入足量食用盐 | 若不变蓝,则不含碘元素 |
| B | 探究火柴头中是否含有 | 火柴头浸泡液中加 溶液和 溶液和 溶液 溶液 | 若有白色沉淀产生则含有 |
| C | 检验乙醇消去反应的产物中有乙烯 | 加热乙醇与 的混合物,将产生的气体通过溴水 的混合物,将产生的气体通过溴水 | 若溴水褪色,则产物中含有乙烯 |
| D | 探究氯化钴溶液的变色原理 | 0.5 溶液中滴入浓盐酸 溶液中滴入浓盐酸 | 若溶液的颜色由蓝色变成粉红色则证明氯化钴溶液中存在平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 某同学研究浓度对化学平衡的影响,下列说法正确的是
已知: (aq)(橙色)+H2O(l) (aq)(橙色)+H2O(l) 2 2 (aq)(黄色)+2H+(aq)∆H=+13.8kJ·mol-1 (aq)(黄色)+2H+(aq)∆H=+13.8kJ·mol-1 | |
步骤: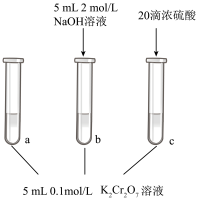 | 现象:待试管b中颜色不变后与试管a比较,溶液颜色变浅。滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深。 |
| A.该反应是一个氧化还原反应 |
B.待试管b中溶液颜色不变的目的是使 完全反应 完全反应 |
| C.对比a、b可以证明减小生成物浓度,平衡正向移动 |
| D.试管c中平衡逆移,该反应的平衡常数增大 |
您最近一年使用:0次
6 . 向锌氨溶液(由 液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂
液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂 。不同
。不同 下(其它条件不变)达到平衡后
下(其它条件不变)达到平衡后 和
和 的萃取效果如图所示。
的萃取效果如图所示。
反应ⅱ:
反应ⅲ:
②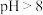 的锌氨溶液中,
的锌氨溶液中,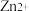 主要以
主要以 形式存在
形式存在
下列说法不正确 的是
 液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂
液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂 。不同
。不同 下(其它条件不变)达到平衡后
下(其它条件不变)达到平衡后 和
和 的萃取效果如图所示。
的萃取效果如图所示。

反应ⅱ:

反应ⅲ:

②
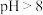 的锌氨溶液中,
的锌氨溶液中,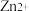 主要以
主要以 形式存在
形式存在下列说法
A.锌氨溶液中存在 的电离平衡和 的电离平衡和 的水解平衡 的水解平衡 |
B. 时,加入萃取剂 时,加入萃取剂 达到平衡后, 达到平衡后,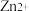 主要以 主要以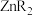 的形式存在 的形式存在 |
C. 由8到10,萃取剂中氨的含量增大的原因是反应ⅲ的平衡向正反应方向移动 由8到10,萃取剂中氨的含量增大的原因是反应ⅲ的平衡向正反应方向移动 |
D. 由8到6, 由8到6, 和 和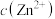 均增大,前者对反应ⅱ的影响小于后者 均增大,前者对反应ⅱ的影响小于后者 |
您最近一年使用:0次
名校
7 . 下列有关对应图像的说法正确的是

A.据①知,某温度下,平衡状态由A变到B时,平衡常数 |
B.据平衡常数的负对数(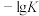 )—温度(T)图像②知,30℃时,B点对应状态的 )—温度(T)图像②知,30℃时,B点对应状态的 |
C.由 的稳定性与溶液pH的关系可知图③中 的稳定性与溶液pH的关系可知图③中 |
D.图④所示体系中气体平均摩尔质量: , , |
您最近一年使用:0次
名校
8 . 在 悬浊液中滴加氨水[浓度以
悬浊液中滴加氨水[浓度以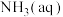 计],存在平衡关系:
计],存在平衡关系:
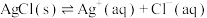 ;
;
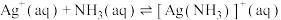 ;
;
 ,
,
平衡常数分别为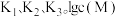 与
与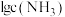 的关系如图所示(其中
的关系如图所示(其中 代表
代表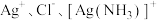 或
或 )。下列说法错误的是
)。下列说法错误的是
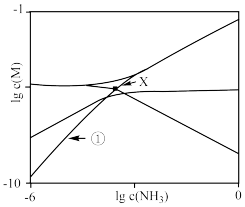
 悬浊液中滴加氨水[浓度以
悬浊液中滴加氨水[浓度以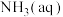 计],存在平衡关系:
计],存在平衡关系: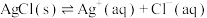 ;
;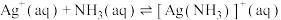 ;
; ,
,平衡常数分别为
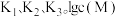 与
与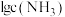 的关系如图所示(其中
的关系如图所示(其中 代表
代表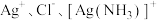 或
或 )。下列说法错误的是
)。下列说法错误的是
A. 时,溶液中 时,溶液中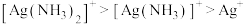 |
B.加入少量 固体后,X点坐标下移 固体后,X点坐标下移 |
C.随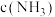 浓度增大, 浓度增大,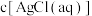 也增大 也增大 |
D.X点对应的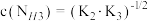 |
您最近一年使用:0次
名校
9 . 以下说法中操作正确、能达到目的且判断正确的是
选项 | 操作 | 目的 | 判断 |
A | 向 | 使 | 错误,根据反应 |
B | 合成氨时在经济性良好的范围内选择尽可能高的压强 | 增加 转化率 转化率 | 正确,压强增大使得反应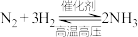 向右进行 向右进行 |
C | 向两支盛有2ml0.2mol/L的乙二酸试管中滴加1ml浓度分别为0.1mol/L和0.2mol/L的 溶液 溶液 | 探究反应物浓度对反应速率的影响 | 正确,浓度越大反应速率越快, 褪色越快 褪色越快 |
D | 向滴有KSCN溶液的 溶液中加入 溶液中加入 固体 固体 | 探究浓度对平衡的影响 | 正确,增加 浓度,使 浓度,使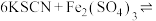 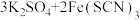 平衡移动 平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 恒温恒容,可逆反应N2O4(g) 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
 2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是
2NO2(g)。充入1molN2O4气体,反应达平衡状态。若再充入1molN2O4气体,下列说法错误的是| A.NO2的体积分数增大 | B.达新平衡后平衡体系压强比原平衡大 |
| C.平衡正向移动 | D.达新平衡后N2O4转化率降低 |
您最近一年使用:0次

 和生石灰混合体系加压
和生石灰混合体系加压 的K的表达式可知,压强增大不能使
的K的表达式可知,压强增大不能使

