以下说法中操作正确、能达到目的且判断正确的是
选项 | 操作 | 目的 | 判断 |
A | 向 | 使 | 错误,根据反应 |
B | 合成氨时在经济性良好的范围内选择尽可能高的压强 | 增加 转化率 转化率 | 正确,压强增大使得反应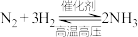 向右进行 向右进行 |
C | 向两支盛有2ml0.2mol/L的乙二酸试管中滴加1ml浓度分别为0.1mol/L和0.2mol/L的 溶液 溶液 | 探究反应物浓度对反应速率的影响 | 正确,浓度越大反应速率越快, 褪色越快 褪色越快 |
D | 向滴有KSCN溶液的 溶液中加入 溶液中加入 固体 固体 | 探究浓度对平衡的影响 | 正确,增加 浓度,使 浓度,使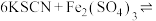 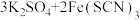 平衡移动 平衡移动 |
| A.A | B.B | C.C | D.D |
更新时间:2024-03-20 11:04:19
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某课题组研究煤燃烧过程中氮氧化物与砷反应的微观机理,得到如下数据和图象。已知:反应速率为反应物浓度和速率常数 的函数,
的函数, 为活化能。对于所研究的三个反应,下列说法错误的是
为活化能。对于所研究的三个反应,下列说法错误的是

 的函数,
的函数, 为活化能。对于所研究的三个反应,下列说法错误的是
为活化能。对于所研究的三个反应,下列说法错误的是反应 |
|
| 78.45 |
| 2.58 |
| 155.85 |

A.相同条件下的氧化性: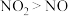 |
| B.相同条件下,As与NO的反应速率最慢 |
C.升高温度能增大As与 反应的活化能 反应的活化能 |
D.其他条件不变,改变温度不能显著改变As与 的反应速率 的反应速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】一定温度下,10mL0.4mol/LH2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:( )
下列叙述错误的是(溶液体积变化忽略不计)
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述错误的是(溶液体积变化忽略不计)
| A.反应至6min时,c(H2O2)=0.20mol/L |
| B.反应至6min时,H2O2分解了40% |
| C.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min) |
| D.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L·min) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知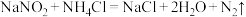 的速率方程为
的速率方程为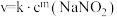 。
。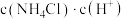 ,为探究反应速率与
,为探究反应速率与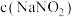 的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L
的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L 
 溶液、2.0 mol⋅L
溶液、2.0 mol⋅L
 溶液、1.0 mol⋅L
溶液、1.0 mol⋅L 醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL
醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL  所需要的时间(t),实验数据如下表。下列说法正确的是
所需要的时间(t),实验数据如下表。下列说法正确的是
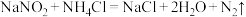 的速率方程为
的速率方程为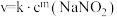 。
。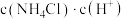 ,为探究反应速率与
,为探究反应速率与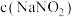 的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L
的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L 
 溶液、2.0 mol⋅L
溶液、2.0 mol⋅L
 溶液、1.0 mol⋅L
溶液、1.0 mol⋅L 醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL
醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL  所需要的时间(t),实验数据如下表。下列说法正确的是
所需要的时间(t),实验数据如下表。下列说法正确的是| 实验 | V/mL | t/s | |||
 溶液 溶液 |  溶液 溶液 | 醋酸 | 水 | ||
| 1 | 4.0 |  | 4.0 | 8.0 | 332 |
| 2 | 6.0 | 4.0 | 4.0 | 6.0 | 148 |
| 3 |  | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 |  | 37 |
A. ; ; |
B.实验3用 表示的反应平均速率 表示的反应平均速率 mol·s mol·s |
| C.醋酸不参与反应,其浓度的大小对该反应速率无影响 |
D.速率方程中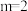 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】室温下,初始浓度为1.0mol·L-1的Na2CrO4溶液中c(Cr2O )随c(H+)的变化如图所示。下列说法正确的是
)随c(H+)的变化如图所示。下列说法正确的是

 )随c(H+)的变化如图所示。下列说法正确的是
)随c(H+)的变化如图所示。下列说法正确的是
| A.随着c(H+)增大,溶液由橙色变为黄色 |
B.由A点可以得出2CrO +2H+=Cr2O +2H+=Cr2O +H2O的K=5×1013 +H2O的K=5×1013 |
C.溶液pH变化过程中c(Na+)=2c(CrO )+4c(Cr2O )+4c(Cr2O ) ) |
D.当溶液pH=7时,c(Na+)=2c(CrO )+2c(Cr2O )+2c(Cr2O ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知反应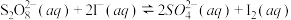 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:
①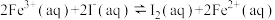
②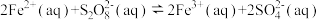
下列说法错误的是
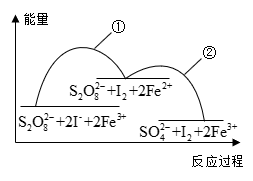
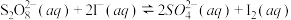 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:①
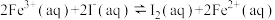
②
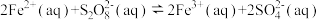
下列说法错误的是

A. 是该反应的催化剂,加入 是该反应的催化剂,加入 后降低了该反应的活化能 后降低了该反应的活化能 |
| B.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
C.步骤①中 和 和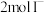 的总能量低于 的总能量低于 和 和 的总能量 的总能量 |
D.增大 浓度或 浓度或 浓度,反应①、反应②的反应速率均加快 浓度,反应①、反应②的反应速率均加快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定量的混合气体,在密闭容器中发生如下反应:xA(g) +yB(g)  zC(g),达到平衡后测得A气体的浓度为lmol • L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.4 mol • L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为lmol • L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.4 mol • L-1,则下列叙述正确的是
 zC(g),达到平衡后测得A气体的浓度为lmol • L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.4 mol • L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为lmol • L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.4 mol • L-1,则下列叙述正确的是| A.平衡向正反应方向移动 | B.A + B  C C |
| C.C的体积分数降低 | D.B的转化率降低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容条件,已知
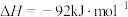 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:
下列说法正确的是

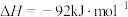 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:容器1 | 容器2 | 容器3 | |
| 反应物投入量 |
|
|
|
|
|
|
|
反应的能量变化 | 放出 | 吸收 | 吸收 |
体系的压强 |
|
|
|
反应物的转化率 |
|
|
|
A.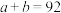 | B. | C. | D.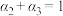 |
您最近一年使用:0次

 和生石灰混合体系加压
和生石灰混合体系加压 的K的表达式可知,压强增大不能使
的K的表达式可知,压强增大不能使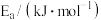

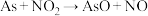

 、
、


 的浓度
的浓度


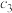
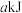
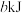
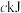








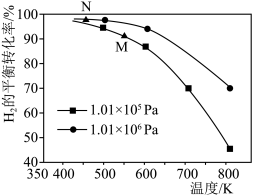
 CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为
CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为 )。下列有关说法正确的是
)。下列有关说法正确的是