已知反应:CO(g)+3H2(g)  CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为
CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为 )。下列有关说法正确的是
)。下列有关说法正确的是
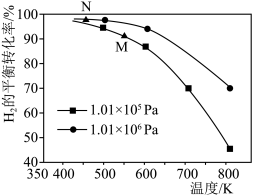
 CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为
CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为 )。下列有关说法正确的是
)。下列有关说法正确的是 
| A.上述反应逆反应的ΔH > 0 |
| B.N点时的反应速率一定比M点的快 |
| C.降低温度,H2的转化率可达到100% |
| D.工业上用此法制取甲烷应采用更高的压强 |
更新时间:2023-04-15 20:56:11
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。在一定条件下,向某0.5L恒容密闭容器中充入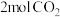 和
和 ,发生反应
,发生反应
 。测得在相同时间内,不同温度下
。测得在相同时间内,不同温度下 的转化率如图1所示,图2表示正、逆反应的速率常数的对数
的转化率如图1所示,图2表示正、逆反应的速率常数的对数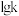 与温度的倒数
与温度的倒数 之间的关系:(已知速率方程
之间的关系:(已知速率方程 ,
,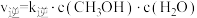 ,k正、k逆是速率常数,只受温度影响),下列说法中错误的是
,k正、k逆是速率常数,只受温度影响),下列说法中错误的是

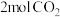 和
和 ,发生反应
,发生反应
 。测得在相同时间内,不同温度下
。测得在相同时间内,不同温度下 的转化率如图1所示,图2表示正、逆反应的速率常数的对数
的转化率如图1所示,图2表示正、逆反应的速率常数的对数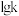 与温度的倒数
与温度的倒数 之间的关系:(已知速率方程
之间的关系:(已知速率方程 ,
,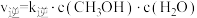 ,k正、k逆是速率常数,只受温度影响),下列说法中错误的是
,k正、k逆是速率常数,只受温度影响),下列说法中错误的是
A. |
B.升高温度, 增大的倍数小于 增大的倍数小于 增大的倍数 增大的倍数 |
C. T2时,起始压强为2.5MPa,20min时达到平衡,若用单位时间内气体的分压的变化来表示反应速率,则0-20min内的平均速率 (分压=总压×物质的量分数) (分压=总压×物质的量分数) |
D.A、B、D、E分别代表图1中a点、c点的正、逆反应的 ,其中点D表示a点的 ,其中点D表示a点的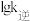 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】向某密闭容器中加入0.6 mol A、0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[其中t0-t1阶段c(B)未画出]。t2时刻后改变条件反应体系中反应速率随时间变化的情况如乙图所示,且四个阶段都各改变一种条件并且改变的条件均不相同。下列说法正确的是( )
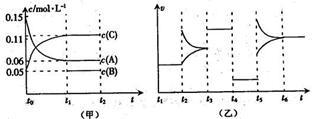

A.反应的方程式为3A(g)+B(g)  2C(g) 2C(g) |
| B.t3~t4,t4~t5,t5~t6各阶段可能改变的条件依次为:加催化剂,降低反应温度,增大压强 |
| C.B的起始物质的量为0.08 mol |
| D.若t1=10 s,A在t0~t1时间段的反应速率为0.00225 mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
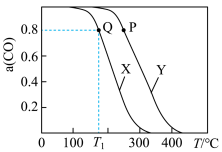
【推荐1】工业上利用CO和 制
制 的反应为
的反应为 。实验测得在两种不同压强下,CO的平衡转化率
。实验测得在两种不同压强下,CO的平衡转化率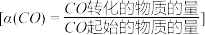 与温度(T)的关系如图所示。查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比。下列说法正确的是
与温度(T)的关系如图所示。查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比。下列说法正确的是
 制
制 的反应为
的反应为 。实验测得在两种不同压强下,CO的平衡转化率
。实验测得在两种不同压强下,CO的平衡转化率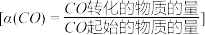 与温度(T)的关系如图所示。查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比。下列说法正确的是
与温度(T)的关系如图所示。查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比。下列说法正确的是
A.反应 的 的 |
| B.图中曲线X所对应的压强大于曲线Y所对应的压强 |
C. ℃, ℃,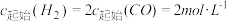 时,平衡常数 时,平衡常数 |
D.图中P点所示条件下,延长反应的时间能提高 转化率 转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反应mX(g)+nY(g) pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
下列说法不正确的是
 pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。容器体积/L c(Y)/(mol·L-1) 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
| A.m+n>p |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】1L恒容密闭容器中充入2molNO和1molCl2反应:2NO(g)+Cl2(g) 2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
 2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是| t/min 温度/℃ | 0 | 5 | 8 | 13 |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
| A.T1>T2 |
| B.T1时,反应前5min的平均速率为v(Cl2)=0.5mol·L-1·min-1 |
| C.反应达平衡时,升高温度促进反应向正反应方向进行 |
| D.T2时,向反应后的容器中充入2molNOCl(g),再次平衡时,c(NOCl)>2mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是

 zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
| A.200℃时,反应从开始到平衡的平均速率v(B)=0.04mol•L﹣1•min﹣1 |
B.图2所知反应xA(g)+yB(g)  zC(g)的△H>0,且a=1 zC(g)的△H>0,且a=1 |
| C.若在图1所示的平衡状态下,再向体系中充入He,此时v正>v逆 |
| D.200℃时,向容器中充入2mol A和1mol B,达到平衡时,A的体积分数小于0.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】CH4和CO2联合重整能减少温室气体的排放。其主要反应为:
①CH4(g)+CO2(g) 2H2(g)+2CO(g)
2H2(g)+2CO(g)
②H2(g)+CO2(g) H2O(g)+CO(g)
H2O(g)+CO(g)
其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。
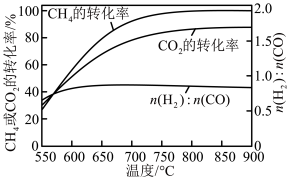
下列说法不正确 的是
①CH4(g)+CO2(g)
 2H2(g)+2CO(g)
2H2(g)+2CO(g)②H2(g)+CO2(g)
 H2O(g)+CO(g)
H2O(g)+CO(g)其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。

下列说法
| A.550~600℃,升温更有利于反应①,反应①先达到平衡 |
| B.n(H2)∶n(CO)始终低于1.0,与反应②有关 |
| C.加压有利于增大CH4和CO2反应的速率但不利于提高二者的平衡转化率 |
| D.若不考虑其他副反应,体系中存在:4[c(CH4)+c(CO)+c(CO2)]=2.3[4c(CH4)+2c(H2)+2c(H2O)] |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】 转化可减少
转化可减少 排放并实现资源利用。
排放并实现资源利用。 催化氧化乙烷制乙烯的主要反应有:
催化氧化乙烷制乙烯的主要反应有:
①:
②:
反应的能量变化如图1所示。体系中还存在其他副反应。相同时间内,乙烷的转化率、乙烯的选择性与温度的关系如图2所示。

已知:乙烯的选择性为转化的乙烷中生成乙烯的百分比,下列说法不正确 的是
 转化可减少
转化可减少 排放并实现资源利用。
排放并实现资源利用。 催化氧化乙烷制乙烯的主要反应有:
催化氧化乙烷制乙烯的主要反应有:①:

②:

反应的能量变化如图1所示。体系中还存在其他副反应。相同时间内,乙烷的转化率、乙烯的选择性与温度的关系如图2所示。

已知:乙烯的选择性为转化的乙烷中生成乙烯的百分比,下列说法
A.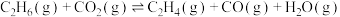  |
| B.反应②比反应①的速率小,是总反应的决速步 |
| C.在图2所画曲线的温度范围内,温度越高,乙烯的产率越低 |
D.其他条件不变,适当增大投料比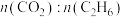 ,能提高 ,能提高 的转化率 的转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】中国从 人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,合成步骤由60多步缩减到11步,突破了自然界淀粉合成的复杂调控障碍。其中
人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,合成步骤由60多步缩减到11步,突破了自然界淀粉合成的复杂调控障碍。其中 加氢的主要反应如下。
加氢的主要反应如下。
反应ⅰ:
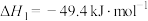
反应ⅱ:

向密闭容器中通入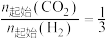 的混合气体,在不同压强(
的混合气体,在不同压强( 、
、 )、不同温度下,平衡体系中
)、不同温度下,平衡体系中 的转化率、
的转化率、 和CO的选择性随温度的变化如图所示。
和CO的选择性随温度的变化如图所示。
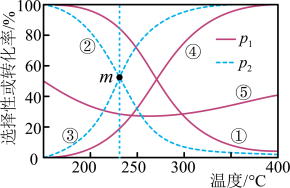
下列说法错误的是
 人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,合成步骤由60多步缩减到11步,突破了自然界淀粉合成的复杂调控障碍。其中
人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,合成步骤由60多步缩减到11步,突破了自然界淀粉合成的复杂调控障碍。其中 加氢的主要反应如下。
加氢的主要反应如下。反应ⅰ:

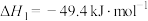
反应ⅱ:


向密闭容器中通入
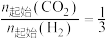 的混合气体,在不同压强(
的混合气体,在不同压强( 、
、 )、不同温度下,平衡体系中
)、不同温度下,平衡体系中 的转化率、
的转化率、 和CO的选择性随温度的变化如图所示。
和CO的选择性随温度的变化如图所示。
下列说法错误的是
A.压强: |
B.曲线①、⑤分别表示平衡体系中 的选择性和 的选择性和 的转化率 的转化率 |
C.235℃时,m点体系中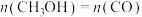 |
D.随着温度升高, 与 与 的平衡转化率之比 的平衡转化率之比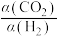 先减小后增大 先减小后增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在某温度下,向三个初始体积均为1L的密闭容器中按下表所示投料,发生反应: 2SO2(g)+O2(g)  2SO3(g) ΔH<0。下列说法不正确的是
2SO3(g) ΔH<0。下列说法不正确的是

 2SO3(g) ΔH<0。下列说法不正确的是
2SO3(g) ΔH<0。下列说法不正确的是

| 容器编号 | 容器类型 | 起始物质的量/mol | 平衡时SO3的 物质的量/mol | ||
| SO2 | O2 | SO3 | |||
| Ⅰ | 恒温恒容 | 2 | 1 | 0 | 1.8 |
| Ⅱ | 绝热恒容 | 0 | 0 | 2 | a |
| Ⅲ | 恒温恒压 | 2 | 1 | 0 | b |
| A.容器Ⅱ中SO3的转化率等于10% |
| B.容器Ⅲ平衡体系中保持容器压强不变,充入0.100mol SO3(g),新平衡后SO3浓度未变 |
| C.平衡时SO3的物质的量:a>1.8、b<1.8 |
| D.若容器Ⅰ中有0.10mol SO2(g)、0.20mol O2(g)和0.100mol SO3(g),则此时v正>v逆 |
您最近一年使用:0次

 )是制备硅烷、多晶硅的重要原料。对于反应
)是制备硅烷、多晶硅的重要原料。对于反应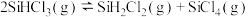 ,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时
,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时
 ,
,

 该反应是放热反应,下列各项对示意图的解释与图像相符的是
该反应是放热反应,下列各项对示意图的解释与图像相符的是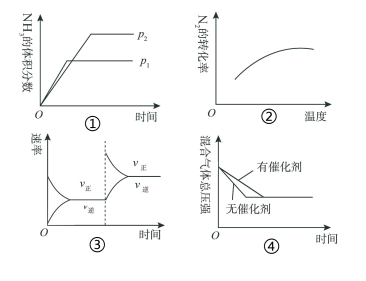
 对反应的影响
对反应的影响

