1 . (1)向盛有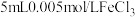 溶液的试管中加入
溶液的试管中加入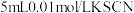 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: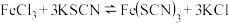
①向上述平衡体系中加入5滴浓的 溶液,溶液颜色
溶液,溶液颜色______ (填“变深”“变浅”或“不变”)。
②向上述平衡体系中加入少量 固体,溶液颜色
固体,溶液颜色______ (填“变深”“变浅”或“不变”)。
(2)氨是一种重要的化工原料,合成氨的反应: ,反应过程如图所示:
,反应过程如图所示:
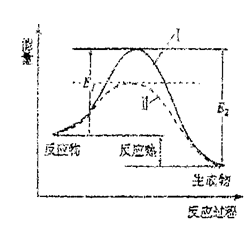
①

______ (用含 、
、 的式子表示)。
的式子表示)。
②加催化剂的曲线______ (填“Ⅰ”或“Ⅱ”)。
③在一定条件下,能说明反应 一定达到平衡的是
一定达到平衡的是______ (填字母代号)。
A.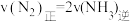
B.单位时间内消耗 的同时消耗
的同时消耗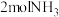
C.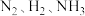 的物质的量之比为
的物质的量之比为
D.混合气体中 保持不变
保持不变
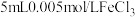 溶液的试管中加入
溶液的试管中加入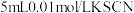 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: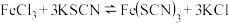
①向上述平衡体系中加入5滴浓的
 溶液,溶液颜色
溶液,溶液颜色②向上述平衡体系中加入少量
 固体,溶液颜色
固体,溶液颜色(2)氨是一种重要的化工原料,合成氨的反应:
 ,反应过程如图所示:
,反应过程如图所示:
①


 、
、 的式子表示)。
的式子表示)。②加催化剂的曲线
③在一定条件下,能说明反应
 一定达到平衡的是
一定达到平衡的是A.
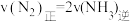
B.单位时间内消耗
 的同时消耗
的同时消耗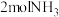
C.
 的物质的量之比为
的物质的量之比为
D.混合气体中
 保持不变
保持不变
您最近一年使用:0次
名校
2 . 在水溶液中,CrO 呈黄色,Cr2O
呈黄色,Cr2O 呈橙红色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙红色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是( )
+2H+,下列说法正确的是( )
 呈黄色,Cr2O
呈黄色,Cr2O 呈橙红色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙红色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是( )
+2H+,下列说法正确的是( )| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应是氧化还原反应 |
| C.向该溶液中通入HCl气体,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
| D.向体系中加入少量水,平衡逆向移动 |
您最近一年使用:0次
2020-11-24更新
|
661次组卷
|
6卷引用:西藏山南第二高级中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
3 . 二氧化氯(ClO2)广泛应用于纸浆漂白、杀菌消毒和水净化处理等领域。工业上利用甲醇还原NaClO3的方法制备ClO2,工艺流程如下:

已知:a.发生器中制备ClO2的反应:12NaClO3+8H2SO4+3CH3OH= 12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2O
b.相关物质的熔沸点:
(1)ClO2可用于纸浆漂白、杀菌消毒是因其具有______ 性。
(2)冷却塔用于分离ClO2并回收CH3OH,应控制的最佳温度为______ (填字母)。
A.0~10℃ B.20~30℃ C.60~70℃
(3)经过程Ⅰ和过程Ⅱ可以获得芒硝(Na2SO4·10H2O)并使部分原料循环利用。
已知:Na2SO4·10H2O和Na2SO4的溶解度曲线如下图:

①Na3H(SO4)2处理器中获得芒硝时需加入NaClO3固体,从芒硝溶解平衡的角度解释其原因:______ 。
②结合Na2SO4·10H2O和Na2SO4的溶解度曲线,过程Ⅱ的操作是:在32.4℃恒温蒸发,______ 。
③Na3H(SO4)2处理器的滤液中可以循环利用的原料是NaClO3和______ 。

已知:a.发生器中制备ClO2的反应:12NaClO3+8H2SO4+3CH3OH= 12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2O
b.相关物质的熔沸点:
| 物质 | CH3OH | HCOOH | ClO2 |
| 熔点/℃ | -97 | 9 | -59 |
| 沸点/℃ | 65 | 101 | 11 |
(1)ClO2可用于纸浆漂白、杀菌消毒是因其具有
(2)冷却塔用于分离ClO2并回收CH3OH,应控制的最佳温度为
A.0~10℃ B.20~30℃ C.60~70℃
(3)经过程Ⅰ和过程Ⅱ可以获得芒硝(Na2SO4·10H2O)并使部分原料循环利用。
已知:Na2SO4·10H2O和Na2SO4的溶解度曲线如下图:

①Na3H(SO4)2处理器中获得芒硝时需加入NaClO3固体,从芒硝溶解平衡的角度解释其原因:
②结合Na2SO4·10H2O和Na2SO4的溶解度曲线,过程Ⅱ的操作是:在32.4℃恒温蒸发,
③Na3H(SO4)2处理器的滤液中可以循环利用的原料是NaClO3和
您最近一年使用:0次
2020-01-12更新
|
738次组卷
|
7卷引用:北京市西城区2020届高三上学期期末考试化学试题
北京市西城区2020届高三上学期期末考试化学试题山东省潍坊市2020届高三下学期第三次线上检测化学试题山东省潍坊五县2019-2020学年高三模拟考试化学试题北京市朝阳区2020届高三4月(一模)适应性试卷练习山东省日照第一中学2021届高三上学期10月份第一次调研考试化学试题辽宁省葫芦岛市2021届高三上学期期末考试化学试题(已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)
19-20高三·江苏苏州·期末
名校
4 . 铁及其化合物在处理工业废水、废气过程中发挥着重要作用。
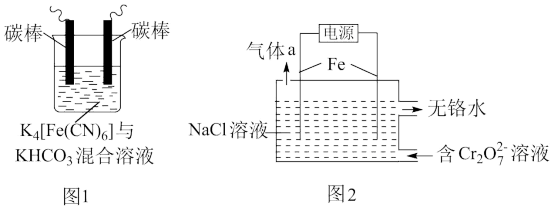
(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为_______ ;电解过程中阴极区溶液的pH_______ (填“变大”、 “变小”或“不变")。
(2)以铁为电极电解除铬,如图2
已知: + H2O=2
+ H2O=2 +2H+
+2H+
氧化性: >
>
①电解过程中主要反应之一: +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是_______ 。
②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是_______ 。
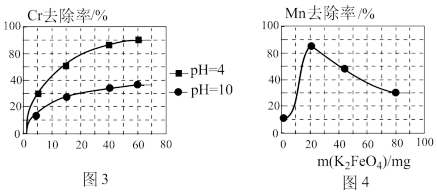
(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式_______ 。
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是_______ 。

(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2
 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为(2)以铁为电极电解除铬,如图2
已知:
 + H2O=2
+ H2O=2 +2H+
+2H+氧化性:
 >
>
①电解过程中主要反应之一:
 +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是

(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是
您最近一年使用:0次
2021-03-25更新
|
449次组卷
|
5卷引用:【苏州新东方】化学试卷
(已下线)【苏州新东方】化学试卷(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)湖北省武汉市蔡甸区汉阳一中2021-2022学年高二上学期12月月考化学试题湖北省武汉市部分重点中学2021-2022学年高二上学期12月联考化学试题江苏省常州市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
5 . 下列事实不能用勒夏特列原理解释的是( )
| A.盛有2mL5%H2O2溶液的试管中加入MnO2作催化剂,试管中迅速产生大量气泡 |
| B.工业合成氨中,将氨气液化分离以提高氨气产率 |
| C.SO2氧化为SO3,使用过量的空气以提高SO2的利用率 |
| D.夏天,打开啤酒瓶时会从瓶口逸出泡沫 |
您最近一年使用:0次
2020-11-23更新
|
595次组卷
|
7卷引用:福建省南平市高级中学2020-2021学年高二上学期期中考试化学(选考)试题
名校
解题方法
6 . 对于已达平衡的下列反应
2HI(g)⇌H2(g)+I2(g) ①
2NO2⇌N2O4 ②
2NH3(g)⇌N2(g)+3H2(g) ③
(1)保持容器容积不变,再通入一定量的反应物,反应①反应物的转化率_______ 反应②的转化率_______ (填增大、减小、不变,下同)。
(2)保持压强不变,通入一定量的N2O4,反应②生成物的百分含量_______
(3)保持容器容积不变,通入一定量氖气,则达到平衡时反应②NO2转化率_______
(4)保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时反应③NH3百分含量_____ 。
2HI(g)⇌H2(g)+I2(g) ①
2NO2⇌N2O4 ②
2NH3(g)⇌N2(g)+3H2(g) ③
(1)保持容器容积不变,再通入一定量的反应物,反应①反应物的转化率
(2)保持压强不变,通入一定量的N2O4,反应②生成物的百分含量
(3)保持容器容积不变,通入一定量氖气,则达到平衡时反应②NO2转化率
(4)保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时反应③NH3百分含量
您最近一年使用:0次
7 . 在水溶液中,CrO 呈黄色,Cr2O
呈黄色,Cr2O 呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是( )
+2H+,下列说法正确的是( )
 呈黄色,Cr2O
呈黄色,Cr2O 呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是( )
+2H+,下列说法正确的是( )| A.向该溶液中滴加适量的NaHSO4固体,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
| B.该反应是氧化还原反应 |
| C.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色 |
| D.向体系中加入少量水,平衡逆向移动 |
您最近一年使用:0次
2021-01-06更新
|
425次组卷
|
5卷引用:安徽涡阳县育萃中学2020-2021学年高二上学期第三次月考化学试题
安徽涡阳县育萃中学2020-2021学年高二上学期第三次月考化学试题(已下线)2020年天津卷化学高考真题变式题1-12安徽省滁州市定远县育才学校2020-2021学年高二下学期开学考试化学试题(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
名校
8 . 下列说法正确的是
A.对于A(s)+B(g)  C(g)+D(g)的反应,加入A,反应速率加快 C(g)+D(g)的反应,加入A,反应速率加快 |
B.2NO2 N2O4(正反应放热),升高温度,v(正)增大,v(逆)减小 N2O4(正反应放热),升高温度,v(正)增大,v(逆)减小 |
C.一定温度下,反应 N2(g)+3H2(g)  2NH3(g)在密闭容器中进行,恒压,充入He不改变化学反应速率 2NH3(g)在密闭容器中进行,恒压,充入He不改变化学反应速率 |
| D.100 mL2 mol·L—1稀盐酸与锌反应时,加入少量硫酸铜固体,生成氢气的速率加快 |
您最近一年使用:0次
2018-08-19更新
|
1416次组卷
|
11卷引用:湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题
湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题广西壮族自治区贺州市平桂区平桂高级中学2019届高三摸底考试化学试题【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题河北省唐山市海港高级中学2019-2020学年高一下学期第五次校考化学试题河北省衡水市第十三中学2019-2020学年高一下学期调研考试化学试题内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题天津市第一中学2020-2021学年高一下学期期中考试化学试题浙江省桐庐分水高级中学2020-2021学年高一下学期第一次月考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题天津市部分重点校2022~2023学年高一下学期期中联考化学试题天津市和平区第五十五中学2022-2023学年高一下学期期中化学试试题
名校
9 . 一定温度下,反应 N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )| A.缩小体积使压强增大 | B.升高体系的温度 |
| C.恒容,充入He | D.加入合适的催化剂 |
您最近一年使用:0次
2019-10-13更新
|
903次组卷
|
8卷引用:甘肃省武威市第六中学2019-2020学年高二上学期第一次学段考试化学试题
名校
10 . 痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理为:
 。下列说法
。下列说法
| A.饮食中摄入过多食盐,会加重痛风病病情 | B.大量饮水会增大痛风病发作的可能性 |
| C.寒冷季节更易诱发关节疼痛 | D.患痛风病的人应少吃能代谢产生更多尿酸的食物 |
您最近一年使用:0次
2024-02-21更新
|
157次组卷
|
41卷引用:北京市西城区2019-2020学年度高二上学期期末考试化学试题
北京市西城区2019-2020学年度高二上学期期末考试化学试题上海市奉贤区2020届高三5月教学质量调研(二模)化学试题湖北省黄冈市麻城市实验高中2020-2021学年高二上学期10月月考化学试题江西省赣州市南康中学2020-2021学年高二上学期第二次大考化学试题内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第三次月考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题辽宁省葫芦岛市2020-2021学年高二上学期期末考试化学试题北京市房山区2020-2021学年高二上学期期末考试化学试题河南省焦作市县级重点中学2021-2022学年高二上学期期中考试化学试题吉林省长白山第二高级中学校2021-2022学年高三上学期第二次月考化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题北京市顺义区杨镇第一中学2021-2022学年高二上学期期中考试化学试题 北京市房山区2022-2023学年高二上学期期中质量检测化学试题北京市第七中学2022-2023学年高二上学期期中化学试题北京市顺义区杨镇第一中学2022-2023学年高二上学期期中检测化学试题广东省信宜市第二中学2022-2023学年高二上学期11月月考化学试题广东省珠海市实验中学2022-2023学年高二上学期第一次段考化学试题北京市顺义区2023届高三第一次统练化学试题广东省汕头市聿怀中学2022-2023学年高二上学期期末线上考试化学试题安徽省宣城市2022-2023学年高二上学期期末调研考试化学试题广东省河源市龙川县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题15 化学反应速率和化学平衡新疆乌鲁木齐市第四中学2022-2023学年高二下学期期中阶段诊断测试化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)云南省玉溪师范学院附属中学2022-2023学年高二下学期期末考试化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期11月期中检测化学试题北京市清华大学附属中学2023-2024学年高二上学期期中考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题黑龙江省哈尔滨市第三十二中学校2023-2024学年高二上学期11月期中考试化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷北京市第一六六中学2022-2023学年高二上学期期中考试化学试卷北京师范大学第二附属中学2023-2024学年高二上学期期中考试化学试题浙江省宁波三锋教研联盟2023-2024学年高二上学期期中联考化学试题河南省信阳市淮滨县2022-2023学年高二上学期11月期中考试化学试题甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题四川省内江市2025届第三中学高二上学期化学试卷北京市北京师范大学附属中学平谷第一分校2023-2024学年高二上学期期中考试化学试题北京市顺义区2022-2023学年高三上学期第一次统练化学试卷



