名校
解题方法
1 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 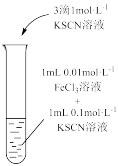 | 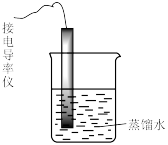 分别测定20℃和80℃蒸馏水的电导率 | 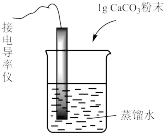 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在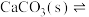  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-06更新
|
933次组卷
|
13卷引用:北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题
北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题北京市第五十中学2023-2024学年高二上学期12月月考化学试题北京交通大学附属中学第二分校2023-2024学年高二上学期12月月考化学试题北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题河南省濮阳市第一高级中学2022-2023学年高二下学期期中质量检测化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题天津市部分区2023-2024学年高二上学期期末练习化学试题
2 . 甲醇是重要的化上原料,研究甲醇的制备及用途在工业上有重要的意义。回答下列问题:
(1)一种重要的工业制备甲醇的反应为
 。
。
已知:①

②
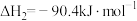
该制备反应的
______ 。升高温度,该制备反应的 的平衡转化率
的平衡转化率______ (填“增大”“减小”或“不变”)。
(2)已知反应 的
的 ,
, ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
在540K下,按初始投料比 、
、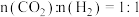 、
、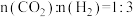 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
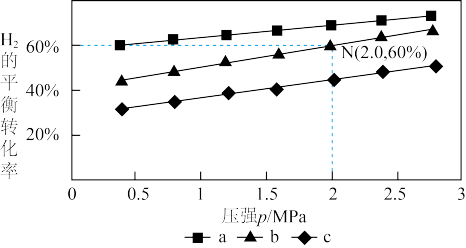
①a、b、c各曲线所表示的投料比由大到小的顺序为______ (用字母表示)。
②N点在b曲线上,540K时的压强平衡常数
______  (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻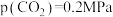 ,
, ,
,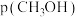
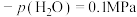 ,此时
,此时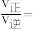
______ (保留两位小数)。
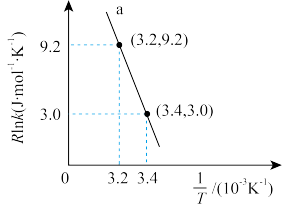
(3)甲醇催化可制取丙烯,反应为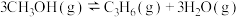 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能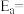
______  。
。
(4)Kistiakowsky曾研究了NOCl光化学分解反应。在一定频率(v)光的照射下,反应的机理为:
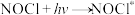

其中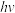 表示一个光子能量,
表示一个光子能量, 表示NOCl的激发态。则吸收1mol光子可分解
表示NOCl的激发态。则吸收1mol光子可分解______ mol NOCl。
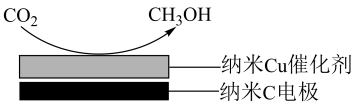
(5)在饱和 电解液中,电解活化的
电解液中,电解活化的 也可以制备
也可以制备 ,其原理如图所示,则阴极的电极反应式为
,其原理如图所示,则阴极的电极反应式为______ 。
(1)一种重要的工业制备甲醇的反应为

 。
。已知:①


②

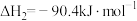
该制备反应的

 的平衡转化率
的平衡转化率(2)已知反应
 的
的 ,
, ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。
分别为正、逆反应速率常数,p为气体分压(分压=总压/物质的量分数)。在540K下,按初始投料比
 、
、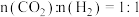 、
、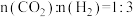 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
①a、b、c各曲线所表示的投料比由大到小的顺序为
②N点在b曲线上,540K时的压强平衡常数

 (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。③540K条件下,某容器测得某时刻
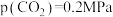 ,
, ,
,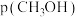
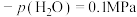 ,此时
,此时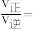
(3)甲醇催化可制取丙烯,反应为
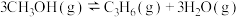 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能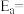
 。
。
(4)Kistiakowsky曾研究了NOCl光化学分解反应。在一定频率(v)光的照射下,反应的机理为:
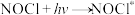

其中
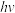 表示一个光子能量,
表示一个光子能量, 表示NOCl的激发态。则吸收1mol光子可分解
表示NOCl的激发态。则吸收1mol光子可分解(5)在饱和
 电解液中,电解活化的
电解液中,电解活化的 也可以制备
也可以制备 ,其原理如图所示,则阴极的电极反应式为
,其原理如图所示,则阴极的电极反应式为
您最近一年使用:0次
3 . 周期表中ⅡA族元素及其化合物应用广泛。铍及其化合物的性质与铝十分相似;工业上以氯化镁为原料制取金属镁;CaS可用于制杀虫剂、发光漆等,CaS与酸反应可以释放出 。硫酸钡用于制造钡盐等,医学上可用于胃肠道造影剂。
。硫酸钡用于制造钡盐等,医学上可用于胃肠道造影剂。 用作供氧剂、氧化剂、漂白剂、消毒剂等。下列说法正确的是
用作供氧剂、氧化剂、漂白剂、消毒剂等。下列说法正确的是
 。硫酸钡用于制造钡盐等,医学上可用于胃肠道造影剂。
。硫酸钡用于制造钡盐等,医学上可用于胃肠道造影剂。 用作供氧剂、氧化剂、漂白剂、消毒剂等。下列说法正确的是
用作供氧剂、氧化剂、漂白剂、消毒剂等。下列说法正确的是| A.实验测得氯化铍的水溶液能导电,说明氯化铍是离子化合物 |
B.反应 能自发进行,说明该反应的 能自发进行,说明该反应的 |
C.向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅,说明 固体,溶液红色变浅,说明 溶液显酸性 溶液显酸性 |
D.反应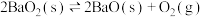 达平衡后,压缩容器体积,反应达新平衡时, 达平衡后,压缩容器体积,反应达新平衡时,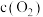 不变,说明平衡没有移动 不变,说明平衡没有移动 |
您最近一年使用:0次
名校
解题方法
4 . 中科院设计并完成了 催化氧化
催化氧化 制取
制取 的新路径,其主要反应为:
的新路径,其主要反应为:
反应I:

反应II: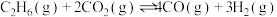

一定条件下,向容积为0.5L的容器中通入2.5mol 和5mol
和5mol ,若仅考虑上述反应,
,若仅考虑上述反应, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度、压强的关系如图所示,
的选择性随温度、压强的关系如图所示, 、
、 代表不同压强下乙烷的平衡转化率。
代表不同压强下乙烷的平衡转化率。
已知: 的选择性
的选择性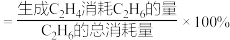
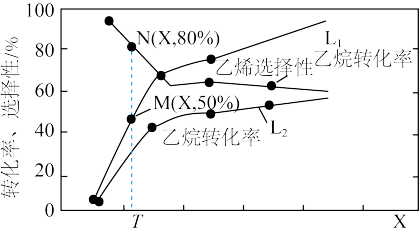
下列说法正确的是
 催化氧化
催化氧化 制取
制取 的新路径,其主要反应为:
的新路径,其主要反应为:反应I:


反应II:
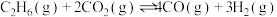

一定条件下,向容积为0.5L的容器中通入2.5mol
 和5mol
和5mol ,若仅考虑上述反应,
,若仅考虑上述反应, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度、压强的关系如图所示,
的选择性随温度、压强的关系如图所示, 、
、 代表不同压强下乙烷的平衡转化率。
代表不同压强下乙烷的平衡转化率。已知:
 的选择性
的选择性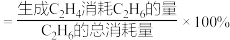

下列说法正确的是
A.压强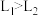 |
B.压强为 温度为T时,反应I平衡常数K为0.5 温度为T时,反应I平衡常数K为0.5 |
C.压强为 、温度为T时,反应达平衡时,混合气体中 、温度为T时,反应达平衡时,混合气体中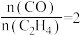 |
D.一定温度下,增大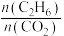 可提高 可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
名校
解题方法
5 . 某反应4A(g)⇌mB(g)+2C(g) ΔH<0,正反应速率的变化如图。其中t1、t2、t3、t4只改变一个条件,t2时刻图像变化并非加入催化剂引起,下列叙述中错误 的是


| A.m=2 | B.t1时增大了A的浓度 |
| C.t3时降低了温度 | D.t1至t4时间段内,化学平衡常数的值保持不变 |
您最近一年使用:0次
2022-12-02更新
|
441次组卷
|
2卷引用:黑龙江省虎林市高级中学2022-2023学年高二9月月考化学试题
名校
6 . 一定温度下,在三个容积均为 的恒容密闭容器中进行反应:
的恒容密闭容器中进行反应: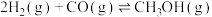 ,并达到平衡。下列说法正确的是
,并达到平衡。下列说法正确的是
 的恒容密闭容器中进行反应:
的恒容密闭容器中进行反应: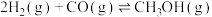 ,并达到平衡。下列说法正确的是
,并达到平衡。下列说法正确的是| 容器 | 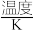 |  | 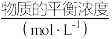 | ||
 |  | 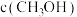 |  | ||
| I | 400 | 0.20 | 0.10 | 0 | 0.080 |
| II | 400 | 0.40 | 0.20 | 0 | |
| III | 500 | 0 | 0 | 0.10 | 0.025 |
| A.该反应的正反应吸热 |
| B.达到平衡时,容器I中反应物转化率比容器II中的大 |
C.达到平衡时,容器II中 大于容器I中 大于容器I中 的两倍 的两倍 |
| D.达到平衡时,容器III中的正反应速率比容器I中的大 |
您最近一年使用:0次
2022-11-29更新
|
209次组卷
|
2卷引用:河南省安阳市第三十九中学2022-2023学年高二上学期第二次考试化学试题
名校
解题方法
7 . 下列说法不正确的是
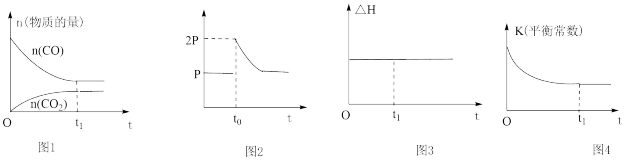

A.图1可表示将一定量的CO和NO通入刚性容器发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 |
| B.图2可表示反应CaCO3(s)=CaO(s)+CO2(g),在t0时刻将容器的体积缩小为原来的一半后再次平衡的过程中压强随时间的变化关系 |
| C.图3可表示反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH与时间的变化关系,且t1时候不一定达到平衡 |
D.图4可表示在绝热容器中充入一定量的A和B,发生反应mA(g)+nB(g) pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 |
您最近一年使用:0次
2022-11-22更新
|
294次组卷
|
2卷引用:陕西省咸阳市实验中学 2022-2023学年高二上学期第三次月考化学试题
名校
解题方法
8 . 工业上利用 和
和 制
制 的反应为
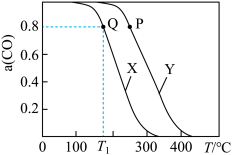
的反应为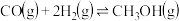 ,实验测得在两种不同压强下,
,实验测得在两种不同压强下, 的平衡转化率
的平衡转化率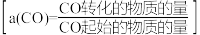 与温度(T)的关系如图所示,查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比,下列说法正确的是
与温度(T)的关系如图所示,查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比,下列说法正确的是
 和
和 制
制 的反应为
的反应为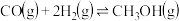 ,实验测得在两种不同压强下,
,实验测得在两种不同压强下, 的平衡转化率
的平衡转化率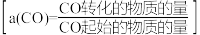 与温度(T)的关系如图所示,查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比,下列说法正确的是
与温度(T)的关系如图所示,查阅资料得:相同压强下,气体的分子数之比等于气体的体积之比,下列说法正确的是
A.反应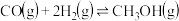 的 的 |
| B.图中曲线X所对应的压强大于曲线Y所对应的压强 |
C.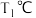 , ,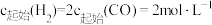 时,平衡常数 时,平衡常数 |
| D.图中P点所示条件下,延长反应的时间能提高CO转化率 |
您最近一年使用:0次
2022-11-19更新
|
280次组卷
|
3卷引用:江苏省南通市如东县2022-2023学年高二上学期10月月考化学试题
9 . 2molSO2和1molO2在一定条件反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。若恒温恒容条件下SO2的转化率为a%;恒温恒压条件下SO2的转化率为b%;恒容绝热条件下SO2的转化率为c%;则它们之间的关系是
| A.a% > b%> c% | B.b%> a% >c% | C.a% >c% > b% | D.b%> c% >a% |
您最近一年使用:0次
名校
10 . 在一定温度下的密闭容器中发生反应: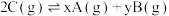 ,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
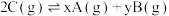 ,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是
,平衡时测得A的浓度为0.50mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断不正确的是A.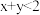 | B.平衡向正反应方向移动 |
| C.C的转化率增大 | D.B的体积分数增大 |
您最近一年使用:0次
2022-10-29更新
|
284次组卷
|
3卷引用:广东省江门市蓬江区棠下中学2022-2023学年高二上学期第一次月考化学试题



