1 . 为减少碳氧化物的排放,工业上可回收 和
和 合成甲醇(
合成甲醇( )。
)。
(1)利用 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:
反应Ⅰ
反应Ⅱ
控制 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
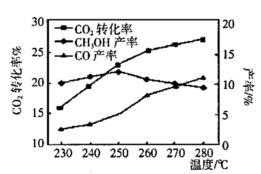
①反应Ⅰ能自发的反应条件:______ 。(填“低温”、“高温”、“任何温度”)
②由图可知温度升高 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是______ 。
③由图可知获取 最适宜的温度是
最适宜的温度是______ 。
④控制 和
和 初始投料比为
初始投料比为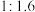 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为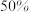 ,甲醇选择性为
,甲醇选择性为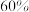 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是______ 。(甲醇的选择性:转化的 中生成甲醇的百分比)
中生成甲醇的百分比)
(2)利用 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:
反应Ⅲ
其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是______ 。
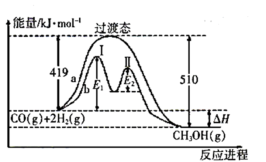
A. 上述反应的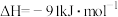
B. 反应正反应的活化能为
反应正反应的活化能为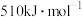
C. 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D. 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E. 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入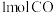 和
和 ,向乙中加入
,向乙中加入 和
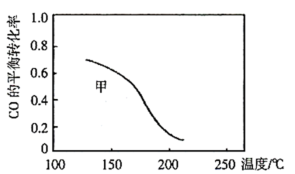
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线______ 。
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式______ 。
 和
和 合成甲醇(
合成甲醇( )。
)。(1)利用
 和
和 反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应:反应Ⅰ

反应Ⅱ

控制
 和
和 初始投料比为
初始投料比为 ,温度对
,温度对 平衡转化率及甲醇和
平衡转化率及甲醇和 产率的影响如图所示:
产率的影响如图所示:
①反应Ⅰ能自发的反应条件:
②由图可知温度升高
 的产率上升,其主要原因可能是
的产率上升,其主要原因可能是③由图可知获取
 最适宜的温度是
最适宜的温度是④控制
 和
和 初始投料比为
初始投料比为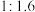 ,在
,在 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态, 的转化率为
的转化率为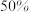 ,甲醇选择性为
,甲醇选择性为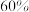 ,此时容器的体积为
,此时容器的体积为 ,若
,若 初始加入量为
初始加入量为 ,则反应Ⅰ的平衡常数是
,则反应Ⅰ的平衡常数是 中生成甲醇的百分比)
中生成甲醇的百分比)(2)利用
 和
和 在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应:反应Ⅲ

其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是

A. 上述反应的
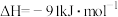
B.
 反应正反应的活化能为
反应正反应的活化能为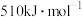
C.
 过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应D.
 过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和
E.
 过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段(3)甲和乙两个恒容密闭容器的体积相同,向甲中加入
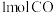 和
和 ,向乙中加入
,向乙中加入 和
和 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中 的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中 的平衡转化率变化趋势的曲线
的平衡转化率变化趋势的曲线
(4)反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式
您最近一年使用:0次
名校
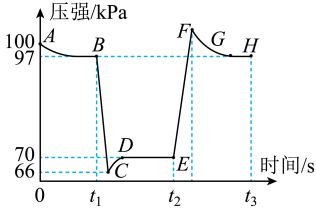
2 . 利用现代传感技术探究压强对 2NO2(g)  N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
 N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的 NO2气体后密封并保持活塞位置不变。分别在 t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列分析中不正确的是
| A.t1时移动活塞,使容器体积增大 |
| B.在 B、E 两点,对应的正反应速率:v(B)>v(E) |
| C.图中除 A、C、F 点外,其他点均为平衡状态 |
| D.在 E,F,H 三点中,H 点的气体平均相对分子质量最大 |
您最近一年使用:0次
2021-01-11更新
|
560次组卷
|
3卷引用:湖南省株洲市2021届高三教学质量统一检测(一)化学试题
湖南省株洲市2021届高三教学质量统一检测(一)化学试题湖南师范大学附属中学2022届高三月考(七)化学试题(已下线)专题09 化学反应速率与化学平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)
名校
解题方法
3 . 某密闭容器内,可逆反应2X(?) ⇌ Y(g)+Z(s)达到平衡。则有
| A.恒容时升高温度,气体的密度增大,X一定为非气态物质 |
| B.恒温时缩小容积,气体的相对平均分子量有可能不变 |
| C.恒温恒容时,加入少量Z,则平衡向左移动 |
| D.恒温恒容时催化剂加入,Z的质量会增加 |
您最近一年使用:0次
2020-12-31更新
|
336次组卷
|
4卷引用:上海市奉贤区2021届高三一模化学试卷
上海市奉贤区2021届高三一模化学试卷上海市行知中学2021届高三下学期3月月考化学试题(已下线)第七章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)练习8 化学平衡的移动-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)
解题方法
4 . CH4和CO2在催化剂作用下反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)-247kJ完成下列填空:
2CO(g)+2H2(g)-247kJ完成下列填空:
(1)有利于提高CH4平衡转化率的措施是___ (任写两条)。
(2)该反应温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:___ 。
(3)CH4和CO2各1mol充入密闭容器中,发生上述反应。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=___ 。
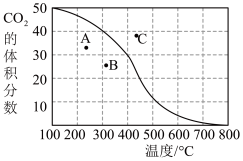
②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数,___ 点对应的平衡常数最小,理由是:___ ;___ 点对应压强最大,理由是:___ 。
(4)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应又使积碳量减少:
积碳反应:CH4(g) C(s)+2H2(g)-75kJ
C(s)+2H2(g)-75kJ
消碳反应:CO2(g)+C(s) 2CO(g)-172kJ
2CO(g)-172kJ
一定时间内,积碳量和反应温度的关系如图所示。
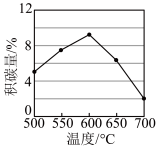
①一定温度,增大CO2的浓度有助于减少积碳,其原因是:___ 。
②温度高于600℃,积碳量减少的可能原因是:___ (任写一条)。
 2CO(g)+2H2(g)-247kJ完成下列填空:
2CO(g)+2H2(g)-247kJ完成下列填空:(1)有利于提高CH4平衡转化率的措施是
(2)该反应温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:
(3)CH4和CO2各1mol充入密闭容器中,发生上述反应。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=

②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数,
(4)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应又使积碳量减少:
积碳反应:CH4(g)
 C(s)+2H2(g)-75kJ
C(s)+2H2(g)-75kJ消碳反应:CO2(g)+C(s)
 2CO(g)-172kJ
2CO(g)-172kJ一定时间内,积碳量和反应温度的关系如图所示。

①一定温度,增大CO2的浓度有助于减少积碳,其原因是:
②温度高于600℃,积碳量减少的可能原因是:
您最近一年使用:0次
2020-12-30更新
|
269次组卷
|
2卷引用:上海市杨浦区2021届高三一模化学试卷
名校
5 . 如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法正确的是( )
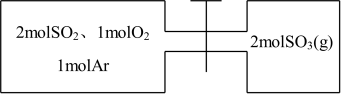

| A.第一次平衡时,SO2的物质的量左室更多 |
| B.充入气体未反应前,左室压强比右室大 |
| C.第一次平衡时,左室内压强一定小于右室 |
| D.第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多 |
您最近一年使用:0次
2020-11-26更新
|
398次组卷
|
6卷引用:内蒙古赤峰市2018届高三4月模拟理科综合化学试题
名校
6 . 一定温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5 (g)  PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol·L-1) | 物质的平衡浓度/(mol·L-1) | ||
 | 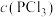 | 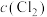 | 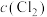 | |
| Ⅰ | 0.4 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0 | 0.2 | |
| Ⅲ | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中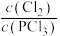 比容器Ⅱ中的小 比容器Ⅱ中的小 |
| B.反应达到平衡时,容器I与容器Ⅱ中的总压强之比为3︰4 |
C.反应达到平衡时,容器Ⅲ中 的体积分数小于 的体积分数小于 |
| D.反应达到平衡时,容器Ⅲ中0.4mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次
2020-09-29更新
|
725次组卷
|
6卷引用:江西省赣州市会昌县七校2021届高三联合9月月考化学试题
7 . 二甲醚(CH3OCH3)是制冷剂、局部麻醉药和燃料。工业上可利用CO2催化加氢合成二甲醚,其过程中主要发生下列反应:
反应I:CO2(g)+H2(g) CO(g)+H2O(g) △H1>0
CO(g)+H2O(g) △H1>0
反应II:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H2<0
CH3OCH3(g)+3H2O(g) △H2<0
一定条件下,于密闭容器中投入一定量CO2和H2发生上述反应。下列说法正确的是
反应I:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1>0
CO(g)+H2O(g) △H1>0反应II:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H2<0
CH3OCH3(g)+3H2O(g) △H2<0一定条件下,于密闭容器中投入一定量CO2和H2发生上述反应。下列说法正确的是
| A.其他条件不变,升高温度CO2的平衡转化率降低 |
| B.其他条件不变,缩小容器体积能提高CH3OCH3平衡产率 |
| C.其他条件不变,增大H2投入量一定能提高CH3OCH3平衡产率 |
| D.其他条件不变,使用不同催化剂对CH3OCH3的平衡产率不产生影响 |
您最近一年使用:0次
名校
解题方法
8 . 运用化学链燃烧技术有利于提高燃料利用率。化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3、FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
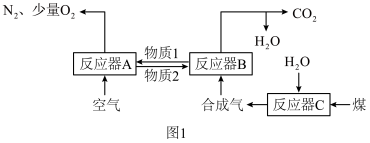
以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:_____
(2)空气经反应器A后得到的尾气_____ (填“能”或“不能”)直接用作工业合成氨的原料气,原因是_____ 。
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。
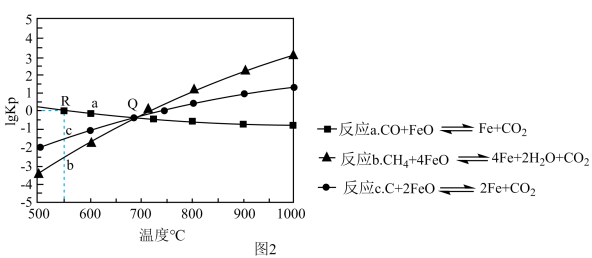
(3)图2涉及的反应中,属于吸热反应的是反应_____ (填字母)。
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为_____ 。
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=_____ 。
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向_____ (填“正反应”或“逆反应”)方向进行。
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率_____ (填“增大”“减小”或“不变”)。

以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图1所示。
①C(s)+H2O(g)═CO(g)+H2(g)△H1=akJ•mol﹣1
②CO(g)+H2(g)+O2(g)═CO2(g)+H2O(g)△H2=bkJ•mol﹣1
(1)写出图1中总反应的热化学方程式:
(2)空气经反应器A后得到的尾气
Ⅱ.用FeO作载氧剂,部分反应的lgKp[K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图2所示。

(3)图2涉及的反应中,属于吸热反应的是反应
(4)R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应CO(g)+FeO(s)⇌Fe(s)+CO2(g),则CO的平衡转化率为
Ⅲ.在T℃下,向某恒容密闭容器中加入1mol CH4(g)和4mol FeO(s)进行反应:CH4(g)+4FeO(s)⇌4Fe(s)+2H2O(g)+CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp=
(6)若起始时向该容器中加入1mol CH4(g),4mol FeO(s),1mol H2O(g),0.5mol CO2(g),此时反应向
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4(g)的平衡转化率
您最近一年使用:0次
2020-07-23更新
|
292次组卷
|
5卷引用:云南省昆明市第一中学2020届高三上学期12月月考理综试卷化学试题
名校
解题方法
9 . 三氧化钼( )是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为
)是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为 )通过一定条件来制备。回答下列相关问题:
)通过一定条件来制备。回答下列相关问题:
⑴已知:①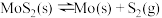

②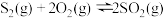

③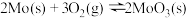

则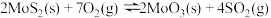 的
的
________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
⑵若在恒温恒容条件下,仅发生反应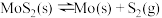 。
。
①下列说法正确的是________ (填字母)。
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加 的量,平衡正向移动
的量,平衡正向移动
②达到平衡时 的浓度为1.4 mol·L−1,充入一定量的
的浓度为1.4 mol·L−1,充入一定量的 ,反应再次达到平衡,
,反应再次达到平衡, 浓度
浓度________ (填“ ”“
”“ ”或“
”或“ ”) 1.4 mol·L−1。
”) 1.4 mol·L−1。
⑶在 恒容密闭容器中充入
恒容密闭容器中充入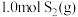 和
和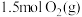 ,若仅发生反应:
,若仅发生反应: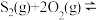
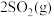 ,
,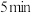 后反应达到平衡,此时容器压强为起始时的80%,则
后反应达到平衡,此时容器压强为起始时的80%,则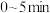 内,
内, 的反应速率为
的反应速率为________  。
。
⑷在恒容密闭容器中,加入足量的 和
和 ,仅发生反应:
,仅发生反应: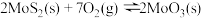

 。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
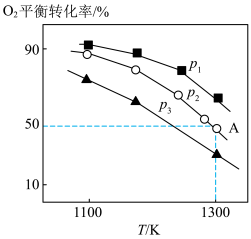
①
________ (填“ ”“
”“ ”或“
”或“ ”)0;比较
”)0;比较 、
、 、
、 的大小:
的大小:________ 。
②若初始时通入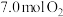 ,
, 为
为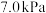 ,则
,则 点平衡常数
点平衡常数
________ (用气体平衡分压代替气体平衡浓度计算,分压 总压
总压 气体的物质的量分数,写出计算式即可)。
气体的物质的量分数,写出计算式即可)。
 )是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为
)是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为 )通过一定条件来制备。回答下列相关问题:
)通过一定条件来制备。回答下列相关问题:⑴已知:①
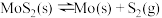

②
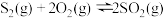

③
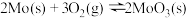

则
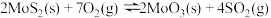 的
的
 、
、 、
、 的代数式表示)。
的代数式表示)。⑵若在恒温恒容条件下,仅发生反应
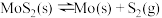 。
。①下列说法正确的是
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加
 的量,平衡正向移动
的量,平衡正向移动②达到平衡时
 的浓度为1.4 mol·L−1,充入一定量的
的浓度为1.4 mol·L−1,充入一定量的 ,反应再次达到平衡,
,反应再次达到平衡, 浓度
浓度 ”“
”“ ”或“
”或“ ”) 1.4 mol·L−1。
”) 1.4 mol·L−1。⑶在
 恒容密闭容器中充入
恒容密闭容器中充入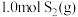 和
和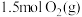 ,若仅发生反应:
,若仅发生反应: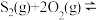
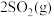 ,
,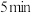 后反应达到平衡,此时容器压强为起始时的80%,则
后反应达到平衡,此时容器压强为起始时的80%,则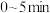 内,
内, 的反应速率为
的反应速率为 。
。⑷在恒容密闭容器中,加入足量的
 和
和 ,仅发生反应:
,仅发生反应: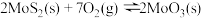

 。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
①

 ”“
”“ ”或“
”或“ ”)0;比较
”)0;比较 、
、 、
、 的大小:
的大小:②若初始时通入
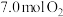 ,
, 为
为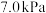 ,则
,则 点平衡常数
点平衡常数
 总压
总压 气体的物质的量分数,写出计算式即可)。
气体的物质的量分数,写出计算式即可)。
您最近一年使用:0次
2020-06-11更新
|
353次组卷
|
5卷引用:云南省楚雄彝族自治州2020届高三上学期期末考试理综化学试题
云南省楚雄彝族自治州2020届高三上学期期末考试理综化学试题陕西省2020届高三3月线上联考理综化学试题吉林省白山市2020届高三二模理综化学试卷(已下线)2021年秋季高三化学开学摸底考试卷01(山东专用)湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
10 . 如图,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由B向左移动,当移至C处时容器体积缩小至最小,为原体积的9/10,随着CO2的继续通入,活塞又逐渐向右移动。下列说法中正确的是
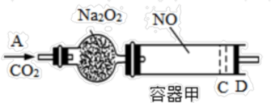

| A.活塞从D处移动到C处的过程中,通入的CO2气体为2.24L(标准状况) |
| B.NO2转化为N2O4的转化率为20% |
| C.容器甲中NO已反应完 |
| D.活塞移至C处后,继续通入a molCO2,此时活塞恰好回至D处,则a小于0.01 |
您最近一年使用:0次
2020-04-17更新
|
338次组卷
|
15卷引用:【全国百强校】湖南省长沙市长郡中学2019届高三上学期第五次调研考试化学试题
【全国百强校】湖南省长沙市长郡中学2019届高三上学期第五次调研考试化学试题(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略【全国百强校】湖南省长沙市雅礼中学2019届高三上学期月考(五)化学试题2020届高考化学小题狂练(全国通用版)专练14 化学平衡黑龙江省哈尔滨市第六中学2020届高三上学期第三次调研考试化学试题2019年秋高三化学复习强化练习—— 化学计量的相关计算2020届高三化学二轮冲刺新题专练——氮氧化物的性质及应用(提升练)夯基提能2020届高三化学选择题对题专练——常见无机物及其性质应用——氮及其化合物(提升练习)福建省厦门双十中学2020届高三上学期第二次(12月)月考化学试题黑龙江省哈尔滨市第三中学校2021届高三上学期第二次验收考试化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高二上学期期末考试化学试题湖北省荆州中学2019-2020学年高二上学期第一次月考化学试题黑龙江省大庆铁人中学2019-2020学年高二10月月考化学试题(已下线)【新东方】2020-67(已下线)【南昌新东方】2019 南昌市豫章 高二上 期末



