三氧化钼( )是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为
)是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为 )通过一定条件来制备。回答下列相关问题:
)通过一定条件来制备。回答下列相关问题:
⑴已知:①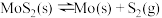

②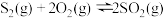

③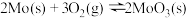

则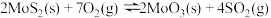 的
的
________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
⑵若在恒温恒容条件下,仅发生反应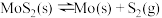 。
。
①下列说法正确的是________ (填字母)。
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加 的量,平衡正向移动
的量,平衡正向移动
②达到平衡时 的浓度为1.4 mol·L−1,充入一定量的
的浓度为1.4 mol·L−1,充入一定量的 ,反应再次达到平衡,
,反应再次达到平衡, 浓度
浓度________ (填“ ”“
”“ ”或“
”或“ ”) 1.4 mol·L−1。
”) 1.4 mol·L−1。
⑶在 恒容密闭容器中充入
恒容密闭容器中充入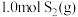 和
和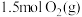 ,若仅发生反应:
,若仅发生反应: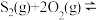
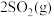 ,
,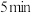 后反应达到平衡,此时容器压强为起始时的80%,则
后反应达到平衡,此时容器压强为起始时的80%,则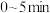 内,
内, 的反应速率为
的反应速率为________  。
。
⑷在恒容密闭容器中,加入足量的 和
和 ,仅发生反应:
,仅发生反应: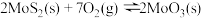

 。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
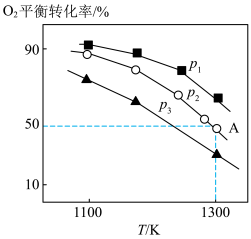
①
________ (填“ ”“
”“ ”或“
”或“ ”)0;比较
”)0;比较 、
、 、
、 的大小:
的大小:________ 。
②若初始时通入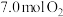 ,
, 为
为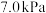 ,则
,则 点平衡常数
点平衡常数
________ (用气体平衡分压代替气体平衡浓度计算,分压 总压
总压 气体的物质的量分数,写出计算式即可)。
气体的物质的量分数,写出计算式即可)。
 )是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为
)是石油工业中常用的催化剂,也是搪瓷釉药的颜料,该物质常使用辉钼矿(主要成分为 )通过一定条件来制备。回答下列相关问题:
)通过一定条件来制备。回答下列相关问题:⑴已知:①
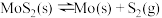

②
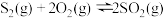

③
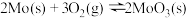

则
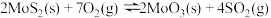 的
的
 、
、 、
、 的代数式表示)。
的代数式表示)。⑵若在恒温恒容条件下,仅发生反应
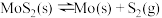 。
。①下列说法正确的是
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加
 的量,平衡正向移动
的量,平衡正向移动②达到平衡时
 的浓度为1.4 mol·L−1,充入一定量的
的浓度为1.4 mol·L−1,充入一定量的 ,反应再次达到平衡,
,反应再次达到平衡, 浓度
浓度 ”“
”“ ”或“
”或“ ”) 1.4 mol·L−1。
”) 1.4 mol·L−1。⑶在
 恒容密闭容器中充入
恒容密闭容器中充入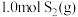 和
和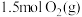 ,若仅发生反应:
,若仅发生反应: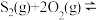
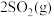 ,
,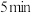 后反应达到平衡,此时容器压强为起始时的80%,则
后反应达到平衡,此时容器压强为起始时的80%,则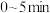 内,
内, 的反应速率为
的反应速率为 。
。⑷在恒容密闭容器中,加入足量的
 和
和 ,仅发生反应:
,仅发生反应: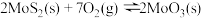

 。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
①

 ”“
”“ ”或“
”或“ ”)0;比较
”)0;比较 、
、 、
、 的大小:
的大小:②若初始时通入
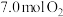 ,
, 为
为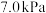 ,则
,则 点平衡常数
点平衡常数
 总压
总压 气体的物质的量分数,写出计算式即可)。
气体的物质的量分数,写出计算式即可)。
20-21高三上·云南楚雄·期末 查看更多[5]
云南省楚雄彝族自治州2020届高三上学期期末考试理综化学试题陕西省2020届高三3月线上联考理综化学试题吉林省白山市2020届高三二模理综化学试卷(已下线)2021年秋季高三化学开学摸底考试卷01(山东专用)湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题
更新时间:2020-06-11 19:40:30
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】研究汽车尾气的产生、转化对环境保护有重要意义。汽车尾气管中的三元催化剂能同时实现CO、CxHy、NOn三种成分的净化。
(1)已知热化学方程式:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
N2(g)+O2(g) 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
则反应CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(l) ΔH=____ kJ·mol-1。
(2)研究表明,温度对CO、CxHy、NOn的产生和排放有较大影响。
①汽车发动机内的温度越高,生成的NO越多,原因是____ 。
②当汽车刚冷启动时,汽车尾气管排放的CO、CxHy、NOn浓度较高,一段时间后浓度逐渐降低。汽车刚冷启动时排放CO、CxHy、NOn浓度较高的原因是____ 。
(3)催化剂表面CO、CxHy、NOn的转化如图1所示,化合物W可借助图2 (傅里叶红外光谱图)确定。
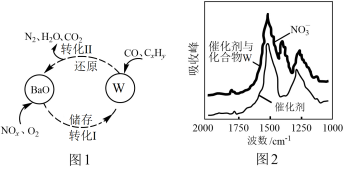
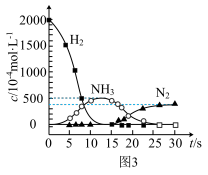
①在图1所示转化中,W的化学式为____ 。若转化Ⅱ中消耗CO的物质的量为1mol,生成N2的物质的量为1mol,则被CxHy还原的W的物质的量为____ 。
②用H2代替CO、CxHy与W反应,该过程相关物质浓度随时间的变化关系如图3所示。该过程分为两步,第一步反应消耗的H2与W的物质的量之比是____ 。
(4)尾气净化过程中,有时会产生N2O。用同位素示踪法研究发现N2O的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的N2O几乎都是15NNO。写出该反应的化学方程式:____ 。
(1)已知热化学方程式:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
N2(g)+O2(g)
 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1则反应CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(l) ΔH=
(2)研究表明,温度对CO、CxHy、NOn的产生和排放有较大影响。
①汽车发动机内的温度越高,生成的NO越多,原因是
②当汽车刚冷启动时,汽车尾气管排放的CO、CxHy、NOn浓度较高,一段时间后浓度逐渐降低。汽车刚冷启动时排放CO、CxHy、NOn浓度较高的原因是
(3)催化剂表面CO、CxHy、NOn的转化如图1所示,化合物W可借助图2 (傅里叶红外光谱图)确定。


①在图1所示转化中,W的化学式为
②用H2代替CO、CxHy与W反应,该过程相关物质浓度随时间的变化关系如图3所示。该过程分为两步,第一步反应消耗的H2与W的物质的量之比是
(4)尾气净化过程中,有时会产生N2O。用同位素示踪法研究发现N2O的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的N2O几乎都是15NNO。写出该反应的化学方程式:
您最近一年使用:0次
【推荐2】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知: ①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJ•mol﹣1
②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ•mol﹣1
③H2O(g)=H2O(1)△H3=﹣44.0kJ•mol﹣1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_____________________
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)⇌CO(g)+3H2(g)
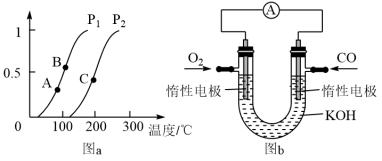
①一定条件下CH4的平衡转化率与温度、压强的关系如图a,则Pl___ P2(填“<”、“>”或“=”)
②A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为_________________
③100℃时,将1molCH4和2molH2O通入容积为10L的反应室,达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=____________
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为__________________________
(1)已知: ①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJ•mol﹣1
②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ•mol﹣1
③H2O(g)=H2O(1)△H3=﹣44.0kJ•mol﹣1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)⇌CO(g)+3H2(g)
①一定条件下CH4的平衡转化率与温度、压强的关系如图a,则Pl
②A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为
③100℃时,将1molCH4和2molH2O通入容积为10L的反应室,达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】二氧化碳是主要的温室气体,也是一种工业原料。将其固定及利用,有利于缓解温室效应带来的环境问题。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) △H1=-484 kJ/mol
2CH3OH(g) +3O2(g)=2CO2(g)+4H2O(g) △H2=-1348 kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是________ 。
(2)用二氧化碳合成低密度聚乙烯(LDPE)。以纳米二氧化钛膜为工作电极,常温常压电解CO2,可制得LDPE,该电极反应可能的机理如下图所示。
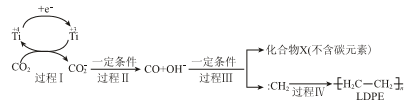
① 过程Ⅰ~Ⅲ中碳元素均发生________ 反应(填“氧化”或“还原”)。
② CO2转化为LDPE的电极反应式是(补充完整并配平)________
2n CO2 + □________ +□________=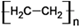 + □________。
+ □________。
③工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下CO2的体积是______ L。
(3)用二氧化碳与环氧丙烷(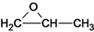 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示;在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示;在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
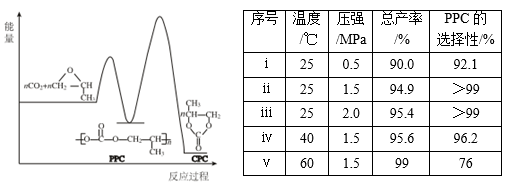
①通过表中数据ⅰ、ⅱ、ⅲ可以得出的结论是________ ;在25℃时,实际生产中选择反应压强为1.5MPa,而不是2.0MPa,理由是________ 。
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是______ 。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) △H1=-484 kJ/mol
2CH3OH(g) +3O2(g)=2CO2(g)+4H2O(g) △H2=-1348 kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是
(2)用二氧化碳合成低密度聚乙烯(LDPE)。以纳米二氧化钛膜为工作电极,常温常压电解CO2,可制得LDPE,该电极反应可能的机理如下图所示。

① 过程Ⅰ~Ⅲ中碳元素均发生
② CO2转化为LDPE的电极反应式是(补充完整并配平)
2n CO2 + □________ +□________=
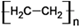 + □________。
+ □________。③工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下CO2的体积是
(3)用二氧化碳与环氧丙烷(
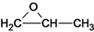 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示;在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示;在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
①通过表中数据ⅰ、ⅱ、ⅲ可以得出的结论是
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,
2NH3(g) ΔH=-92.4 kJ·mol-1,
I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:
(1)测得反应放出的热量_________ 92.4kJ.(填“小于”,“大于”或“等于”)
(2)当反应达到平衡时,N2和H2的浓度比是___________ ;N2和H2的转化率比是___________ 。
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量________ 。(填“变大”、“变小”或“不变”)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将___________ (填“正向”、“逆向”或“不”)移动。
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将____________ (填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________ (填“大于”、“小于”或“等于”)原来的2倍。
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。
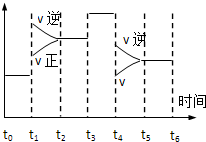
(1)t1、t3、时刻,体系中分别是什么条件发生了变化?
t1_____________________ ,t3_____________________ 。
(2)下列时间段中,氨的百分含量最高的是_______
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
Ⅲ.在一容积为2 L的密闭容器内加入0.2 mol N2和0.6 mol H2,在一定条件下发生该反应,反应中NH3的物质的量浓度的变化情况如图所示:
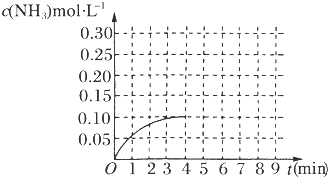
(1)根据图示,计算从反应开始到第4分钟达到平衡时,平均反应速率υ(N2)为__________ 。
(2)达到平衡后,第5分钟末,若保持其它条件不变,只改变反应温度,则NH3的物质的量浓度不可能为_____________ 。
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)达到平衡后,第5分钟末,若保持其它条件不变,只把容器的体积缩小,新平衡时NH3的浓度恰好为原来的2倍,则新体积_____ (选填“大于”、“等于”、“小于”)二分之一倍的原体积,化学平衡常数________ (选填“增大”、“减小”或“不变”)。
 2NH3(g) ΔH=-92.4 kJ·mol-1,
2NH3(g) ΔH=-92.4 kJ·mol-1,I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:
(1)测得反应放出的热量
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。

(1)t1、t3、时刻,体系中分别是什么条件发生了变化?
t1
(2)下列时间段中,氨的百分含量最高的是
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
Ⅲ.在一容积为2 L的密闭容器内加入0.2 mol N2和0.6 mol H2,在一定条件下发生该反应,反应中NH3的物质的量浓度的变化情况如图所示:

(1)根据图示,计算从反应开始到第4分钟达到平衡时,平均反应速率υ(N2)为
(2)达到平衡后,第5分钟末,若保持其它条件不变,只改变反应温度,则NH3的物质的量浓度不可能为
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)达到平衡后,第5分钟末,若保持其它条件不变,只把容器的体积缩小,新平衡时NH3的浓度恰好为原来的2倍,则新体积
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】水泥窑炉可产生大量NOx,是高污染排放的工业窑炉,如何处理水泥窑炉产生的尾气是科技工作者非常关心的问题。回答下列问题:
(1)NOx可能引发的环境问题是_______ (填一种)。
(2)“水泥窑协同焚烧污泥”既有助于减少水泥窑烟气中NOx的排放,又能处理城市污泥。该方法是将污泥投加到水泥预分解炉内,利用污泥燃烧产生的还原性气体(NH3、CO等)还原水泥窑烟气中的NOx。
①CO还原NO的反应历程中相对能量变化如下图:

该历程中最大能垒(活化能)E正=_______ kJ·mol-1,该步骤的化学方程式是_______ ;CO还原NO总反应的热化学方程式是_______ 。
②将一定量的污泥投加到水泥预分解炉内,控制燃烧温度为1200 ℃,测得燃烧过程中NO的浓度和O2、CO2的体积分数随时间变化如图所示。0~50 s内,以NO表示的反应速率v(NO)=_______ mol·L−1·s−1;图中表示CO2的体积分数随时间变化的曲线是_______ (填“a”或“b”)。

(3)在水泥窑炉高温主燃区喷氨也可还原NO,主要反应为:6NO(g)+4NH3(g) 5N2(g)+6H2O(g) ΔH<0。实验测得主燃区温度、过量空气系数(KSR1)与NO还原效率的关系如图所示。
5N2(g)+6H2O(g) ΔH<0。实验测得主燃区温度、过量空气系数(KSR1)与NO还原效率的关系如图所示。
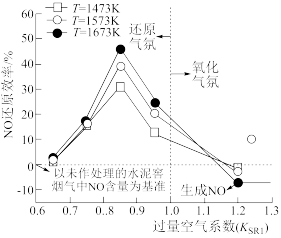
①“还原气氛”下,该反应的最佳条件是_______ (填标号)。
A.T=1473,KSR1=0.75 B.T=1573,KSR1=1.2 C.T=1673,KSR1=0.85
②“氧化气氛”下,当KSR1=1.2时,NO的还原效率低于“基准”的原因是_______ 。
(1)NOx可能引发的环境问题是
(2)“水泥窑协同焚烧污泥”既有助于减少水泥窑烟气中NOx的排放,又能处理城市污泥。该方法是将污泥投加到水泥预分解炉内,利用污泥燃烧产生的还原性气体(NH3、CO等)还原水泥窑烟气中的NOx。
①CO还原NO的反应历程中相对能量变化如下图:

该历程中最大能垒(活化能)E正=
②将一定量的污泥投加到水泥预分解炉内,控制燃烧温度为1200 ℃,测得燃烧过程中NO的浓度和O2、CO2的体积分数随时间变化如图所示。0~50 s内,以NO表示的反应速率v(NO)=

(3)在水泥窑炉高温主燃区喷氨也可还原NO,主要反应为:6NO(g)+4NH3(g)
 5N2(g)+6H2O(g) ΔH<0。实验测得主燃区温度、过量空气系数(KSR1)与NO还原效率的关系如图所示。
5N2(g)+6H2O(g) ΔH<0。实验测得主燃区温度、过量空气系数(KSR1)与NO还原效率的关系如图所示。
①“还原气氛”下,该反应的最佳条件是
A.T=1473,KSR1=0.75 B.T=1573,KSR1=1.2 C.T=1673,KSR1=0.85
②“氧化气氛”下,当KSR1=1.2时,NO的还原效率低于“基准”的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】(1)25℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
则该温度下,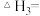
______  (用a和b表示)。
(用a和b表示)。
(2)25℃时,在体积为2L的恒容密闭容器中通入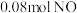 和
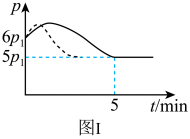
和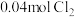 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则
______ (填“﹥”“﹤”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图I虚线所示,则改变的条件是______ 。图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(1gK)与温度的变化关系图,其中正确的曲线是______ (填“甲”或“乙”),a值为______ 。25℃时测得反应③在某时刻, 、
、 、
、 的浓度分别为0.8、0.1、03,则此时V正
的浓度分别为0.8、0.1、03,则此时V正_____ V逆(填“>”“<”或“=”)
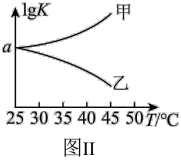
| 热化学方程式 | 平衡常数 | |
| ① | 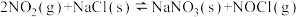 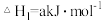 |  |
| ② | 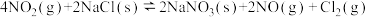  |  |
| ③ | 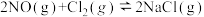  |  |
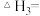
 (用a和b表示)。
(用a和b表示)。(2)25℃时,在体积为2L的恒容密闭容器中通入
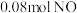 和
和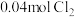 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则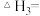
 、
、 、
、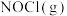 的浓度分别为0.8、0.1、03,则此时V正
的浓度分别为0.8、0.1、03,则此时V正
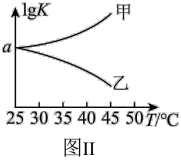
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】二氧化硫和氮氧化物都是常见的大气污染物、回答下列相关问题。
Ⅰ.某温度下氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
ⅰ.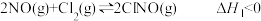
ⅱ.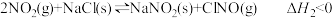
(1)现有反应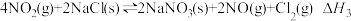 ,则此反应的平衡常数的表达式
,则此反应的平衡常数的表达式
___________ ,反应热
___________ (用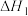 、
、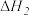 表示)。
表示)。
(2)为研究不同条件对反应ⅱ的影响,在恒温条件下,向 恒容密闭容器中加入
恒容密闭容器中加入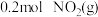 和足量的
和足量的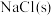 ,
, 时反应ⅱ达到平衡。测得平衡时
时反应ⅱ达到平衡。测得平衡时 的转化率
的转化率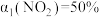 ,则
,则 内反应速率
内反应速率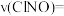
___________ ,平衡常数
___________ 。
Ⅱ.除氮氧化物外,也是重要的大气污染物,需要对其进行吸收处理。
(3)工业上也可以用 溶液吸收
溶液吸收 ,并用电解法处理吸收后所得溶液以实现吸收液的回收再利用,装置如图所示,则
,并用电解法处理吸收后所得溶液以实现吸收液的回收再利用,装置如图所示,则
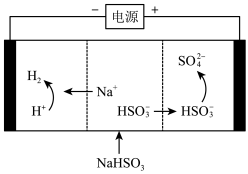
①工作一段时间后,阴极区溶液的
___________ (填“增大”“减小”或“不变”)。
②写出阳极的电极反应式___________ 。
Ⅰ.某温度下氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
ⅰ.
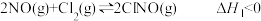
ⅱ.
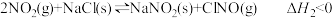
(1)现有反应
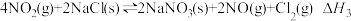 ,则此反应的平衡常数的表达式
,则此反应的平衡常数的表达式

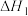 、
、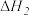 表示)。
表示)。(2)为研究不同条件对反应ⅱ的影响,在恒温条件下,向
 恒容密闭容器中加入
恒容密闭容器中加入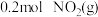 和足量的
和足量的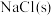 ,
, 时反应ⅱ达到平衡。测得平衡时
时反应ⅱ达到平衡。测得平衡时 的转化率
的转化率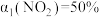 ,则
,则 内反应速率
内反应速率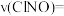

Ⅱ.除氮氧化物外,也是重要的大气污染物,需要对其进行吸收处理。
(3)工业上也可以用
 溶液吸收
溶液吸收 ,并用电解法处理吸收后所得溶液以实现吸收液的回收再利用,装置如图所示,则
,并用电解法处理吸收后所得溶液以实现吸收液的回收再利用,装置如图所示,则
①工作一段时间后,阴极区溶液的

②写出阳极的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分为CO、 和
和 )可以合成甲醇,涉及的反应如下:
)可以合成甲醇,涉及的反应如下:
反应i:
反应ii:
(1)关于 叙述不正确的是___________
叙述不正确的是___________
(2)在温度T℃下,向一体积为1L的恒容密闭容器中充入4mol 和8mol
和8mol ,在某催化剂作用下发生反应i和ii,经5min达到平衡,测得
,在某催化剂作用下发生反应i和ii,经5min达到平衡,测得 的物质的量为3mol,起始及平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用
的物质的量为3mol,起始及平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用 的平均反应速率为
的平均反应速率为________  ;反应i的压强平衡常数
;反应i的压强平衡常数
________ 。
Ⅱ.基于新材料及3D打印技术,科学家研制出的微胶囊吸收剂,它能将排放的 以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入
以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入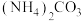 溶液,其原理如图所示。
溶液,其原理如图所示。
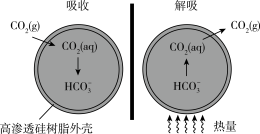
已知: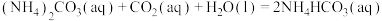
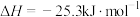
(3)吸收 时宜选用
时宜选用_________ (选填“低温”或“高温”)理由________ 、_________ (列举两点)。
(4)吸收 过程中,胶囊内部溶液的
过程中,胶囊内部溶液的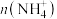
_________ (“增大、减小、或不变”),理由是___________ (不考虑其他副反应及溶液体积变化)。
(5)已知 为二元弱酸,常温下用0.1mol/LNaOH溶液滴定20mL0.1mol/L
为二元弱酸,常温下用0.1mol/LNaOH溶液滴定20mL0.1mol/L 溶液的滴定曲线如下图。
溶液的滴定曲线如下图。
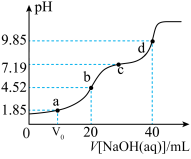
①d点溶液中离子的物质的量浓度由大到小的关系:___________ 。
②b点溶液中:
___________ 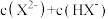 (填“>、<或=”)。
(填“>、<或=”)。
 和
和 )可以合成甲醇,涉及的反应如下:
)可以合成甲醇,涉及的反应如下:反应i:

反应ii:

(1)关于
 叙述不正确的是___________
叙述不正确的是___________A. 属于酸性氧化物 属于酸性氧化物 | B. 的水溶液能导电,故 的水溶液能导电,故 属于电解质 属于电解质 |
C. 的晶体结构属于分子密堆积 的晶体结构属于分子密堆积 | D. 分子中存在 分子中存在 离域大x键 离域大x键 |
(2)在温度T℃下,向一体积为1L的恒容密闭容器中充入4mol
 和8mol
和8mol ,在某催化剂作用下发生反应i和ii,经5min达到平衡,测得
,在某催化剂作用下发生反应i和ii,经5min达到平衡,测得 的物质的量为3mol,起始及平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用
的物质的量为3mol,起始及平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用 的平均反应速率为
的平均反应速率为 ;反应i的压强平衡常数
;反应i的压强平衡常数
Ⅱ.基于新材料及3D打印技术,科学家研制出的微胶囊吸收剂,它能将排放的
 以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入
以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入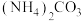 溶液,其原理如图所示。
溶液,其原理如图所示。
已知:
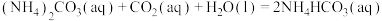
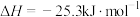
(3)吸收
 时宜选用
时宜选用(4)吸收
 过程中,胶囊内部溶液的
过程中,胶囊内部溶液的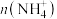
(5)已知
 为二元弱酸,常温下用0.1mol/LNaOH溶液滴定20mL0.1mol/L
为二元弱酸,常温下用0.1mol/LNaOH溶液滴定20mL0.1mol/L 溶液的滴定曲线如下图。
溶液的滴定曲线如下图。
①d点溶液中离子的物质的量浓度由大到小的关系:
②b点溶液中:

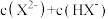 (填“>、<或=”)。
(填“>、<或=”)。
您最近一年使用:0次
【推荐3】以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
(1)已知: 2C(s) + O2(g) = 2CO(g) ∆H1= a kJ/mol
N2(g) + O2(g) = 2NO(g) ∆H2= b kJ/mol
2NO(g) + 2CO(g) =2CO2(g) + N2(g) ∆H3= c kJ/mol
则 2NO(g) + C(s) = CO2(g) + N2(g) ∆H=_______ kJ/mol
(2)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应减少尾气污染。
已知2NO(g)+2CO(g) N2(g)+2CO2(g) ∆H<0。
N2(g)+2CO2(g) ∆H<0。
①在500℃时,向恒容密闭体系中通入1mol的NO和1mol的CO进行反应时,下列描述能说明反应达到平衡状态的是_______ 。
A. (CO)正 = 2
(CO)正 = 2 (N2)逆
(N2)逆
B.体系中混合气体密度不变
C.混合气体的平均相对分子质量不变
D.体系中NO、CO的浓度相等
E.单位时间内消耗nmol的NO同时消耗nmol的N2
②向1L密闭容器中通入1mol的NO和1mol的CO气体,在不同温度下反应达到平衡时,NO的平衡转化率随压强变化曲线如图所示:

T1_______ T2(填“>”、“<”),理由是_______ 。M点时混合气体中CO的体积分数为_______ 。
③一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
该反应条件下的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),该反应中的 正=k正·p2(NO)p2(CO),
正=k正·p2(NO)p2(CO), 逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正_______ k逆(填“>”、“<”或“=”)。
(1)已知: 2C(s) + O2(g) = 2CO(g) ∆H1= a kJ/mol
N2(g) + O2(g) = 2NO(g) ∆H2= b kJ/mol
2NO(g) + 2CO(g) =2CO2(g) + N2(g) ∆H3= c kJ/mol
则 2NO(g) + C(s) = CO2(g) + N2(g) ∆H=
(2)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应减少尾气污染。
已知2NO(g)+2CO(g)
 N2(g)+2CO2(g) ∆H<0。
N2(g)+2CO2(g) ∆H<0。①在500℃时,向恒容密闭体系中通入1mol的NO和1mol的CO进行反应时,下列描述能说明反应达到平衡状态的是
A.
 (CO)正 = 2
(CO)正 = 2 (N2)逆
(N2)逆 B.体系中混合气体密度不变
C.混合气体的平均相对分子质量不变
D.体系中NO、CO的浓度相等
E.单位时间内消耗nmol的NO同时消耗nmol的N2
②向1L密闭容器中通入1mol的NO和1mol的CO气体,在不同温度下反应达到平衡时,NO的平衡转化率随压强变化曲线如图所示:

T1
③一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| p/kPa | 200 | 185 | 173 | 165 | 160 | 160 |
 正=k正·p2(NO)p2(CO),
正=k正·p2(NO)p2(CO), 逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
您最近一年使用:0次



