名校
1 . 苯乙烯是生产塑料和合成橡胶的重要有机原料,国内外目前生产苯乙烯的方法主要是乙苯催化脱氢法,反应方程式为:

(1)实际生产过程中,通常向乙苯中掺混氮气(N2不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示(其中投料比m为原料气中乙苯和N2的物质的量之比,取值分别为1:0、1:1、1:5、1:9)。
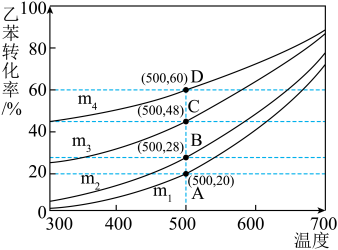
①乙苯催化脱氢反应的∆H______ 0(填“>”或“<”).
②投料比m为1:9的曲线是______ (填m1、m2、m3或m4).
(2)近年来,有研究者发现若将上述生产过程中通入N2改为通入CO2,在CO2气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
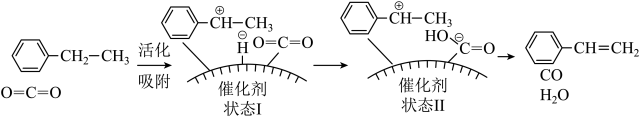
①该过程中发生的总反应化学方程式为______ .
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,乙苯的转化率______ (填“升高”或“降低”)。
(3)苯乙烯与溴苯在一定条件下发生Heck反应:

根据上表数据,下列说法正确的是______。

(1)实际生产过程中,通常向乙苯中掺混氮气(N2不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示(其中投料比m为原料气中乙苯和N2的物质的量之比,取值分别为1:0、1:1、1:5、1:9)。

①乙苯催化脱氢反应的∆H
②投料比m为1:9的曲线是
(2)近年来,有研究者发现若将上述生产过程中通入N2改为通入CO2,在CO2气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:

①该过程中发生的总反应化学方程式为
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,乙苯的转化率
(3)苯乙烯与溴苯在一定条件下发生Heck反应:

| 溴苯用量(mmol) | 100 | 100 | 100 | 100 | 100 | 100 | 100 |
| 催化剂用量(mmol) | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| 反应温度(℃) | 100 | 100 | 100 | 100 | 120 | 140 | 160 |
| 反应时间(h) | 10 | 12 | 14 | 16 | 14 | 14 | 14 |
| 4产率(%) | 81.2 | 84.4 | 86.6 | 86.2 | 93.5 | 96.6 | 89.0 |
| A.最佳反应温度为100℃ | B.最佳反应时间为16h |
| C.温度过高时催化剂活性可能降低 | D.反应产物是顺式结构 |
您最近一年使用:0次
解题方法
2 . 压强变化对化学平衡的影响规律
增大压强,平衡向___________ 的方向移动;
减小压强,平衡向___________ 的方向移动。
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡___________ 移动。
增大压强,平衡向
减小压强,平衡向
对于反应前后气体分子数目不变的反应,增大压强时,改变反应体系的压强,平衡
您最近一年使用:0次
2023-07-15更新
|
126次组卷
|
2卷引用:山东省济宁市特殊教育学校2023-2024学年高二上学期期末化学试卷
22-23高一下·上海·期末
3 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近一年使用:0次
4 . 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为_____ 。

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为_____ ,振荡试管,然后再向其中滴加8滴0.1 mol Na2S溶液,发生反应的离子方程式为_____ ,观察到的现象为_____ 。
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为_____ ,几分钟后,观察导管中水柱的变化为______ ,引起这种变化的原因为_____ 。

Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为

您最近一年使用:0次
名校
5 . 现有反应mA(g)+nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)m+n_______ (填“>”“<”或“=”)p。
(2)减压时,A的质量分数_______ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则B的转化率_______ 。
(4)若升高温度,则平衡时,B、C的浓度之比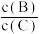 将
将_______ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_______ 。
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数_______ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色_______ (填“变浅”“变深”或“不变”)。
(1)m+n
(2)减压时,A的质量分数
(3)若加入B(体积不变),则B的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
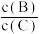 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数
您最近一年使用:0次
解题方法
6 . 已知:①
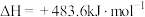
②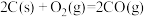
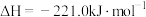
③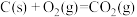

④
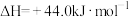
回答下列问题:
(1)上述过程属于放热反应的是_______ (填序号)。
(2)下图是反应②的能量变化图
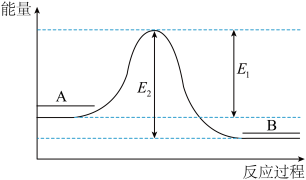
①请写出图中A、B处对应的物质、状态及其物质的量[如:
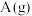 ]:
]:
A:_______ ;B:_______ 。
② 表示
表示_______ ;
③ 与
与 的差值为
的差值为_______ (填具体数字)
(3)写出 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式_______ 。
(4)其他条件不变,压缩容器体积,反应④的平衡_______ (填“正反应方向”“逆反应方向”或“不”)移动,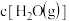
_______ (填“变大”“变小”或“不变”)。

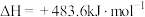
②
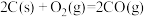
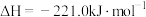
③
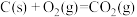

④

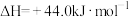
回答下列问题:
(1)上述过程属于放热反应的是
(2)下图是反应②的能量变化图

①请写出图中A、B处对应的物质、状态及其物质的量[如:

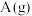 ]:
]:A:
②
 表示
表示③
 与
与 的差值为
的差值为(3)写出
 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式(4)其他条件不变,压缩容器体积,反应④的平衡
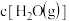
您最近一年使用:0次
7 . 一定条件下,某可逆反应在密闭容器中建立化学平衡,在t1时刻改变某一个条件,建立新的平衡,其v-t图像如下:

(1)对于反应:2SO2(g)+O2(g) 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为________ (填字母,下同),平衡_________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应2NH3(g) N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为________ ,平衡__________________ 移动。
(3)对于反应H2(g)+I2(g) 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为________ ,平衡________ 移动。

(1)对于反应:2SO2(g)+O2(g)
 2SO3(g),t1时刻缩小容器体积,其图像为
2SO3(g),t1时刻缩小容器体积,其图像为(2)对于反应2NH3(g)
 N2(g)+3H2(g),t1时刻增大容器体积,其图像为
N2(g)+3H2(g),t1时刻增大容器体积,其图像为(3)对于反应H2(g)+I2(g)
 2HI(g),t1时刻缩小容器体积,其图像为
2HI(g),t1时刻缩小容器体积,其图像为
您最近一年使用:0次
2022-09-27更新
|
988次组卷
|
4卷引用:河北省魏县第五中学2022-2023学年高二上学期1月期末考试化学试题
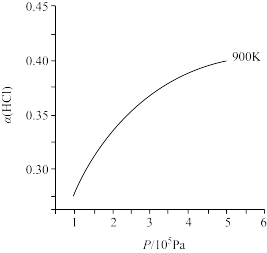
8 . 氯及其化合物在生活和生产中应用广泛。已知下列反应: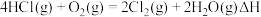
900 K时,将 和
和 按4:1充入恒容的密闭容器中。
按4:1充入恒容的密闭容器中。
(1)若该反应可自发进行,则
_______ (填“>”或“<”)。
(2)下列不可以 作为该反应达到平衡的判据是_______。
(3)已知:某气体的分压=气体总压强×该气体的体积分数(或物质的量分数),且在化学平衡体系中,各气体物质的分压替代浓度,计算的平衡常数即为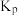 。若上述反应达到平衡时,混合气体平衡总压强为p,
。若上述反应达到平衡时,混合气体平衡总压强为p, 气体的平衡转化率为50%,则该反应的压强平衡常数
气体的平衡转化率为50%,则该反应的压强平衡常数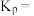
_______ 。
(4) 的平衡转化率
的平衡转化率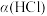 随压强(P)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在
随压强(P)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在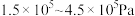 范围内,
范围内, 的平衡转化率
的平衡转化率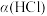 随压强(P)变化曲线示意图。
随压强(P)变化曲线示意图。_______
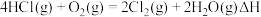
900 K时,将
 和
和 按4:1充入恒容的密闭容器中。
按4:1充入恒容的密闭容器中。(1)若该反应可自发进行,则

(2)下列
| A.气体的压强不变 | B.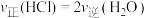 |
| C.K不变 | D.容器内气体的密度不变 |
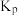 。若上述反应达到平衡时,混合气体平衡总压强为p,
。若上述反应达到平衡时,混合气体平衡总压强为p, 气体的平衡转化率为50%,则该反应的压强平衡常数
气体的平衡转化率为50%,则该反应的压强平衡常数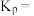
(4)
 的平衡转化率
的平衡转化率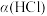 随压强(P)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在
随压强(P)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在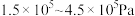 范围内,
范围内, 的平衡转化率
的平衡转化率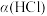 随压强(P)变化曲线示意图。
随压强(P)变化曲线示意图。
您最近一年使用:0次
名校
9 . 在密闭容器内,使1 mol N2和3 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
(1)当反应达到平衡时,N2和H2的浓度之比为_______ 。
(2)保持体积不变,升高温度,平衡_______ (填“正向”、“逆向”或“不”,下同)移动,密度_______ (填“变大”“变小”或“不变”)。
(3)当反应达到平衡时,保持温度、体积不变,充入氩气,平衡_______ 移动。
(4)当反应达到平衡时,保持温度、压强不变,充入氩气,平衡_______ 移动。
(5)当反应达到平衡时,保持温度、体积不变,充入氮气,平衡_______ 移动;氢气的转化率_______ (填“增大”“减小”或“不变”)。
 2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1(1)当反应达到平衡时,N2和H2的浓度之比为
(2)保持体积不变,升高温度,平衡
(3)当反应达到平衡时,保持温度、体积不变,充入氩气,平衡
(4)当反应达到平衡时,保持温度、压强不变,充入氩气,平衡
(5)当反应达到平衡时,保持温度、体积不变,充入氮气,平衡
您最近一年使用:0次
解题方法
10 . 美国Bay工厂使用石油热裂解的副产物甲烷来制取氢气,其过程分两步进行;
第一步:CH4(g)+H2O(g) CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
第二步:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)其他条件相同时、第Ⅰ步反应中CH4的平衡转化率随压强和温度的变化如图所示。
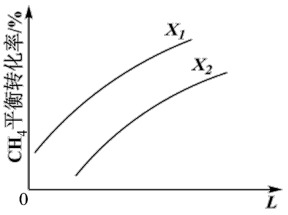
图中L表示____ (填“温度”或“压强”)。其另外一个物理量X1____ X2(填“>”或“<”)。
(2)反应CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
①从表中数据可以推断,此反应的正反应为____ (填“吸热”或“放热”)反应。
②500℃时,向恒容密闭容器中充入CO(g)和H2O(g)各3mol,达到平衡后CO(g)的转化率为____ ;若该反应在绝热容器(与外界环境没有热交换)中进行,达到平衡后CO(g)的转化率将____ (填“增大”、“减小”或“不变”)。
③在830℃时,向恒容密闭容器中充入2molCO(g),5molH2O(g),4molH2(g)和3molCO2(g),此时v正____ v逆(填“>”、“<”或“=”)。
第一步:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0第二步:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)(1)其他条件相同时、第Ⅰ步反应中CH4的平衡转化率随压强和温度的变化如图所示。

图中L表示
(2)反应CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。
H2(g)+CO2(g)的平衡常数K随湿度的变化如表所示。| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①从表中数据可以推断,此反应的正反应为
②500℃时,向恒容密闭容器中充入CO(g)和H2O(g)各3mol,达到平衡后CO(g)的转化率为
③在830℃时,向恒容密闭容器中充入2molCO(g),5molH2O(g),4molH2(g)和3molCO2(g),此时v正
您最近一年使用:0次



