2023高三·全国·专题练习
1 . 现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]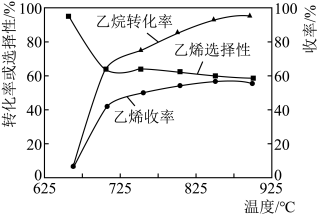
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
您最近一年使用:0次
2023高三·全国·专题练习
2 . 乙苯催化脱氢制苯乙烯反应:

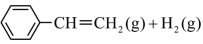 ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________
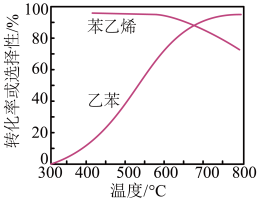


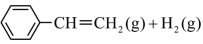 ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
ΔH=+124 kJ·mol-1,工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图,掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
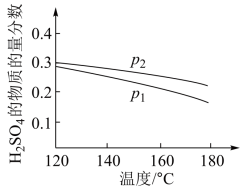
3 . 对反应:3SO2(g)+2H2O (g)=2H2SO4 (l)+S(s) ΔH2=−254 kJ·mol−1,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2___________ p 1(填“>”或“<”),得出该结论的理由是___________

您最近一年使用:0次
2023高三·全国·专题练习
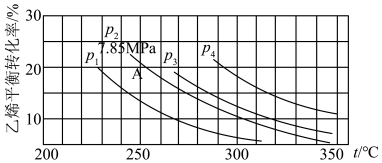
4 . 乙烯气相水合反应的热化学方程式为C2H4(g)+H2O(g)=C2H5OH(g) ΔH=−45.5kJ∙mol−1,下图是乙烯气相水合法制乙醇中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。图中压强(p1、p2、p3、p4)的大小顺序为___________ ,理由是___________

您最近一年使用:0次
2023高三·全国·专题练习
5 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。某兴趣小组对反应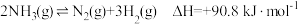 进行了实验探究。在一定温度和催化剂的条件下,将
进行了实验探究。在一定温度和催化剂的条件下,将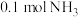 通入
通入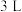 的密闭容器中进行反应(此时容器内总压为
的密闭容器中进行反应(此时容器内总压为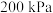 ),各物质的分压随时间的变化曲线如图所示。
),各物质的分压随时间的变化曲线如图所示。
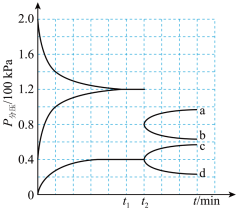
(1)t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是_______ (用图中a、b、c、d表示),理由是______________ 。
(2)在该温度下,反应的标准平衡常数
_______ 。(已知:分压=总压×该组分物质的量分数,对于反应 ,
, ,其中
,其中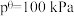 ,
,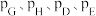 为各组分的平衡分压)
为各组分的平衡分压)
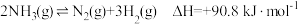 进行了实验探究。在一定温度和催化剂的条件下,将
进行了实验探究。在一定温度和催化剂的条件下,将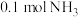 通入
通入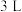 的密闭容器中进行反应(此时容器内总压为
的密闭容器中进行反应(此时容器内总压为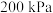 ),各物质的分压随时间的变化曲线如图所示。
),各物质的分压随时间的变化曲线如图所示。
(1)t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
 分压变化趋势的曲线是
分压变化趋势的曲线是(2)在该温度下,反应的标准平衡常数

 ,
, ,其中
,其中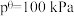 ,
,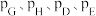 为各组分的平衡分压)
为各组分的平衡分压)
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 工业上常用 与水蒸气在一定条件下来制取
与水蒸气在一定条件下来制取 ,其反应原理为
,其反应原理为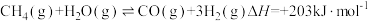 ,在容积为
,在容积为 的密闭容器中通入物质的量均为
的密闭容器中通入物质的量均为 的
的 和水蒸气,在一定条件下发生上述反应,测得平衡时
和水蒸气,在一定条件下发生上述反应,测得平衡时 的体积分数与温度及压强的关系如图所示。
的体积分数与温度及压强的关系如图所示。

压强为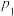 时,在
时,在 点:
点:
_______ 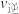 (填“>”“<”或“=”),N点对应温度下该反应的平衡常数
(填“>”“<”或“=”),N点对应温度下该反应的平衡常数
_______ 。比较: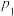
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 与水蒸气在一定条件下来制取
与水蒸气在一定条件下来制取 ,其反应原理为
,其反应原理为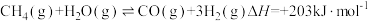 ,在容积为
,在容积为 的密闭容器中通入物质的量均为
的密闭容器中通入物质的量均为 的
的 和水蒸气,在一定条件下发生上述反应,测得平衡时
和水蒸气,在一定条件下发生上述反应,测得平衡时 的体积分数与温度及压强的关系如图所示。
的体积分数与温度及压强的关系如图所示。
压强为
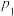 时,在
时,在 点:
点:
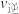 (填“>”“<”或“=”),N点对应温度下该反应的平衡常数
(填“>”“<”或“=”),N点对应温度下该反应的平衡常数
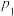
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
2023高三·全国·专题练习
7 . 某实验室模拟反应 ,在密闭容器中加入足量的C和一定量的
,在密闭容器中加入足量的C和一定量的 气体,维持温度为
气体,维持温度为 ,如图为不同压强下该反应经过相同时间
,如图为不同压强下该反应经过相同时间 的转化率随着压强变化的示意图。请从动力学角度分析,
的转化率随着压强变化的示意图。请从动力学角度分析,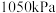 前,反应中
前,反应中 的转化率随着压强增大而增大的原因为
的转化率随着压强增大而增大的原因为_______ ;在 时,
时, 的体积分数为
的体积分数为_______ 。

 ,在密闭容器中加入足量的C和一定量的
,在密闭容器中加入足量的C和一定量的 气体,维持温度为
气体,维持温度为 ,如图为不同压强下该反应经过相同时间
,如图为不同压强下该反应经过相同时间 的转化率随着压强变化的示意图。请从动力学角度分析,
的转化率随着压强变化的示意图。请从动力学角度分析, 前,反应中
前,反应中 的转化率随着压强增大而增大的原因为
的转化率随着压强增大而增大的原因为 时,
时, 的体积分数为
的体积分数为
您最近一年使用:0次
2022高三·全国·专题练习
名校
解题方法
8 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=_______ mol·L-1·min-1(用含t1的代数式表示);
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________
(3)在该温度下,反应的标准平衡常数Kθ=____ 。[已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)⇌gG(g)+hH(g) Kθ= ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
(3)在该温度下,反应的标准平衡常数Kθ=
 ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
您最近一年使用:0次
2021高二·全国·专题练习
9 . 在10℃和2×105Pa的条件下,反应aA(g) dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变)。表中列出了不同压强下平衡时物质D的浓度。
dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变)。表中列出了不同压强下平衡时物质D的浓度。
根据表中数据,回答下列问题:
(1)压强从2×105Pa增加到5×105Pa时,平衡移动方向是____ ,理由是____ 。
(2)压强5×105Pa增加到1×106Pa时,平衡移动的方向是_____ ,理由是____ 。
 dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变)。表中列出了不同压强下平衡时物质D的浓度。
dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变)。表中列出了不同压强下平衡时物质D的浓度。| 压强(Pa) | 2×105 | 5×105 | 1×106 |
| 浓度(mol·L-1) | 0.085 | 0.20 | 0.44 |
根据表中数据,回答下列问题:
(1)压强从2×105Pa增加到5×105Pa时,平衡移动方向是
(2)压强5×105Pa增加到1×106Pa时,平衡移动的方向是
您最近一年使用:0次
2021高二·全国·专题练习
10 . 在密闭容器中进行如下反应:CO2(g)+C(s)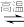 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加C,平衡_____ ,c(CO2)____ 。
(2)缩小反应容器的容积,保持温度不变,则平衡____ ,c(CO2)_____ 。
(3)保持反应容器的容积和温度不变,通入N2,则平衡____ ,c(CO2)____ 。
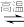 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。(1)增加C,平衡
(2)缩小反应容器的容积,保持温度不变,则平衡
(3)保持反应容器的容积和温度不变,通入N2,则平衡
您最近一年使用:0次



