2024·辽宁沈阳·一模
名校
解题方法
1 . 氢能作为一种清洁、高效、安全、可持续的新能源,被视为21世纪最具发展潜力的清洁能源,是人类的战略能源发展方向。目前,制备氢气有多种途径:途径一:甲醇产生氢气的反应为:
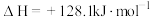
(1)已知相关物质的标准熵数值如下表:
该反应能自发进行的最低温度为___________ K。(保留小数点后1位)
途径二:乙酸制氢的反应为:
反应I: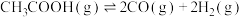
反应Ⅱ: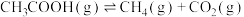
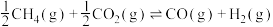

①由图1可得,
___________ kJ·mol-1;
②恒温恒容下发生上述反应,下列说法正确的是___________ 。
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是___________ 。
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数 为
为___________ 。(用平衡分压代替平衡浓度计算)
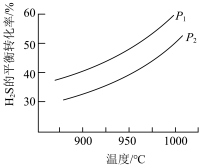
途径三:热分解H2S制氢的反应为: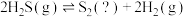
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为___________ (填“气态”或“非气态”),P1___________ P2(填“>”或“<”)。

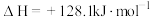
(1)已知相关物质的标准熵数值如下表:
| 化学式 |  |  |  |
标准熵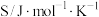 | 126.8 | 130.7 | 197.7 |
途径二:乙酸制氢的反应为:
反应I:
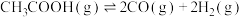
反应Ⅱ:
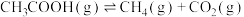
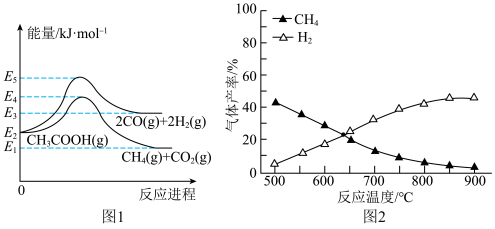
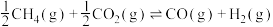

①由图1可得,

②恒温恒容下发生上述反应,下列说法正确的是
A.混合气体密度不变时,反应达到平衡
B.充入CO2,可提高CH4的转化率
C.加入催化剂,可提高H2的平衡产率
D.充入Ar,对H2的产率不产生影响
(3)一定条件下,在密闭容器中加入一定量的乙酸,只发生反应I和反应Ⅱ。
①在相同时间,测得温度与气体产率的关系如上图2所示。约650℃之前,氢气产率低于甲烷的可能原因是
②设达到平衡时,体系总压强为p,乙酸体积分数为20%,反应I消耗的乙酸占投入量的20%,则反应Ⅱ的平衡常数
 为
为途径三:热分解H2S制氢的反应为:
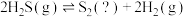
(4)不同温度和压强下,H2S的平衡转化率变化如图。生成物S2的状态为
您最近一年使用:0次
2024-04-13更新
|
274次组卷
|
3卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
名校
解题方法
2 . 完成下列问题。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: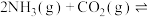
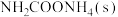
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
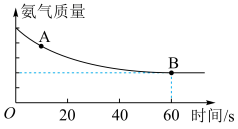
A点正反应速率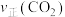
___________ B点逆反应速率 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比___________ (填“下降”、“不变”或“升高”)
(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
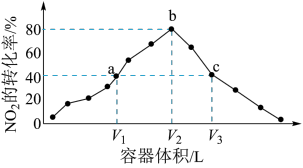
下列说法正确的是___________ 。
A.容器内的压强: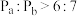
B.图中c点所示条件下,
C.向a点平衡体系中充入一定量的 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大
(3)电解法制取 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
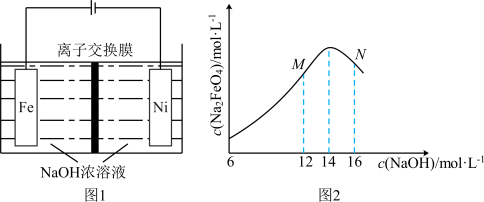
①电解时,Fe电极发生的电极反应式为___________ 。
②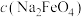 随初始
随初始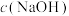 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点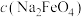 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点___________ ;N点___________ 。
(4)甲醚( )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:
主反应①: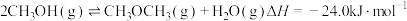 。
。
副反应②: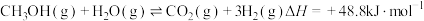 。
。
选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
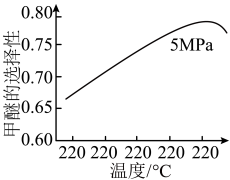
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是___________ 。
(1)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2∶1的
 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡: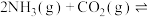
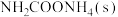
 ,反应过程中氨气质量与时间关系如图所示:
,反应过程中氨气质量与时间关系如图所示:
A点正反应速率
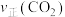
 (填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中
(填“>”、“<”或“=”),上述反应达平衡状态后降低体系温度,新平衡体系中 的体积分数与原平衡相比
的体积分数与原平衡相比(2)温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1mol
 ,发生反应:
,发生反应: ,反应相同时间,测得各容器中
,反应相同时间,测得各容器中 的转化率与容器体积的关系如下图所示。
的转化率与容器体积的关系如下图所示。
下列说法正确的是
A.容器内的压强:
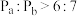
B.图中c点所示条件下,

C.向a点平衡体系中充入一定量的
 ,达到平衡时,
,达到平衡时, 的转化率比原平衡大
的转化率比原平衡大(3)电解法制取
 ,同时可获得氢气:
,同时可获得氢气: ,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质:
,工作原理如图1所示。已知:若NaOH溶液浓度过高,铁电极区会产生红褐色物质: 只在强碱性条件下稳定。
只在强碱性条件下稳定。
①电解时,Fe电极发生的电极反应式为
②
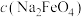 随初始
随初始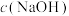 的变化如图2,则分别分析M、N点
的变化如图2,则分别分析M、N点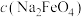 均低于最高值的可能的原因:M点
均低于最高值的可能的原因:M点(4)甲醚(
 )是重要的化工原料,制取原理如下:
)是重要的化工原料,制取原理如下:主反应①:
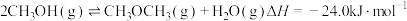 。
。副反应②:
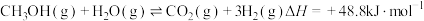 。
。选择合适的催化剂。在不同温度和5MPa压强下,测得甲醚的选择性如下图所示。
 的选择性=(2×
的选择性=(2× 的物质的量/反应的
的物质的量/反应的 的物质的量)×100%
的物质的量)×100%
图中,温度高于265℃后甲醚选择性降低,从平衡的角度分析,其可能的原因是
您最近一年使用:0次
3 . 填空。
(1)下列事实不能用勒夏特列原理来解释的是___________ 。
A.高压有利于氢气与氮气合成氨
B.实验室中常用排饱和食盐水的方法收集Cl2
C.工业上生产硫酸时,充入过量的空气以提高SO2的转化率
D.H2、I2、HI平衡混合气体加压后颜色加深
E.压缩NO2与N2O4混合气,气体颜色变深
F.500℃左右比常况下更有利于合成氨
G.开启啤酒后,瓶中马上泛起大量泡沫
(2)某化学科研小组研究在其他条件不变时,改变某一条件对反应 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)

根据图像得出的结论,若正反应吸热,则T1___________ T2(填“>”“<”或“=”)。对于a、b、c三点:AB3的物质的量由大到小为___________ ,A2的平衡转化率由大到小为___________ ,B2的平衡转化率由大到小为___________ 。
(3)根据以下3个热化学方程式:
 △H1
△H1
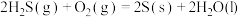 △H2
△H2
 △H3
△H3
△H1、△H2、△H3三者由大到小的顺序是___________ 。
(4)已知(NH4)2CO3捕碳的反应: 。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。

I.c点的逆反应速率和d点的正反应速率的大小关系为
___________  。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。
Ⅱ.b、c、d三点的平衡常数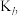 、
、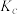 、
、 从大到小的顺序为
从大到小的顺序为___________ (填“>”、“=”或“<”)。
(1)下列事实不能用勒夏特列原理来解释的是
A.高压有利于氢气与氮气合成氨
B.实验室中常用排饱和食盐水的方法收集Cl2
C.工业上生产硫酸时,充入过量的空气以提高SO2的转化率
D.H2、I2、HI平衡混合气体加压后颜色加深

E.压缩NO2与N2O4混合气,气体颜色变深
F.500℃左右比常况下更有利于合成氨
G.开启啤酒后,瓶中马上泛起大量泡沫
(2)某化学科研小组研究在其他条件不变时,改变某一条件对反应
 的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
的化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)
根据图像得出的结论,若正反应吸热,则T1
(3)根据以下3个热化学方程式:
 △H1
△H1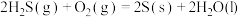 △H2
△H2 △H3
△H3△H1、△H2、△H3三者由大到小的顺序是
(4)已知(NH4)2CO3捕碳的反应:
 。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
。将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图。
I.c点的逆反应速率和d点的正反应速率的大小关系为

 。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。Ⅱ.b、c、d三点的平衡常数
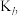 、
、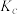 、
、 从大到小的顺序为
从大到小的顺序为
您最近一年使用:0次
名校
4 . 硝酸广泛用于化肥、化纤、医药、染料、橡胶等的制造,在国防工业、冶金工业、印染工业以及其他工业部门中,也是不可缺少的重要的化学试剂。
(1)工业生产中未直接在一个设备中将 催化氧化至
催化氧化至 ,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_____ 目的;
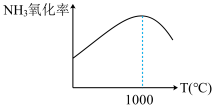
(2)实验发现,单位时间内 的氧化率[
的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后
]会随着温度的升高先增大后减小(如图所示),分析1000℃后 的氧化率减小的可能原因
的氧化率减小的可能原因_____
(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: (快)
(快) 


反应Ⅱ: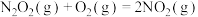 (慢)
(慢) 

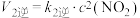
①一定条件下,反应 达到平衡状态,平衡常数
达到平衡状态,平衡常数
_____ (用含 、
、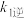 、
、 、
、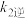 的代数式表示);
的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后 增大的倍数
增大的倍数_____ 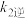 增大的倍数(填“大于”“小于”或“等于”)。
增大的倍数(填“大于”“小于”或“等于”)。
(Ⅱ)工业上也可以直接由 合成
合成 ,其中最关键的步骤为
,其中最关键的步骤为 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的 气体后密封并保持活塞位置不变。分别在
气体后密封并保持活塞位置不变。分别在 、
、 时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

(4)有关该过程说法正确的是_____
a.E、H两点对应的 的体积分数较大的为E点
的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深X
(5)下列表述能表示该反应已达平衡的是_____ (填序号)
a.活塞位置不变时,针管中的压强不再改变
b.针管内各物质的物质的量相等
c.针管内气体的平均摩尔质量不再改变
d.针管中温度、压强不变时,管内气体的密度不再改变
(6)求D点
_____ (不必化成小数)
(7)图像中C、E两点气体平均摩尔质量最大的点为_____ (填代号)。
(1)工业生产中未直接在一个设备中将
 催化氧化至
催化氧化至 ,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有(2)实验发现,单位时间内
 的氧化率[
的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后
]会随着温度的升高先增大后减小(如图所示),分析1000℃后 的氧化率减小的可能原因
的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
 (快)
(快) 


反应Ⅱ:
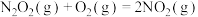 (慢)
(慢) 

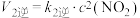
①一定条件下,反应
 达到平衡状态,平衡常数
达到平衡状态,平衡常数
 、
、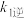 、
、 、
、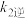 的代数式表示);
的代数式表示);②已知反应速率常数k随温度升高而增大,则升高温度后
 增大的倍数
增大的倍数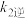 增大的倍数(填“大于”“小于”或“等于”)。
增大的倍数(填“大于”“小于”或“等于”)。(Ⅱ)工业上也可以直接由
 合成
合成 ,其中最关键的步骤为
,其中最关键的步骤为 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的
 气体后密封并保持活塞位置不变。分别在
气体后密封并保持活塞位置不变。分别在 、
、 时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的
 的体积分数较大的为E点
的体积分数较大的为E点b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深X
(5)下列表述能表示该反应已达平衡的是
a.活塞位置不变时,针管中的压强不再改变
b.针管内各物质的物质的量相等
c.针管内气体的平均摩尔质量不再改变
d.针管中温度、压强不变时,管内气体的密度不再改变
(6)求D点

(7)图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
名校
5 . 含碳物质的价值型转化,有利于“减碳”和可持续发展。结合相关信息,回答:
(1)相关的化学键键能数据如下:


_________________  。
。
下列有利于提高CO平衡转化率的措施有_________________ (填标号)。
a.增大压强 b.降低温度
c.提高原料气中 的比例 d.使用高效催化剂
的比例 d.使用高效催化剂
(2)已知将 、
、 催化重整为可用的化学品,对改善环境意义重大,某科研团队在密闭容器中进行“合成气催化重整”,反应的化学方程式为
催化重整为可用的化学品,对改善环境意义重大,某科研团队在密闭容器中进行“合成气催化重整”,反应的化学方程式为
①下列能说明该反应达到化学平衡状态的是_________________ 。
a.混合气体的平均相对分子质量不再变化 B.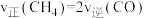
C.甲烷与氢气浓度比值不再变化 D.容器内混合气体的密度不再变化
②当投料比 时,
时, 的平衡转化率(
的平衡转化率( )与温度(T),初始压强(p)的关系如图所示。
)与温度(T),初始压强(p)的关系如图所示。
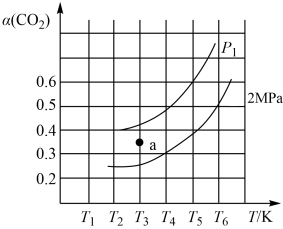
可知:压强
_________________ 2MPa(填“>”“<”或“=”);当温度为 、压强为2MPa时,a点时的v(逆)
、压强为2MPa时,a点时的v(逆)_________________ v(正)(填“>”“<”或“=”)
起始时向1L恒容容器中加入2mol 和2mol
和2mol  ,在温度为
,在温度为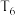 、初始压强为2MPa时反应,用压强表示该反应平衡常数的值的
、初始压强为2MPa时反应,用压强表示该反应平衡常数的值的
_____________ (分压=总压×物质的量百分数)。
(3)图为一种可以循环利用人体呼出的 并提供
并提供 的装置,总反应方程式为
的装置,总反应方程式为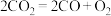 。写出阴极的电极反应:
。写出阴极的电极反应:_______________________
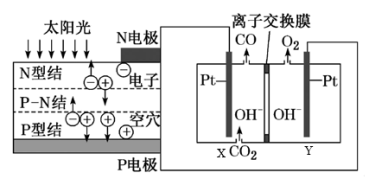
(1)相关的化学键键能数据如下:
化学键 | H-O | C≡O | C=O | H-H |
E/( | 463 | 1075 | 803 | 436 |


 。
。下列有利于提高CO平衡转化率的措施有
a.增大压强 b.降低温度
c.提高原料气中
 的比例 d.使用高效催化剂
的比例 d.使用高效催化剂(2)已知将
 、
、 催化重整为可用的化学品,对改善环境意义重大,某科研团队在密闭容器中进行“合成气催化重整”,反应的化学方程式为
催化重整为可用的化学品,对改善环境意义重大,某科研团队在密闭容器中进行“合成气催化重整”,反应的化学方程式为
①下列能说明该反应达到化学平衡状态的是
a.混合气体的平均相对分子质量不再变化 B.
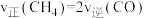
C.甲烷与氢气浓度比值不再变化 D.容器内混合气体的密度不再变化
②当投料比
 时,
时, 的平衡转化率(
的平衡转化率( )与温度(T),初始压强(p)的关系如图所示。
)与温度(T),初始压强(p)的关系如图所示。
可知:压强

 、压强为2MPa时,a点时的v(逆)
、压强为2MPa时,a点时的v(逆)起始时向1L恒容容器中加入2mol
 和2mol
和2mol  ,在温度为
,在温度为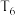 、初始压强为2MPa时反应,用压强表示该反应平衡常数的值的
、初始压强为2MPa时反应,用压强表示该反应平衡常数的值的
(3)图为一种可以循环利用人体呼出的
 并提供
并提供 的装置,总反应方程式为
的装置,总反应方程式为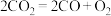 。写出阴极的电极反应:
。写出阴极的电极反应:
您最近一年使用:0次
名校
6 . 空间站利用“萨巴蒂尔反应”配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:
Ⅰ.萨巴蒂尔反应为:

(1)萨巴蒂尔反应的前三步历程图如下。其中物质吸附在催化剂表面用“。”标注, 表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会___________ (填“放出热量”或“吸收热量”)。

(2)在恒容密闭容器中加入 和
和 ,其分压分别20kPa和40kPa,一定条件下发生萨巴蒂尔反应。某时刻测得
,其分压分别20kPa和40kPa,一定条件下发生萨巴蒂尔反应。某时刻测得 的分压15kPa,
的分压15kPa, 的反应速率
的反应速率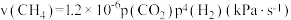 ,则该时刻
,则该时刻
___________  。
。
(3)航天器中可用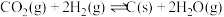
 ,然后电解水又得
,然后电解水又得 和
和 来处理
来处理 。现向一恒容密闭容器中通入
。现向一恒容密闭容器中通入 和
和 ,测得反应过程中压强随时间的变化如图中a所示,若其它条件不变,仅改变某一条件时,测得其压强随时间的变化如图中b所示。曲线a中,反应开始时,压强先变大的原因可能是
,测得反应过程中压强随时间的变化如图中a所示,若其它条件不变,仅改变某一条件时,测得其压强随时间的变化如图中b所示。曲线a中,反应开始时,压强先变大的原因可能是___________ ,曲线b改变的条件是___________ 。

Ⅱ.工业上利用甲酸的能量关系转换图如下:

(4)反应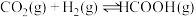 的焓变
的焓变
___________  。
。
(5)温度为 ℃时,将等物质的量的
℃时,将等物质的量的 和
和 充入体积为1L的密闭容器中发生反应:
充入体积为1L的密闭容器中发生反应: 。实验测得:
。实验测得: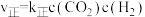 ,
, ,
, 、
、 为速率常数。则
为速率常数。则 ℃时,
℃时,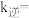
___________  ;温度为
;温度为 ℃时,
℃时,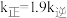 ,则
,则 ℃>
℃> ℃,理由是
℃,理由是___________ 。
 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:Ⅰ.萨巴蒂尔反应为:


(1)萨巴蒂尔反应的前三步历程图如下。其中物质吸附在催化剂表面用“。”标注,
 表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
(2)在恒容密闭容器中加入
 和
和 ,其分压分别20kPa和40kPa,一定条件下发生萨巴蒂尔反应。某时刻测得
,其分压分别20kPa和40kPa,一定条件下发生萨巴蒂尔反应。某时刻测得 的分压15kPa,
的分压15kPa, 的反应速率
的反应速率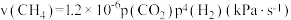 ,则该时刻
,则该时刻
 。
。(3)航天器中可用
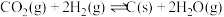
 ,然后电解水又得
,然后电解水又得 和
和 来处理
来处理 。现向一恒容密闭容器中通入
。现向一恒容密闭容器中通入 和
和 ,测得反应过程中压强随时间的变化如图中a所示,若其它条件不变,仅改变某一条件时,测得其压强随时间的变化如图中b所示。曲线a中,反应开始时,压强先变大的原因可能是
,测得反应过程中压强随时间的变化如图中a所示,若其它条件不变,仅改变某一条件时,测得其压强随时间的变化如图中b所示。曲线a中,反应开始时,压强先变大的原因可能是
Ⅱ.工业上利用甲酸的能量关系转换图如下:

(4)反应
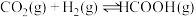 的焓变
的焓变
 。
。(5)温度为
 ℃时,将等物质的量的
℃时,将等物质的量的 和
和 充入体积为1L的密闭容器中发生反应:
充入体积为1L的密闭容器中发生反应: 。实验测得:
。实验测得: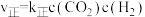 ,
, ,
, 、
、 为速率常数。则
为速率常数。则 ℃时,
℃时,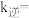
 ;温度为
;温度为 ℃时,
℃时,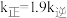 ,则
,则 ℃>
℃> ℃,理由是
℃,理由是
您最近一年使用:0次
名校
解题方法
7 . 1,6−己二醇是一种重要的化工原料,与乙二醇相比,用1,6−己二醇为原料制备的聚酯具有更为优异的柔韧性和抗腐蚀性。工业上利用己二酸二甲酯加氢制备1,6−己二醇,该反应的化学方程式如图:
 (g)+4H2(g)→
(g)+4H2(g)→ (g)+2CH3OH(g) ΔH。
(g)+2CH3OH(g) ΔH。
(1)已知:
计算上述反应的△H=___ ;此反应自发进行的条件是____ (填“高温易自发”“低温易自发”或“任何温度都能自发”)。
(2)将组成(物质的量分数)为4n%H2(g)、n% (g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时
(g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时 (g)的转化率为=
(g)的转化率为=____ (用p、q的代数式表示,下同),平衡常数Kp=____ (以分压表示,分压=总压×物质的量分数)。
(3)科研小组在高压反应釜中进行催化加氢反应,对己二酸二甲酯制备1,6−己二醇的工艺条件进行了研究。图甲和图乙为此反应在相同时间时,反应压力、反应温度与反应物的转化率和1,6−己二醇选择性的变化关系。

已知,选择性= ×100%。
×100%。
①由图可知,在压强为27MPa时,己二酸二甲酯制备1,6−己二醇应选择的合适温度为____ ;选择此温度的理由是____ ;当260℃时,转化率随着压强增大而不断增大的原因是____ 。
②图丙为反应时间与加氢反应时反应物的转化率和选择性的关系。

综合考虑,反应时间控制在5h左右较为合适。此时1,6−己二醇的产率为____ 。
 (g)+4H2(g)→
(g)+4H2(g)→ (g)+2CH3OH(g) ΔH。
(g)+2CH3OH(g) ΔH。(1)已知:
化学键 | C=O | C−O | C−H | C−C | O−H | H−H |
| 键能/ kJ∙mol−1 | 745 | 358 | 413 | 347 | 467 | 436 |
(2)将组成(物质的量分数)为4n%H2(g)、n%
 (g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时
(g)的气体通入刚性密闭反应器中,在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时 (g)的转化率为=
(g)的转化率为=(3)科研小组在高压反应釜中进行催化加氢反应,对己二酸二甲酯制备1,6−己二醇的工艺条件进行了研究。图甲和图乙为此反应在相同时间时,反应压力、反应温度与反应物的转化率和1,6−己二醇选择性的变化关系。

已知,选择性=
 ×100%。
×100%。①由图可知,在压强为27MPa时,己二酸二甲酯制备1,6−己二醇应选择的合适温度为
②图丙为反应时间与加氢反应时反应物的转化率和选择性的关系。

综合考虑,反应时间控制在5h左右较为合适。此时1,6−己二醇的产率为
您最近一年使用:0次
2022-04-26更新
|
1201次组卷
|
7卷引用:东北育才学校超常教育实验部(少32届)2022届高三第十次模拟考试化学试题
东北育才学校超常教育实验部(少32届)2022届高三第十次模拟考试化学试题福建省百校2021-2022学年高三下学期4月联合测评化学试题(已下线)押全国卷理综第28题 化学反应原理-备战2022年高考化学临考题号押题(课标全国卷)河北省衡水市2022届高考二模化学试题山东省东营市胜利第一中学2022届高三仿真演练押题化学试题吉林省吉林市第一中学2021-2022学年高二下学期6月月考化学试题(理科创新班)(已下线)T17-原理综合题
名校
8 . 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上用天然气为原料,分为两阶段制备甲醇:
(Ⅰ)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(Ⅱ)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)在刚性容器中制备合成气,下列说法中能说明此反应达到平衡状态的是_______ 。
A.体系的压强不再发生变化
B.生成1mol CH4的同时消耗3mol H2
C.各组分的物质的量浓度不再改变
D.体系的密度不再发生变化
E.反应速率v(CH4)=3v(H2)
(2)在一容积可变的密闭容器中充入10mol CO和20mol H2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
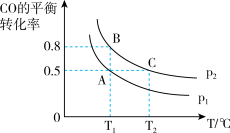
①比较A、B 两点压强大小PA_______ PB(填“>、<、=”)
②若达到化学平衡状态 A 时,容器的体积为 10L,如果反应开始时仍充入 10mol CO和20mol H2,则在平衡状态 B 时,容器的体积V(B)=_______ L;
(3)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①二氧化碳加氢合成水蒸气和甲醇,CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g)该反应在低温下可自发进行,则ΔH_______ 0(填“>、=、<”)
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示;a~d点中反应可能处于平衡状态的点是_______ ;CO2的转化率a 点比c点高的原因是_______ 。
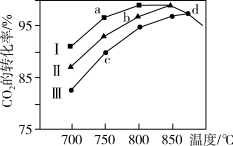
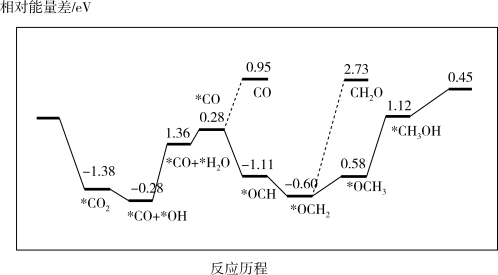
③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示;容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为_______ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______ (填字母)的能量变化。
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3 D.*OCH3→*CH3OH
(Ⅰ)制备合成气:CH4(g)+H2O(g) ⇌CO(g)+3H2(g) ΔH= +206.0kJ•mol-1
(Ⅱ)合成甲醇:CO(g)+2H2(g)⇌CH3OH(g) ΔH= -90.67kJ•mol-1
(1)在刚性容器中制备合成气,下列说法中能说明此反应达到平衡状态的是
A.体系的压强不再发生变化
B.生成1mol CH4的同时消耗3mol H2
C.各组分的物质的量浓度不再改变
D.体系的密度不再发生变化
E.反应速率v(CH4)=3v(H2)
(2)在一容积可变的密闭容器中充入10mol CO和20mol H2合成甲醇,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。

①比较A、B 两点压强大小PA
②若达到化学平衡状态 A 时,容器的体积为 10L,如果反应开始时仍充入 10mol CO和20mol H2,则在平衡状态 B 时,容器的体积V(B)=
(3)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①二氧化碳加氢合成水蒸气和甲醇,CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g)该反应在低温下可自发进行,则ΔH
②研究表明在二氧化碳合成甲醇的原料气的反应中,保持其它条件不变,采用Ⅰ、Ⅱ、Ⅲ三种催化剂,反应进行相同时间后,CO2的转化率随反应体系的温度变化如图所示;a~d点中反应可能处于平衡状态的点是

③最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示;容易得到的副产物有 CO 和CH2O,其中相对较少的副产物为
A.*CO → *OCH B.*CO+*OH→*CO+*H2O
C.*OCH2→*OCH3 D.*OCH3→*CH3OH

您最近一年使用:0次



