1 . 硫及其化合物在生产、生活中有广泛应用。回答下列问题:
Ⅰ.已知:①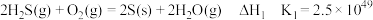
②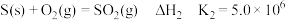
(1)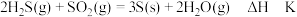 ,根据上述信息推知,
,根据上述信息推知,
___________ ,
___________ (填具体数值)。
Ⅱ.羰基硫 是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以
是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以 固体为催化剂,
固体为催化剂, 分别与
分别与 反应制备
反应制备 的反应如下:
的反应如下:
 ;
;
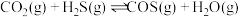 。
。
(2)一定温度下,向恒容密闭容器中充入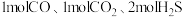 气体,加入适量的
气体,加入适量的 固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
Ⅲ.利用 和
和 反应制备
反应制备 。
。
已知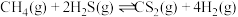 分以下两步进行:
分以下两步进行:
(a)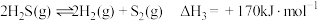
(b)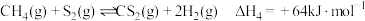
(3) 温度下,保持总压强为
温度下,保持总压强为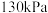 ,向反应器中充入
,向反应器中充入 和
和 ,只发生反应a,测得
,只发生反应a,测得 平衡转化率与投料比
平衡转化率与投料比 的关系如图所示。
的关系如图所示。 增大,
增大, 平衡转化率增大的原因是
平衡转化率增大的原因是___________ ; 温度下,该反应的平衡常数
温度下,该反应的平衡常数
___________  。(提示:用分压计算的平衡常数叫压强平衡常数
。(提示:用分压计算的平衡常数叫压强平衡常数 ,分压等于总压×物质的量分数。)
,分压等于总压×物质的量分数。)
(4)向一密闭容器中通入 和
和 ,同时通入一定量的
,同时通入一定量的 稀释。常压下,不同温度下反应相同时间后,测得
稀释。常压下,不同温度下反应相同时间后,测得 和
和 的体积分数如图所示。
的体积分数如图所示。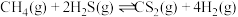 能自发进行的条件是
能自发进行的条件是___________ (填标号)。
a.较低温度 b.较高温度 c.任何温度
②其他条件不变,在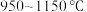 范围内,
范围内, 的体积分数随温度的变化趋势与图
的体积分数随温度的变化趋势与图___________ (填标号)相符。
Ⅰ.已知:①
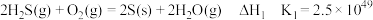
②
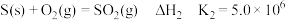
(1)
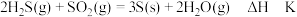 ,根据上述信息推知,
,根据上述信息推知,

Ⅱ.羰基硫
 是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以
是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以 固体为催化剂,
固体为催化剂, 分别与
分别与 反应制备
反应制备 的反应如下:
的反应如下: ;
;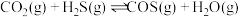 。
。(2)一定温度下,向恒容密闭容器中充入
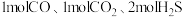 气体,加入适量的
气体,加入适量的 固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。| A.气体总压强不变时反应达到平衡状态 |
B.平衡时混合气体中 体积分数的最大值为50% 体积分数的最大值为50% |
C.达到平衡时再充入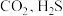 的平衡转化率增大 的平衡转化率增大 |
D.其他条件相同,使用纳米 比使用颗粒 比使用颗粒 的反应速率大 的反应速率大 |
Ⅲ.利用
 和
和 反应制备
反应制备 。
。已知
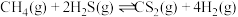 分以下两步进行:
分以下两步进行:(a)
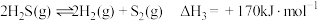
(b)
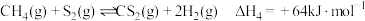
(3)
 温度下,保持总压强为
温度下,保持总压强为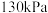 ,向反应器中充入
,向反应器中充入 和
和 ,只发生反应a,测得
,只发生反应a,测得 平衡转化率与投料比
平衡转化率与投料比 的关系如图所示。
的关系如图所示。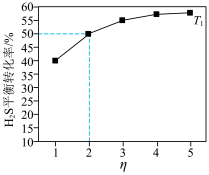
 增大,
增大, 平衡转化率增大的原因是
平衡转化率增大的原因是 温度下,该反应的平衡常数
温度下,该反应的平衡常数
 。(提示:用分压计算的平衡常数叫压强平衡常数
。(提示:用分压计算的平衡常数叫压强平衡常数 ,分压等于总压×物质的量分数。)
,分压等于总压×物质的量分数。)(4)向一密闭容器中通入
 和
和 ,同时通入一定量的
,同时通入一定量的 稀释。常压下,不同温度下反应相同时间后,测得
稀释。常压下,不同温度下反应相同时间后,测得 和
和 的体积分数如图所示。
的体积分数如图所示。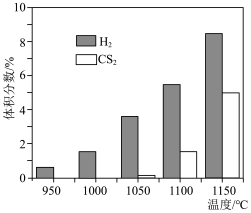
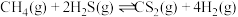 能自发进行的条件是
能自发进行的条件是a.较低温度 b.较高温度 c.任何温度
②其他条件不变,在
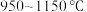 范围内,
范围内, 的体积分数随温度的变化趋势与图
的体积分数随温度的变化趋势与图A.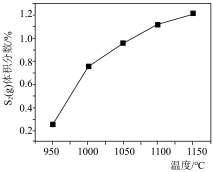 B.
B.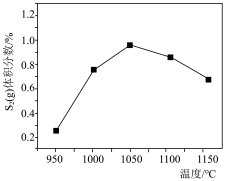
C.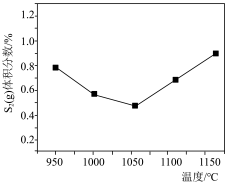 D.
D.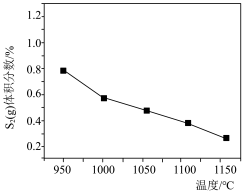
您最近一年使用:0次
名校
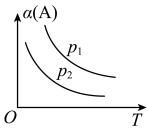
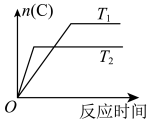
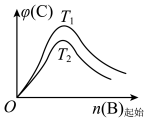
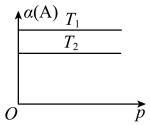
2 . 改变某条件对反应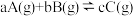 的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,
的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率,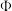 表示体积分数)。根据图象,下列判断正确的是
表示体积分数)。根据图象,下列判断正确的是
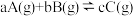 的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,
的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率,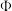 表示体积分数)。根据图象,下列判断正确的是
表示体积分数)。根据图象,下列判断正确的是
|
|
| 反应I | 反应Ⅱ |
|
|
| 反应Ⅲ | 反应Ⅳ |
A.反应I:若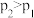 ,则此反应可以在任何温度下均自发进行 ,则此反应可以在任何温度下均自发进行 |
B.反应Ⅱ:此反应的 ,且 ,且 |
C.反应Ⅲ: 且 且 或 或 且 且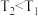 |
D.反应Ⅳ:在恒压条件下,若起始时充入反应物的物质的量相等且该反应为放热反应,则平衡时体积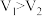 |
您最近一年使用:0次
3 . 已知:反应Ⅰ.
反应Ⅱ.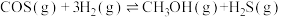
在恒压条件下,按 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。
投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。

反应Ⅱ.
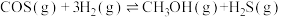
在恒压条件下,按
 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。
投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。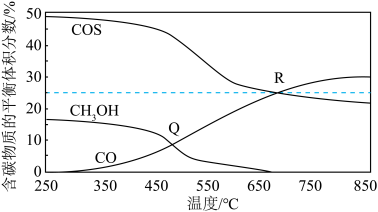
| A.反应Ⅱ高温易自发进行 |
| B.加入合适的催化剂可使Q点上移 |
C.随着温度的升高, 的转化率减小 的转化率减小 |
| D.R点反应Ⅰ的平衡常数K的为1 |
您最近一年使用:0次
4 . 氢气可将 还原为甲烷(
还原为甲烷( ):
):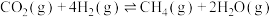 ,科学家研究在催化剂表面上
,科学家研究在催化剂表面上 与
与 反应的前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法正确的是
反应的前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法正确的是
 还原为甲烷(
还原为甲烷( ):
):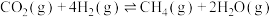 ,科学家研究在催化剂表面上
,科学家研究在催化剂表面上 与
与 反应的前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法正确的是
反应的前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法正确的是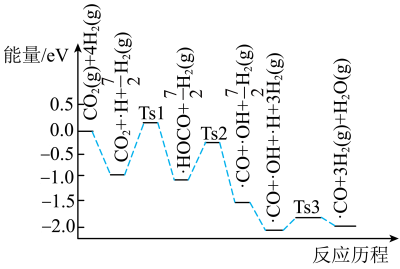
A. 是极性分子,能溶于水 是极性分子,能溶于水 |
| B.从起始到Ts1历程中发生了非极性共价键的断裂和形成 |
| C.该转化反应的速率取决于Ts1的能垒 |
| D.使用催化剂可以改变反应历程,使非自发反应反应历程 |
您最近一年使用:0次
名校
解题方法
5 . 利用甲烷可以除去 ,反应为
,反应为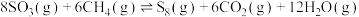 。下列说法正确的是
。下列说法正确的是
 ,反应为
,反应为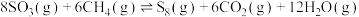 。下列说法正确的是
。下列说法正确的是A.上述反应的 |
B.上述反应的化学平衡常数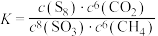 |
C.及时分离出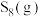 ,正反应速率增大,平衡向正反应方向移动 ,正反应速率增大,平衡向正反应方向移动 |
D.上述反应中生成1mol  ,转移电子的数目约为 ,转移电子的数目约为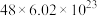 |
您最近一年使用:0次
解题方法
6 . 我国科研团队研究 电催化合成氨反应[
电催化合成氨反应[ △H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
△H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
 电催化合成氨反应[
电催化合成氨反应[ △H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
△H<0]时,发现不同电解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法不正确的是
| A.反应放热是合成氨反应自发进行的主要助力 |
B.选用 作电解质的反应速率比选用 作电解质的反应速率比选用 的快 的快 |
C. 先吸附于催化剂表面再参加合成氨反应 先吸附于催化剂表面再参加合成氨反应 |
| D.形成Li-S键合作用时,合成氨反应的△H的绝对值较小 |
您最近一年使用:0次
7 . 我国科学家研发出一种新型双温催化剂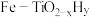 ,该催化剂催化
,该催化剂催化 和
和 合成
合成 (反应体系温度为495℃)的原理如图所示,下列分析错误的是
(反应体系温度为495℃)的原理如图所示,下列分析错误的是
 ,该催化剂催化
,该催化剂催化 和
和 合成
合成 (反应体系温度为495℃)的原理如图所示,下列分析错误的是
(反应体系温度为495℃)的原理如图所示,下列分析错误的是
A.“热 ”上的变化属于焓增、熵增的变化 ”上的变化属于焓增、熵增的变化 |
B.“热 ”有利于 ”有利于 快速转化为N 快速转化为N |
C.“冷 ”低于体系温度,有利于提高合成氨反应速率 ”低于体系温度,有利于提高合成氨反应速率 |
| D.该催化剂能较好地解决传统合成氨工艺中存在的反应速率和平衡产率的矛盾 |
您最近一年使用:0次
解题方法
8 . 在葡萄糖水溶液中,链状结构与环状结构的平衡关系及百分含量如下:不正确 的是
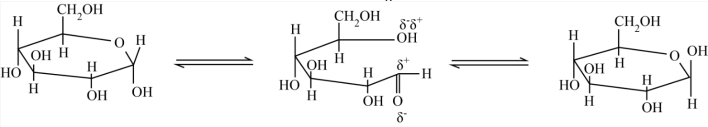

| A.链状葡萄糖成环是-OH与-CHO发生加成反应的结果 |
B.链状葡萄糖成环反应的 , , |
| C.链状葡萄糖成环后,分子中多了一个手性碳原子 |
D.水溶液中,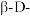 吡喃葡萄糖比 吡喃葡萄糖比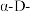 吡喃葡萄糖稳定 吡喃葡萄糖稳定 |
您最近一年使用:0次
名校
解题方法
9 . 科学家对 负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定
负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定 在不同催化剂上发生还原反应生成
在不同催化剂上发生还原反应生成 的自由能如图所示,数字标注的为吉布斯自由能变化值。
的自由能如图所示,数字标注的为吉布斯自由能变化值。
 负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定
负载的不同过渡金属催化剂上产物活性和选择性的不同进行了探究。测定 在不同催化剂上发生还原反应生成
在不同催化剂上发生还原反应生成 的自由能如图所示,数字标注的为吉布斯自由能变化值。
的自由能如图所示,数字标注的为吉布斯自由能变化值。
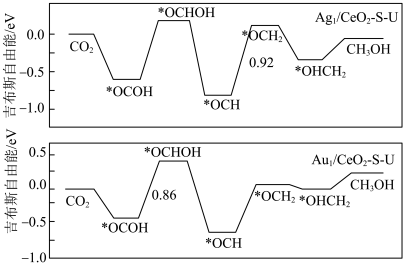
A.由图可知, 在不同催化剂上发生还原反应生成 在不同催化剂上发生还原反应生成 的吉布斯自由能相同 的吉布斯自由能相同 |
B. 在三种催化剂上发生还原反应生成 在三种催化剂上发生还原反应生成 的决速步骤均相同 的决速步骤均相同 |
| C.中间体的吸附构型与催化剂的活性和选择性存在直接的关系 |
D. 发生还原反应的过程中,碳氧双键均断裂,且氧原子均生成甲醇 发生还原反应的过程中,碳氧双键均断裂,且氧原子均生成甲醇 |
您最近一年使用:0次
解题方法
10 . 根据下列有关实验方案设计和现象,所得结论不正确 的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将打磨过的铁铜合金放在氨水中一段时间 | 溶液变为深蓝色 | 可能是铜在氨水中发生吸氧腐蚀 |
| B | 向FeCl3溶液中滴加KSCN溶液,再加入少量Cu粉 | 溶液先变成血红色,加入Cu粉后,血红色变浅 | 与SCN-的配位能力: |
| C | 将 和NH4NO3固体混合并用玻璃棒快速搅拌 和NH4NO3固体混合并用玻璃棒快速搅拌 | 有刺激性气味的气体产生,并伴随降温 | 该反应能发生的主要原因是熵增 |
| D | 用精密pH试纸测定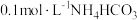 溶液的pH值 溶液的pH值 | 测得pH为7.8 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次