解题方法
1 . 用实验确定某酸HA是否为弱电解质,两位同学的方案如下:
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是____ 。
(2)甲方案中,若测得溶液的pH____ (填“>”“<”或“=”)1,则可说明HA是弱电解质。
(3)乙方案中,能说明HA是弱电解质的现象是____ (填字母序号)。
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价____ 。
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述_____ 。
甲:①称取一定质量的HA,配制0.1mol•L-1的溶液100mL;②用pH计测出该溶液的pH,根据测定结果即可判断HA是否为弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸分别配制pH=2的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液于两支试管中,同时加入相同纯度的锌粒,根据观察到的实验现象即可判断HA是否为弱电解质。
(1)在两个方案的步骤①中,都要用到的定量仪器是
(2)甲方案中,若测得溶液的pH
(3)乙方案中,能说明HA是弱电解质的现象是
A.装盐酸的试管中放出H2的速率较大
B.装HA溶液的试管中放出H2的速率较大
C.两支试管中产生气体的速率一样大
(4)请你对两种方案的可行性作出评价
(5)请你再设计一个合理而比较容易进行的实验方案(药品可任取),并作简明扼要的表述
您最近一年使用:0次
2022-11-25更新
|
84次组卷
|
2卷引用:苏教2020版选择性必修1专题3第四单元 沉淀溶解平衡课后习题
9-10高二下·江西·期中
名校
2 . 将0.1mol•L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起的变化是
| A.溶液的pH增大 | B.CH3COOH的电离度变大 |
| C.溶液中c(OH-)减小 | D.溶液的导电能力减弱 |
您最近一年使用:0次
2022-11-25更新
|
1360次组卷
|
42卷引用:苏教2020版选择性必修1专题3第四单元 沉淀溶解平衡课后习题
苏教2020版选择性必修1专题3第四单元 沉淀溶解平衡课后习题3.4.1沉淀溶解平衡原理 课中(已下线)09~10年江西四校高二下学期期中联考化学卷(已下线)2011-2012学年福建省罗源一中高二上学期期末考试化学试卷(已下线)2010-2011学年安徽省怀宁县高河中学高二下学期第二次月考化学试卷(已下线)2012-2013学年福建省罗源县第一中学高二第二次月考化学试卷(已下线)2012-2013学年广东省实验中学高二上学期期中化学试卷(已下线)2012-2013学年浙江省桐乡一中高二下学期期中考试化学试卷(已下线)2013-2014学年内蒙古包头三十三中高二下学期期中考试理科化学试卷(已下线)2014届内蒙古包钢一中高二下学期期中Ⅰ考试化学试卷2015-2016学年山东枣庄八中南校区高二12月月考化学卷2015-2016学年山东省临沂一中高二上学期期中测试化学试卷2015-2016学年黑龙江省海林林业局一中高二上期末考试化学试卷2016-2017学年河北省张家口万全中学高二上第一次月考化学试卷河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第二次月考化学试题吉林省东北师范大学附属中学2017-2018学年高二上学期期末考试化学试题福建省永春县第一中学2017-2018高二下学期期末考试化学试题上海市复旦大学附中2017-2018学年高二上学期期中考试化学试题江西省南昌市第二中学2019-2020学年高二上学期期中考试化学试题江西省南昌市顶级名校2019-2020学年高二上学期12月月考化学考试题北京市海淀实验中学2019-2020学年高二下学期期末考试化学试题广西壮族自治区贺州市桂梧高中2020-2021学年高二上学期(12月)第二次月考化学试题青海省湟川中学2019-2020学年高二上学期期中考试化学试题第27届(2013年)高中学生化学竞赛天津市预赛试题上海市控江中学2020-2021学年高二下学期等级班期中考试化学试题陕西省安康市六校联考2021-2022学年高二上学期期末考试化学试题(已下线)第07练 电离平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)吉林省长春市北师大附属学校2021-2022学年高二上学期期末考试化学试题湖南省岳阳市华容县2021-2022学年高二上学期期末教学质量监测化学试题江苏省淮安市涟水县第一中学2021-2022学年高二下学期第二次阶段检测化学试题安徽省肥东凯悦中学2021-2022学年高二上学期第三次自主检测化学试题广东省华南师范大学附属中学2022-2023学年高二上学期1月期末化学试题陕西省汉中市乡县第一中学2023-2024学年高二上学期10月月考化学试题(已下线)2013届上海市金山区高三上学期期末考试化学试卷2016届上海市杨浦区高三上学期期末3+1质量调研化学试卷上海市闵行三中2018.-2019学年高三期中考试试卷吉林省吉林市普通高中2020届高三上学期第一次调研测试化学试题上海市静安区2020届高三上学期第一次模拟考试化学试题2020届高三化学二轮冲刺新题专练——弱电解质电解常数、电离度及其应用(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)
名校
3 . 在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。
(1)草酸( )是一种二元弱酸。写出它在水中的电离方程式:
)是一种二元弱酸。写出它在水中的电离方程式:_______ 。
(2)试比较 草酸溶液中
草酸溶液中 、
、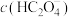 、
、 的大小:
的大小:_______ 。
(3)要使溶液中 的电离程度增大,可以采取的措施是
的电离程度增大,可以采取的措施是_______ 。
(1)草酸(
 )是一种二元弱酸。写出它在水中的电离方程式:
)是一种二元弱酸。写出它在水中的电离方程式:(2)试比较
 草酸溶液中
草酸溶液中 、
、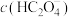 、
、 的大小:
的大小:(3)要使溶液中
 的电离程度增大,可以采取的措施是
的电离程度增大,可以采取的措施是
您最近一年使用:0次
2022-11-25更新
|
198次组卷
|
3卷引用:苏教2020版选择性必修1专题3第一单元 弱电解质的电离平衡课后习题
4 . 电离平衡常数(用 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。
(1)水是极弱的电解质, 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是_______ ,温度升高, 的值
的值_______ (填“变大”“变小”或“不变”)。
(2) 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性_______ ,当用蒸馏水稀释 醋酸时,醋酸的
醋酸时,醋酸的
_______ (填“变大”“变小”或“不变”)。
(3)常温下, 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为_______ , 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为_______ 。
(4)常温下,4种酸的电离平衡常数如下:
①物质的量浓度相同的HF、 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是_______ 。
② 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是_______ 。
 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。(1)水是极弱的电解质,
 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是 的值
的值(2)
 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性 醋酸时,醋酸的
醋酸时,醋酸的
(3)常温下,
 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为(4)常温下,4种酸的电离平衡常数如下:
| 化学式 | HF |  |  | HClO |
| 电离平衡常数 | 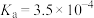 |  |   | 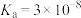 |
 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是②
 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是
您最近一年使用:0次
5 . 一水合氨的电离方程式为 。若在氨水中加入下表中的物质(保持温度不变),一水合氨的电离平衡以及平衡时
。若在氨水中加入下表中的物质(保持温度不变),一水合氨的电离平衡以及平衡时 、
、 如何变化?请填写下表。
如何变化?请填写下表。
 。若在氨水中加入下表中的物质(保持温度不变),一水合氨的电离平衡以及平衡时
。若在氨水中加入下表中的物质(保持温度不变),一水合氨的电离平衡以及平衡时 、
、 如何变化?请填写下表。
如何变化?请填写下表。| 加入的物质 |  |  | 电离平衡移动方向 |
 | |||
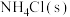 | |||
| NaOH(s) | |||
| 浓盐酸 |
您最近一年使用:0次
6 . 用 醋酸溶液进行导电性实验,发现灯泡亮度很低;用
醋酸溶液进行导电性实验,发现灯泡亮度很低;用 氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。_________
 醋酸溶液进行导电性实验,发现灯泡亮度很低;用
醋酸溶液进行导电性实验,发现灯泡亮度很低;用 氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
氨水进行导电性实验,发现灯泡亮度同样很低。但若将两种溶液等体积混合再进行导电性实验,灯泡亮度却显著增加。请分析其中的原因。
您最近一年使用:0次
名校
解题方法
7 . 下列各组物质中都是强电解质的是
| A.HF、HCl、BaSO4 | B.NH4F、CH3COONa、Na2S |
| C.NaOH、Ca(OH)2、NH3·H2O | D.HClO、NaF、Ba(OH)2 |
您最近一年使用:0次
2022-11-13更新
|
101次组卷
|
9卷引用:人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡 课时1 弱电解质的电离平衡
人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡 课时1 弱电解质的电离平衡选择性必修1(SJ)专题3第一单元课时1 弱电解质的电离平衡2015-2016学年重庆市杨家坪中学高二上学期第一次月考化学试卷广东省东莞市第四高级中学2020-2021学年高二上学期期中考试化学试题吉林省长春市第二实验中学2021-2022学年高二上学期10月月考化学试题福建省福州高级中学2021-2022学年高二上学期期末化学考试题广东省肇庆市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)2022年浙江省6月高考真题变式题1-10天津市外国语大学附属外国语学校2022~2023学年高一上学期阶段性检测化学试题
名校
8 . 25℃时,三种酸的电离平衡常数如下:
(1)一般情况下,当温度升高时,
_______ (填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力最强的是_______ (填序号);
a、 b、
b、 c、
c、 d、
d、
(3)下列反应不能发生的是_______ (填序号)
a.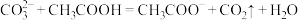
b.
c.
d.
(4)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是_______ (填序号);
a.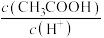 b.
b. c.
c. d.
d.
| 化学式 |  |  |  |
| 电离平衡常数 |  |  , , |  |
(1)一般情况下,当温度升高时,

(2)下列四种离子结合质子能力最强的是
a、
 b、
b、 c、
c、 d、
d、
(3)下列反应不能发生的是
a.
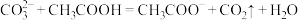
b.

c.

d.

(4)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
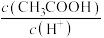 b.
b. c.
c. d.
d.
您最近一年使用:0次
2022-11-08更新
|
354次组卷
|
5卷引用:章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)
(已下线)章末培优3 专题3 水溶液中的离子反应-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)江西省遂川中学2021-2022学年高二上学期第二次月考化学(B卷)试题天津市第二十一中学2022-2023学年高二上学期期中调研化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题江西省高安中学2020-2021学年高一上学期第一次月考(A)化学试题
名校
解题方法
9 . 下列关于醋酸性质的描述,不能证明它是弱电解质的是
| A.0.1mol·L-1的醋酸溶液中H+浓度约为10-3mol·L-1 |
| B.醋酸溶液中存在CH3COOH分子 |
| C.CH3COONa溶液pH大于7 |
| D.5mL0.1mol·L-1的醋酸溶液与5mL0.1mol·L-1的KOH溶液恰好完全中和 |
您最近一年使用:0次
2022-11-02更新
|
334次组卷
|
5卷引用:第三章 第一节 弱电解质的电离(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)
(已下线)第三章 第一节 弱电解质的电离(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题四川省巴中市恩阳区2022-2023学年高二上学期1月期末化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)
13-14高一上·重庆·期末
名校
解题方法
10 . 下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
| A | B | C | D | |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| 非电解质 | C12H22O11(蔗糖) | BaSO4 | C2H5OH | H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-30更新
|
485次组卷
|
66卷引用:鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第1节 水与水溶液
鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第1节 水与水溶液(已下线)3.1 弱电解质的电离(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)3.1.1 强电解质与弱电解质 弱电解质的电离平衡(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)2015-2016学年湖南省娄底市湘中名校高二上期末理化学试卷2015-2016学年甘肃省嘉峪关市第一中学高二上学期期末化学试卷2016-2017学年黑龙江哈尔滨师大附中高二上期中化学卷河北省邯郸三中2017-2018学年高二上学期第二次月考化学试卷陕西省黄陵中学2017-2018学年高二(普通班)上学期期末考试化学试题新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题黑龙江省伊春市第二中学2017-2018学年高二下学期期末考试化学试题(已下线)2018年9月30日《每日一题》人教选修4每周一测甘肃省武威市第十八中学2018-2019学年高二上学期期末考试化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高二上学期期末考试化学试题【全国百强校】四川省南充市阆中中学2018-2019学年高二下学期3月月考化学试题【全国百强校】内蒙古杭锦后旗奋斗中学2018-2019学年高二下学期第一次月考化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题甘肃省静宁县第一中学2019-2020学年高二上学期第一次月考化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期期中考试(A班)化学试题江西省上饶市上饶中学2019-2020学年高二上学期第二次月考化学(理科实验、重点)试题河北省邯郸市大名县第一中学2019-2020学年高二上学期12月月考化学试题(普通班)(已下线)【南昌新东方】2019 南大附中 高二上 期末云南省玉溪市峨山彝族自治县第一中学2019-2020学年高二下学期期中考试化学试题内蒙古自治区呼和浩特市内蒙古师范大学附属中学2019-2020学年高二上学期期中考试化学试题(已下线)1.2.1 电解质的电离-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)人教版(2019)高一必修第一册 第一章 物质及其变化 第二节 离子反应 教材帮内蒙古通辽市开鲁县第一中学2020-2021学年高二上学期第一次月考化学试题陕西省延安市吴起高级中学2020-2021学年高二上学期第一次月考化学试题辽宁省铁岭市开原市第二高级中学2020-2021学年高二上学期期初考试化学试题吉林省长春市第二十九中学2020-2021学年高二上学期第二学程考试化学(理)试题新疆昌吉州教育共同体2020-2021学年高二上学期期中考试化学试题甘肃省白银市会宁县第一中学2020-2021学年高二上学期第二次月考化学试题吉林省长春市第二十九中学2020-2021学年高二上学期期末考试化学试题吉林省汪清县第六中学2020-2021学年高二上学期期末考试化学试题江西省鄱阳县第一中学2019-2020学年高二上学期第二次检测化学试题湖北省新高考联考协作体2021-2022学年高二上学期10月联考化学试题江西省南昌市八一中学、洪都中学等4校2021-2022学年高二上学期期中联考化学试题江西省九校2021-2022学年高二上学期期中联考化学试题云南省弥勒市第二中学2020-2021学年高二下学期期中考试化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第二学程考试化学试题四川省内江市威远中学校2021-2022学年高二下学期第一次月考化学试题黑龙江省双鸭山市集贤县一中、四中等2021-2022学年高二下学期期末考试化学试题(已下线)1.2.1 电解质和非电解质-同步学习必备知识黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题安徽省怀宁县第二中学2021-2022学年高二上学期期中考试化学试题辽宁省新民市第一高级中学2021-2022学年高二上学期10月月考化学试题四川省广安市育才学校2022-2023学年高二上学期11月期中考试化学试题湖南省常德市西洞庭管理区第一中学2022-2023学年高二上学期第二次月考化学试题广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题(已下线)2012-2013学年重庆市重庆一中高一上学期期末考试化学试卷(已下线)2014年高考化学苏教版总复习 8-1 弱电解质的电离平衡练习卷2016届山东省枣庄第三中学高三上10月阶段质检化学试卷2016届辽宁省沈阳东北育才学校高三上第三次模拟化学试卷辽宁省阜新二高2017-2018学年高一上学期第二次月考化学试卷(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化 第2讲 离子反应和离子方程式【教学案】(已下线)2019届高考热点题型和提分秘籍 第二章 化学物质及其变化 第2讲 离子反应 (教学案)重庆市云阳江口中学校2020届高三上学期第一次月考化学试题安徽省滁州市定远县育才学校2019-2020学年高一上学期期中考试(实验班)化学试题河南省洛阳市第一高级中学2021届高三9月月考化学试题(已下线)练习1 离子反应-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(已下线)第04讲 离子反应 离子方程式(精讲)-2022年一轮复习讲练测山东省济宁市微山县第二中学2021-2022学年高一上学期第一学段考试化学试题上海交通大学附属中学2021-2022学年高一下学期开学摸底考试化学试题上海市风华中学2021-2022学年高一上学期期中考试化学试题(已下线)第2章能力提升测评-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)新疆阿克苏地区阿瓦提县第四中学2022-2023学年高一上学期第二次诊断性测试化学试题黑龙江省佳木斯市第十二中学2022-2023学年高三上学期开学考试化学试题



