名校
1 .  为二元弱酸,常温下将
为二元弱酸,常温下将 的NaOH溶液滴入20mL
的NaOH溶液滴入20mL 的NaHA溶液中,溶液中
的NaHA溶液中,溶液中 (或
(或 )的分布系数
)的分布系数 、加入NaOH溶液的体积V与pH的关系如图所示[已知:
、加入NaOH溶液的体积V与pH的关系如图所示[已知: ]。下列叙述正确的是
]。下列叙述正确的是
 为二元弱酸,常温下将
为二元弱酸,常温下将 的NaOH溶液滴入20mL
的NaOH溶液滴入20mL 的NaHA溶液中,溶液中
的NaHA溶液中,溶液中 (或
(或 )的分布系数
)的分布系数 、加入NaOH溶液的体积V与pH的关系如图所示[已知:
、加入NaOH溶液的体积V与pH的关系如图所示[已知: ]。下列叙述正确的是
]。下列叙述正确的是
| A.到达m点需要加入NaOH溶液的体积大于10mL |
B.q点溶液中溶质的第一步水解平衡常数的数量级为 |
| C.随着NaOH溶液的加入,水的电离程度一直在增大 |
D.n点满足关系: |
您最近一年使用:0次
2 . 向10mLHCOOH-NH4Cl混合溶液(浓度均为0.1mol·L−1)中滴加0.1mol·L−1NaOH溶液,并监测溶液pH变化,实验数据如图。由该实验可得到的结论是
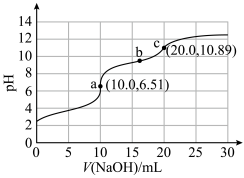
| A.HCOOH电离方程式为HCOOH=H++HCOO− |
| B.由a点数据可推出电离能力:HCOOH>NH3·H2O |
| C.b点溶液中的OH−主要来自HCOO−水解 |
| D.0.05mol·L−1氨水的pH<10.89 |
您最近一年使用:0次
2024-04-13更新
|
479次组卷
|
3卷引用:湖南省衡阳县第四中学2023-2024学年高三下学期4月月考化学试题
名校
3 . 电位滴定是利用溶液电位突变指示终点的滴定法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。常温下,用 盐酸标准溶液测定xmL某纯碱样品溶液中
盐酸标准溶液测定xmL某纯碱样品溶液中 的含量(其他杂质不参与反应),电位滴定曲线如图所示。下列说法错误的是
的含量(其他杂质不参与反应),电位滴定曲线如图所示。下列说法错误的是

 盐酸标准溶液测定xmL某纯碱样品溶液中
盐酸标准溶液测定xmL某纯碱样品溶液中 的含量(其他杂质不参与反应),电位滴定曲线如图所示。下列说法错误的是
的含量(其他杂质不参与反应),电位滴定曲线如图所示。下列说法错误的是
A.水的电离程度: |
B.a点溶液中: ,c点溶液中滴入2滴甲基橙溶液一定变黄色 ,c点溶液中滴入2滴甲基橙溶液一定变黄色 |
C.xmL该纯碱样品溶液中含有 的质量为0.084cg 的质量为0.084cg |
D.b到c过程中存在 |
您最近一年使用:0次
名校
解题方法
4 . 电位滴定法是靠电极电位的突跃来指示滴定终点。在滴定过程中,计算机对数据自动采集、处理,并利用滴定反应化学计量点前后电位突变的特性,自动寻找滴定终点。室温时,用 的NaOH标准溶液滴定同浓度的
的NaOH标准溶液滴定同浓度的 溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。已知
溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。已知 。下列说法错误的是
。下列说法错误的是

 的NaOH标准溶液滴定同浓度的
的NaOH标准溶液滴定同浓度的 溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。已知
溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。已知 。下列说法错误的是
。下列说法错误的是
A.a点溶液中 |
B.b点溶液中 |
C.常温时,c点溶液中 |
D.b、d点水的电离程度: |
您最近一年使用:0次
2023-03-08更新
|
500次组卷
|
5卷引用:湖南省邵阳市2023届高三下学期第二次联考(二模)化学试题
湖南省邵阳市2023届高三下学期第二次联考(二模)化学试题湖南省邵阳市邵东市2022-2023学年高三下学期3月月考化学试题山东省曹县第一中学2022-2023学年高三下学期2月月考化学试题(已下线)山东省青岛市2023届高三下学期一模化学试题变式题(不定项选择题)(已下线)专题8 新概念应用
名校
解题方法
5 . I.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂(指示剂加在待测液中)。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ ,直到_______ ,停止滴定。
(2)下列操作中可能使所测NaOH溶液的浓度偏高的是_______(填字母)。
(3)用0.1000mol/LNaOH溶液分别滴定0.1000mol/L的盐酸和醋酸溶液各25.00mL。滴定过程中溶液pH随滴入的NaOH溶液体积变化的两条滴定曲线如图所示:

滴定醋酸的曲线是_______ (填“I”或“II”),V1_______ V2。(填“>”“<”或“=”)
II.氧化还原滴定实验同中和滴定类似。人体缺乏维生素C(C6H8O6)易得坏血病。维生素C易被空气氧化。在新鲜的水果、蔬菜、乳制品中都富含维生素C,新鲜橙汁中维生素C的含量在500mg•L-1左右。某课外活动小组测定了某品牌的软包装橙子中维生素C的含量。下面是测定实验分析报告
i.测定目的:测定××牌软包装橙汁维生素的含量,是否为纯天然
ii.测定原理:C6H8O6+I2=C6H6O6+2H++2I-
iii.实验过程:
①移取20.00mL饮料样品于250mL锥形瓶中,加入50mL蒸馏水,2mL指示剂
②在滴定管中装入7.50×10-3mol·L-1标准碘溶液,滴定至终点,读取并记录相关数据
③重复测定3次,数据记录如下表
(4)回答下列问题:
①实验选择选用_______ 作指示剂
②计算该饮料样品中维生素C含量为_______ mg•L-1.该饮料_______ (填“是”或“不是”)鲜榨橙汁。(已知维生素C的摩尔质量为176g/mol)
③滴定时不能剧烈摇动锥形瓶原因是_______ 。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测NaOH溶液的浓度偏高的是_______(填字母)。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸溶液体积时,开始仰视读数,滴定结束时俯视读数 |

滴定醋酸的曲线是
II.氧化还原滴定实验同中和滴定类似。人体缺乏维生素C(C6H8O6)易得坏血病。维生素C易被空气氧化。在新鲜的水果、蔬菜、乳制品中都富含维生素C,新鲜橙汁中维生素C的含量在500mg•L-1左右。某课外活动小组测定了某品牌的软包装橙子中维生素C的含量。下面是测定实验分析报告
i.测定目的:测定××牌软包装橙汁维生素的含量,是否为纯天然
ii.测定原理:C6H8O6+I2=C6H6O6+2H++2I-
iii.实验过程:
①移取20.00mL饮料样品于250mL锥形瓶中,加入50mL蒸馏水,2mL指示剂
②在滴定管中装入7.50×10-3mol·L-1标准碘溶液,滴定至终点,读取并记录相关数据
③重复测定3次,数据记录如下表
| 第一次 | 第二次 | 第三次 | |
| 滴定前读数/mL | 0.00 | 0.44 | 1.33 |
| 滴定后读数/mL | 15.01 | 15.44 | 15.32 |
①实验选择选用
②计算该饮料样品中维生素C含量为
③滴定时不能剧烈摇动锥形瓶原因是
您最近一年使用:0次
2023-02-02更新
|
155次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三下学期第三次模拟检测化学试题
6 . 25℃时,用 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是

 气体调节
气体调节 氨水的
氨水的 ,溶液中微粒浓度的对数值(
,溶液中微粒浓度的对数值( )、反应物的物质的量之比[
)、反应物的物质的量之比[ ]与
]与 的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
A.25℃时, 的电离平衡常数为 的电离平衡常数为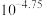 |
B. 所示溶液中: 所示溶液中: |
C. 所示溶液中: 所示溶液中: |
D. 所示溶液中: 所示溶液中: |
您最近一年使用:0次
名校
解题方法
7 . 用0.10 的NaOH溶液分别滴定体积均为20.00mL、浓度均为0.050
的NaOH溶液分别滴定体积均为20.00mL、浓度均为0.050 的盐酸、磷酸及谷氨酸
的盐酸、磷酸及谷氨酸 ,滴定曲线如图所示。下列说法正确的是
,滴定曲线如图所示。下列说法正确的是

 的NaOH溶液分别滴定体积均为20.00mL、浓度均为0.050
的NaOH溶液分别滴定体积均为20.00mL、浓度均为0.050 的盐酸、磷酸及谷氨酸
的盐酸、磷酸及谷氨酸 ,滴定曲线如图所示。下列说法正确的是
,滴定曲线如图所示。下列说法正确的是
A.用酚酞作指示剂滴定磷酸到终点时,溶液中的溶质为 |
B.滴定盐酸时, 时, 时, |
C. 的第一电离平衡常数 的第一电离平衡常数 的数量级不同 的数量级不同 |
D. 溶液中: 溶液中: |
您最近一年使用:0次
名校
解题方法
8 . 室温下,向20.00mL0.1000mol/L的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度、酸度AG[AG= 随加入稀硫酸体积的变化如图所示。下列说法正确的是
随加入稀硫酸体积的变化如图所示。下列说法正确的是

 随加入稀硫酸体积的变化如图所示。下列说法正确的是
随加入稀硫酸体积的变化如图所示。下列说法正确的是
| A.硫酸的浓度为0.1000mol/L |
| B.b点对应的溶液中:c(M+)+2c(H+)=2c(OH-)+c(MOH) |
C.当AG=0时,溶液中存在:c( )>c(M+)>c(H+)=c(OH-) )>c(M+)>c(H+)=c(OH-) |
| D.b、c、d三点对应的溶液中,水的电离程度的大小关系是b>c>d |
您最近一年使用:0次
2022-05-03更新
|
496次组卷
|
4卷引用:湖南省湘潭市第一中学2022届2021-2022学年高三下学期月考化学试题
湖南省湘潭市第一中学2022届2021-2022学年高三下学期月考化学试题广东省韶关市2022届高三综合测试(二模)化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)选择题11-16
名校
9 . 常温下,用0.10mol/L的NaOH溶液滴定0.10mol/L的HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列叙述错误的是


| A.Ka(HA)的数量级约为10-5 |
B.N点,c(Na+)-c(A-)=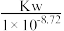 |
| C.P→Q过程中,水的电离程度逐渐减小 |
| D.当滴定至溶液呈中性时,c(A-)>c(HA) |
您最近一年使用:0次
名校
解题方法
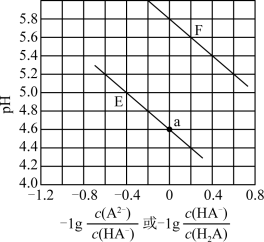
10 . 常温下向二元弱酸 溶液中滴加
溶液中滴加 溶液,所得溶液的pH与离子浓度的变化关系如图所示。下列说法错误的是
溶液,所得溶液的pH与离子浓度的变化关系如图所示。下列说法错误的是
 溶液中滴加
溶液中滴加 溶液,所得溶液的pH与离子浓度的变化关系如图所示。下列说法错误的是
溶液,所得溶液的pH与离子浓度的变化关系如图所示。下列说法错误的是
A.曲线F表示溶液pH与 的变化关系 的变化关系 |
B.图中a点对应溶液中: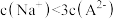 |
C. |
| D.pH从4.6到5.8的过程中,水电离出的氢离子浓度逐渐增大 |
您最近一年使用:0次
2022-04-24更新
|
252次组卷
|
2卷引用:湖南省长沙市第一中学2021-2022学年高三下学期月考(九)化学试题



