1 . 向5mL 0.10mol·L-1 H2A溶液滴加一定浓度的NaOH溶液,滴定过程中溶液pH和温度随 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是

 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是
| A.Z点为第二反应终点,可选用甲基橙作为指示剂 |
| B.从W至Z点,水的电离程度逐渐增大,Kw不变 |
C.当 =1.5时,c(H2A) > =1.5时,c(H2A) >  c(A2−) − c(A2−) −  c(HA−) c(HA−) |
| D.25 ℃时,H2A的电离常数Ka1=10-2.3,Ka2=10-9.7 |
您最近一年使用:0次
名校
2 .  时,向0.1mol/L甘氨酸水溶液中通入HCl或加入NaOH固体,溶液pH变化曲线如图所示。已知:
时,向0.1mol/L甘氨酸水溶液中通入HCl或加入NaOH固体,溶液pH变化曲线如图所示。已知:

①在溶液中甘氨酸以 三种形式存在,且有如下平衡:
三种形式存在,且有如下平衡:

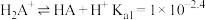

②在某pH下,溶液中甘氨酸主要以HA存在,且甘氨酸整体所带的正负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。下列说法正确的是
 时,向0.1mol/L甘氨酸水溶液中通入HCl或加入NaOH固体,溶液pH变化曲线如图所示。已知:
时,向0.1mol/L甘氨酸水溶液中通入HCl或加入NaOH固体,溶液pH变化曲线如图所示。已知:
①在溶液中甘氨酸以
 三种形式存在,且有如下平衡:
三种形式存在,且有如下平衡:
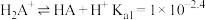

②在某pH下,溶液中甘氨酸主要以HA存在,且甘氨酸整体所带的正负电荷数目相等,此时的pH称为该氨基酸的等电点(pI)。下列说法正确的是
A.甘氨酸的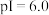 |
B.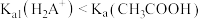 |
C.a点溶液中, |
| D.b点NaOH当量=0.5 |
您最近一年使用:0次
2023-07-12更新
|
928次组卷
|
3卷引用:湖北省华中师范大学第一附属中学2023届高三下学期考前核心素养卷化学试题
湖北省华中师范大学第一附属中学2023届高三下学期考前核心素养卷化学试题湖南省长沙市湖南师范大学附属中学2024届高三下学期模拟试卷(一) 化学试题(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
3 . 室温下,向20.00 mL0.1 mol·L-1的H3AsO4溶液中滴加等浓度的NaOH溶液。混合溶液中-lg X[表示 、
、 、
、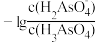 ]随溶液pH的变化如图所示。
]随溶液pH的变化如图所示。

下列说法正确的是
 、
、 、
、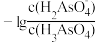 ]随溶液pH的变化如图所示。
]随溶液pH的变化如图所示。
下列说法正确的是
A.曲线a表示 与溶液pH的关系 与溶液pH的关系 |
B.当消耗20.00 mL的NaOH溶液时,c(Na+ )> 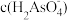 > > > >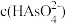 |
C.pH=7.00时,c (Na+) = 3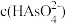 +3 +3 |
D.溶液中存在关系: > >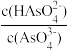 |
您最近一年使用:0次
4 . 常温下,用0.2 mol·L-1NaOH溶液滴定20.00mL一定浓度的一元酸HR溶液时,混合溶液的pH变化情况如图所示,图中a点为滴定终点。下列有关说法正确的是


| A.图中x=7 |
| B.常温下,HR的电离常数Ka=5.0×10-5 |
| C.a点溶液中: c(R-)+ c(OH-)- c(H+)=0.1 mol·L-1 |
| D.b点溶液中: c(Na+)> c(R-)> c(OH-)> c(H+) |
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象及结论均正确的是
选项 | 操作 | 现象. | 结论 |
A | 向红热的铁粉与水蒸气反应后的固体中加入稀硫酸酸化,再滴入几滴KSCN溶液 | 溶液未变红 | 说明铁粉与水蒸气未反应 |
B | 向0.01 mol/L FeCl3溶液中,加入少量FeCl3固体 | 溶液颜色加深 | Fe3+水解程度增大 |
C | 相同温度下,用pH计分别测定0.010mol/LHF溶液和0.010 mol/L CH3COOH溶液的pH | HF溶液pH更小 | 电离常数:HF<CH3COOH |
D | 将在酒精灯上灼烧后的铜丝迅速插入乙醇中 | 铜丝表面由黑色变为红色 | 乙醇具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的MOH溶液,其导电率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。

下列说法正确的是

下列说法正确的是
| A.a→d过程中,水的电离程度逐渐增大 |
| B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小 |
| C.常温下,Kb (MOH) =Ka(HA)≈10 -4.6 |
| D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- ) |
您最近一年使用:0次
2023-06-13更新
|
261次组卷
|
5卷引用:河南省南阳市第一中学校2023届高三下学期第三次模拟考试理综化学试题
河南省南阳市第一中学校2023届高三下学期第三次模拟考试理综化学试题(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第30讲水的电离和溶液的酸碱性陕西省汉中中学2023-2024学年高三上学期11月质量检测化学试题(已下线)T13-水溶液中的离子平衡
7 . 常温下,二元酸H2A的Ka2(H2A)= 1.0 ×10-2。 在某体系中,H+与A2-离子不能穿过隔膜,HA-可自由穿过该膜(如图所示)。溶液中c 总(H2A)=c(HA-)+c(A2-),当达到平衡时,下列叙述正确的是
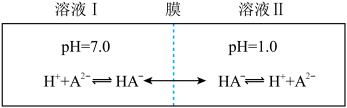

| A.溶液I中: c(H+)-c(OH-)=c 总(H2A) |
| B.溶液II中: c (H2A) >c(H+)>c(HA-) >c(OH-) |
| C.溶液I和II中的c总(H2A)不相等 |
| D.溶液I和II中的c(A2-)之比为105 |
您最近一年使用:0次
解题方法
8 . 25℃时,用同一较高浓度的NaOH溶液分别滴定酸HA和CuSO4溶液,pM[p 表示负对数, M表示 、c(Cu2+)]与溶液pH的变化关系如图。已知; CuA2 易溶于水,一般认为反应的平衡常数为K> 105时反应进行完全。下列说法错误的是
、c(Cu2+)]与溶液pH的变化关系如图。已知; CuA2 易溶于水,一般认为反应的平衡常数为K> 105时反应进行完全。下列说法错误的是

 、c(Cu2+)]与溶液pH的变化关系如图。已知; CuA2 易溶于水,一般认为反应的平衡常数为K> 105时反应进行完全。下列说法错误的是
、c(Cu2+)]与溶液pH的变化关系如图。已知; CuA2 易溶于水,一般认为反应的平衡常数为K> 105时反应进行完全。下列说法错误的是
| A.HA为一元弱酸,25℃时 Ka=10-7.4 |
| B.①表示滴定CuSO4溶液时pM与溶液pH的关系 |
| C.滴定HA溶液至x点时,溶液中c(HA)> c(A-)> c(Na+) |
| D.滴定CuSO4溶液至x点时,若改为滴加HA溶液,沉淀会逐渐完全溶解 |
您最近一年使用:0次
9 . 人体血液存在H2CO3/ ,
, /
/ 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示 或
或 ]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是

 ,
, /
/ 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx [x表示 或
或 ]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
]与pH的关系如图所示。已知碳酸pKa1=6.4、磷酸pKa2=7.2 (pKa=-lgKa)。则下列说法错误的是
A.曲线I表示lg 与pH的变化关系 与pH的变化关系 |
| B.a→b的过程中,水的电离程度逐渐增大 |
C.当pH增大时, 逐渐减小 逐渐减小 |
D.当c(H2CO3) =c( ) 时,c( ) 时,c( ) <c( ) <c( ) ) |
您最近一年使用:0次
名校
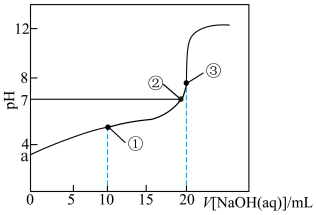
10 . 已知:叠氮酸( )是一元弱酸,其电离常数
)是一元弱酸,其电离常数 (298K)。298K时,在20mL浓度为
(298K)。298K时,在20mL浓度为 溶液中滴加
溶液中滴加 的NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示(已知:
的NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示(已知: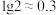 )。下列说法错误的是
)。下列说法错误的是
 )是一元弱酸,其电离常数
)是一元弱酸,其电离常数 (298K)。298K时,在20mL浓度为
(298K)。298K时,在20mL浓度为 溶液中滴加
溶液中滴加 的NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示(已知:
的NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示(已知: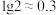 )。下列说法错误的是
)。下列说法错误的是
| A.298K时,水的电离程度①<②<③ |
| B.a点pH约为2.7 |
C.①点溶液中: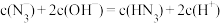 |
D.②点溶液中: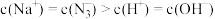 |
您最近一年使用:0次



