名校
1 . 25℃时,滴有两滴酚酞试液的Na2SO3溶液中存在平衡: +H2O
+H2O
 +OH-,溶液呈红色,下列说法不正确的是
+OH-,溶液呈红色,下列说法不正确的是
 +H2O
+H2O
 +OH-,溶液呈红色,下列说法不正确的是
+OH-,溶液呈红色,下列说法不正确的是| A.升高温度,红色变深,平衡常数增大 |
| B.通入SO2,溶液pH减小 |
| C.加入 BaCl2固体,红色变浅,证明溶液中存在上述平衡 |
D.稀释溶液,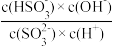 不变 不变 |
您最近一年使用:0次
名校
2 .  溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓 ,黄色加深(b)。
,黄色加深(b)。
已知: (黄色);浓度较小时
(黄色);浓度较小时 (用
(用 表示)几乎无色
表示)几乎无色
取溶液进行如下实验,对现象的分析不正确 的是
 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓
溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓 ,黄色加深(b)。
,黄色加深(b)。已知:
 (黄色);浓度较小时
(黄色);浓度较小时 (用
(用 表示)几乎无色
表示)几乎无色取溶液进行如下实验,对现象的分析
A.测溶液a的 ,证明 ,证明 发生了水解 发生了水解 |
B.将溶液a滴入沸水中并加热,有丁达尔效应,说明加热能促进 水解 水解 |
C.加入浓 , , 与 与 对溶液颜色变化、 对溶液颜色变化、 浓度大小的影响是一致的 浓度大小的影响是一致的 |
D.向b中加入 后,黄色褪至几乎无色,说明 后,黄色褪至几乎无色,说明 能抑制 能抑制 水解 水解 |
您最近一年使用:0次
2023-12-11更新
|
352次组卷
|
11卷引用:必刷卷02-2022年高考化学考前信息必刷卷(河北专用)
(已下线)必刷卷02-2022年高考化学考前信息必刷卷(河北专用)(已下线)必刷卷04-2022年高考化学考前信息必刷卷(河北专用)北京市朝阳区2022届高三一模化学试题北京市第一七一中学2022届高三下学期三模化学试题湖南省娄底市第五中学2021-2022学年高三下学期第三次模拟考试化学试题北京市一0一中学2022-2023学年高二下学期期中考试化学试题北京市育英学校2023-2024学年高三上学期(12月)统测五化学学科试题(已下线)北京市第四中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业06 盐类的水解-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)专题05 盐类的水解-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)北京市第四中学2023-2024学年高三下学期一模模拟化学试题
2023·河北·模拟预测
3 . 氯化铁是一种很重要的铁盐,主要用于污水处理、印染工业、电子工业、建筑工业等。氯化铁有吸水性,遇水极易水解。某化学兴趣小组设计实验制备氯化铁并探究其性质。回答下列问题:
I.氯化铁的制备:
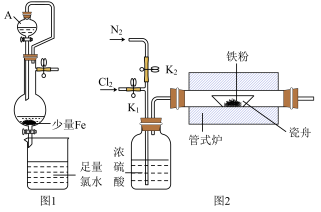
(1)图1为湿法制备的装置。仪器A的名称为___________ ,烧杯中发生反应的离子方程式为___________ 。
(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是___________ ;氮气和氯气都必须经过浓硫酸,原因是___________ 。
Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁[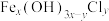 ]。已知聚合氯化铁极易溶于水,写出氯化铁水解反应的总离子方程式
]。已知聚合氯化铁极易溶于水,写出氯化铁水解反应的总离子方程式_____ 。
(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化),获得如下数据:
①根据实验数据,结合所学化学知识,下列说法正确的是___________ (填标号)。
A.氯化铁的水解程度与温度、铁离子的浓度均有关系
B.实验1和实验2说明氯化铁浓度越大,水解程度越大
C.实验2和实验3说明 的水解是吸热反应
的水解是吸热反应
D.实验4和实验5中加入固体的质量不等,无法对比参照
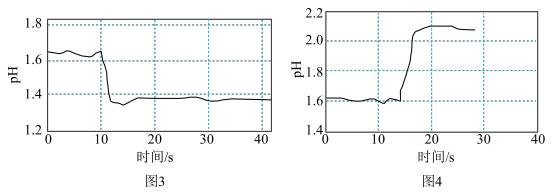
②查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。
i.根据实验现象,提出假设:a.氯离子对铁离子的水解活性有促进作用;b.___________ 。
ii..设计其他简单实验证明假设a:___________ (写出实验操作、现象和结论)。
I.氯化铁的制备:

(1)图1为湿法制备的装置。仪器A的名称为
(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是
Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁[
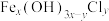 ]。已知聚合氯化铁极易溶于水,写出氯化铁水解反应的总离子方程式
]。已知聚合氯化铁极易溶于水,写出氯化铁水解反应的总离子方程式(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化),获得如下数据:
| 实验 | 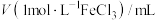 | 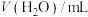 | 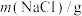 | 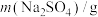 | 温度/℃ | pH |
| 1 | 10 | 0 | 0 | 0 | 25 | 0.74 |
| 2 | 10 | 90 | 0 | 0 | 25 | 1.62 |
| 3 | 10 | 90 | 0 | 0 | 35 | 1.47 |
| 4 | 10 | 90 | 1.17 | 0 | 25 | x |
| 5 | 10 | 90 | 0 | 1.42 | 25 | y |
A.氯化铁的水解程度与温度、铁离子的浓度均有关系
B.实验1和实验2说明氯化铁浓度越大,水解程度越大
C.实验2和实验3说明
 的水解是吸热反应
的水解是吸热反应D.实验4和实验5中加入固体的质量不等,无法对比参照
②查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。

i.根据实验现象,提出假设:a.氯离子对铁离子的水解活性有促进作用;b.
ii..设计其他简单实验证明假设a:
您最近一年使用:0次
名校
4 . 下列实验方案能达到实验目的的是
| 选项 | A | B | C | D |
| 目的 | 制备并收集乙酸乙酯 | 证明温度对平衡的影响 | 证明AgI的溶解度小于AgCl | 蒸干氯化锰溶液制 |
| 实验方案 |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-10更新
|
292次组卷
|
4卷引用:河北省五校联盟(保定市第一中学等)2021-2022学年高三下学期3月模拟考试化学试题
河北省五校联盟(保定市第一中学等)2021-2022学年高三下学期3月模拟考试化学试题河北省唐山市开滦一中2022-2023学年高二下学期期末考试化学试题(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省永州市第四中学2022届高三下学期期中考试化学试题
5 . 绿矾常用于制造补血制剂、净水剂等。以废铁屑(主要含 ,含少量
,含少量 、油脂等杂质)为原料制备绿矾晶体(
、油脂等杂质)为原料制备绿矾晶体( )的流程如图,并设计实验探究绿矾的性质。
)的流程如图,并设计实验探究绿矾的性质。
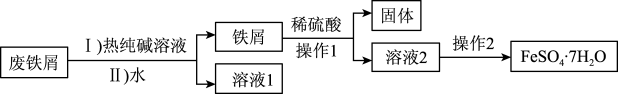
回答下列问题:
(1)用热纯碱溶液洗涤废铁屑的目的是___________ 。“操作1”需要的玻璃仪器有___________ 。
(2)检验“溶液2”中是否含 的试剂是___________(填标号)。
的试剂是___________(填标号)。
(3)“操作2”包括蒸发浓缩、___________ 、过滤、洗涤、干燥。选用75%酒精而不选用蒸馏水洗涤绿矾的优点是___________ 。
(4)实验室配制绿矾溶液时常加入少量铁粉,其作用是___________ (用离子方程式表示)。
(5)大多数文献认为“ 分解生成
分解生成 、
、 、
、 ”。某实验小组提出质疑,认为可能还有
”。某实验小组提出质疑,认为可能还有 生成。他们设计实验分离
生成。他们设计实验分离 、
、 并检验
并检验 ,实验装置如图所示(加热仪器省略)。
,实验装置如图所示(加热仪器省略)。

已知部分信息如下:
Ⅰ.几种物质的熔、沸点如表所示:
Ⅱ.几种盐浴温度如表所示:
①低温浴槽A宜选择盐浴___________ (填字母),仪器C收集的物质是___________ (填化学式)。
②若___________ (填实验操作和现象),则证明 分解有
分解有 生成。
生成。
 ,含少量
,含少量 、油脂等杂质)为原料制备绿矾晶体(
、油脂等杂质)为原料制备绿矾晶体( )的流程如图,并设计实验探究绿矾的性质。
)的流程如图,并设计实验探究绿矾的性质。
回答下列问题:
(1)用热纯碱溶液洗涤废铁屑的目的是
(2)检验“溶液2”中是否含
 的试剂是___________(填标号)。
的试剂是___________(填标号)。A. 溶液 溶液 | B. 溶液 溶液 |
C.酸性 溶液 溶液 | D.氯水和 溶液 溶液 |
(4)实验室配制绿矾溶液时常加入少量铁粉,其作用是
(5)大多数文献认为“
 分解生成
分解生成 、
、 、
、 ”。某实验小组提出质疑,认为可能还有
”。某实验小组提出质疑,认为可能还有 生成。他们设计实验分离
生成。他们设计实验分离 、
、 并检验
并检验 ,实验装置如图所示(加热仪器省略)。
,实验装置如图所示(加热仪器省略)。
已知部分信息如下:
Ⅰ.几种物质的熔、沸点如表所示:
| 物质 |  |  |  |
| 熔点/℃ | 16.8 | -72.7 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |
| 盐浴 | 浴温 | 盐类及用量 | 碎冰用量 |
| a | 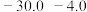 ℃ ℃ | 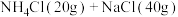 |  |
| b | 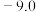 ℃ ℃ | 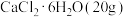 |  |
| c | 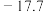 ℃ ℃ | 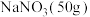 |  |
②若
 分解有
分解有 生成。
生成。
您最近一年使用:0次
2022-01-28更新
|
218次组卷
|
3卷引用:河北省邯郸市2021-2022学年高三上学期十校期末联考化学试题
名校
6 . 下述实验能达到预期目的的是
| 实验内容 | 实验目的 | |
| A | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 证明SO2具有漂白性 |
| B | 向滴有酚酞的Na2CO3溶液中加入BaCl2固体,红色褪去 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 证明氧化性:Cu2+>Fe3+ |
| D | 向Na2SiO3溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 证明非金属性:Cl>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 下列实验能达到预期目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 室温下,用 试纸分别测定浓度均为 试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| B | 向 悬浊液中滴入 悬浊液中滴入 溶液,悬浊液变黄 溶液,悬浊液变黄 | 证明相同温度下: |
| C | 常温下,测得饱和溶液的 : : | 证明常温下的水解程度: |
| D | 等体积、 均为2的 均为2的 和 和 两种酸分别与足量 两种酸分别与足量 反应, 反应, 放出的 放出的 多 多 | 证明 是强酸 是强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作能达到实验目的的是
| 目的 | 操作 | |
| A | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点滴于试纸的中部,与标准比色卡对比 |
| B | 验证Ksp(AgCl)>Ksp( AgI) | 取2 mL0. 1mol·L-1AgNO3溶液,先后滴加3滴0.1mol·L-1NaCl溶液和5滴0.1mol·L-1KI溶液,先生成白色沉淀,后又产生黄色沉淀 |
| C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
| D | 检验Fe(NO3)2晶体是否已 氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-24更新
|
624次组卷
|
8卷引用:河北省邯郸市永年区第二中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
9 . 下列实验操作能达到实验目的的是
| 目的 | 操作 | |
| A | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点滴于试纸的中部,与标准比色卡对比 |
| B | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
| C | 验证Ksp(AgCl)>Ksp(AgI) | 取2mL0.1mol·L-1AgNO3溶液,先后滴加3滴0.1mol·L-1NaCl溶液和5滴0.1mol·L-1KI溶液,先生成白色沉淀,后又产生黄色沉淀 |
| D | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-07-31更新
|
140次组卷
|
2卷引用:河北省沧州市第一中学2020-2021学年高二下学期第一次月考化学试题
名校
10 . 已知:[FeCl4(H2O)2]-呈黄色,由下列实验所得结论不正确的是
注:加热为微热,忽略溶液体积变化。
| ① | ② | ③ | ④ |
 0.1mol/L Fe2(SO4)3溶液 |  酸化的0.1mol/L Fe2(SO4)3溶液 |  酸化的0.1mol/L Fe2(SO4)3溶液 |  0.1mol/L FeCl3溶液 |
| 加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色加深 | 加热前溶液为黄色,加热后溶液颜色变深 |
注:加热为微热,忽略溶液体积变化。
| A.实验①中,Fe2(SO4)3溶液显浅黄色的原因是Fe3+水解产生了少量Fe(OH)3 |
| B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响 |
C.实验③中,存在平衡:Fe3+ +4Cl- +2H2O [FeCl4(H2O)2]- [FeCl4(H2O)2]- |
| D.实验④中,可证明升高温度,Fe3+水解平衡一定正向发生移动 |
您最近一年使用:0次
2020-03-03更新
|
358次组卷
|
6卷引用:河北省实验中学2021届高三上学期第一次月考化学试题



