解题方法
1 . 下列反应过程对应的离子方程式书写正确的是
A.向 溶液中通入过量 溶液中通入过量 : :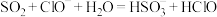 |
B.向氯化铝溶液中加入小苏打溶液: |
C.向 溶液中加入少量 溶液中加入少量 溶液: 溶液: |
D.向稀硝酸中加入 溶液: 溶液: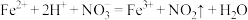 |
您最近一年使用:0次
2 . 下列化学用语或图示表达正确的是
A. 的名称为:1-丁醇 的名称为:1-丁醇 |
B.邻羟基苯甲醛分子内氢键示意图: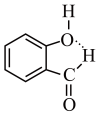 |
C. 水解的离子方程式: 水解的离子方程式: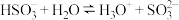 |
D.HCl分子中 键的形成: 键的形成: |
您最近一年使用:0次
名校
解题方法
3 . 下列解释事实的离子方程式正确的是
A.泡沫灭火器的反应原理: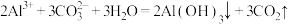 |
B. 化学性质非常稳定,在工业上有着广泛用途,可用 化学性质非常稳定,在工业上有着广泛用途,可用 制备 制备 : : |
C. 溶液显酸性的原因: Mg2++2H2O 溶液显酸性的原因: Mg2++2H2O Mg (OH) 2+2H+ Mg (OH) 2+2H+ |
D. 溶液的水解方程式: 溶液的水解方程式: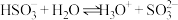 |
您最近一年使用:0次
2022-11-22更新
|
593次组卷
|
5卷引用:贵州省贵州铜仁伟才学校2022-2023学年高二上学期12月月考化学试题
解题方法
4 . 食醋是市民餐桌上不可或缺的调味品,其中的酸性物质主要是乙酸。查阅教材附录可以了解更多弱酸在25℃时的电离常数如下表:。
回答下列问题:
(1)25℃时,pH=3的醋酸溶液中,
_______  ,将其加水稀释,
,将其加水稀释,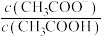 的值将
的值将_______ (填“增大”、“减小”或“不变”)。
(2)家用84消毒液的有效成分是NaClO。用离子方程式表示NaClO溶液呈碱性的原因_______ ,其溶液中各离子浓度由大到小的顺序为_______ 。
(3)25℃时,浓度均为0.1 的①
的① ;②NaClO;③
;②NaClO;③ 三种溶液的pH由大到小的顺序是
三种溶液的pH由大到小的顺序是_______ (填序号)。
| 弱酸 |  | HClO |  |
 /25℃ /25℃ |  | 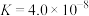 | 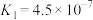  |
(1)25℃时,pH=3的醋酸溶液中,

 ,将其加水稀释,
,将其加水稀释,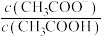 的值将
的值将(2)家用84消毒液的有效成分是NaClO。用离子方程式表示NaClO溶液呈碱性的原因
(3)25℃时,浓度均为0.1
 的①
的① ;②NaClO;③
;②NaClO;③ 三种溶液的pH由大到小的顺序是
三种溶液的pH由大到小的顺序是
您最近一年使用:0次
2023-02-14更新
|
208次组卷
|
2卷引用:贵州省贵阳市普通中学2022-2023学年高二上学期期末监测化学试题
名校
5 . 下列离子方程式中,属于水解反应的是
A. |
B. |
C. |
D.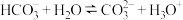 |
您最近一年使用:0次
2022-12-18更新
|
259次组卷
|
4卷引用:贵州省黔东南州凯里市第一中学2022-2023学年高二上学期12月月考化学试题
解题方法
6 . 硫及其化合物在生产、生活中具有广泛的应用,根据所学知识,回答下列问题:
(1)Al2(SO4)3溶液显___________ (填“酸”、“碱”或“中”)性,判断的理由是___________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为___________ (填化学式)。
(2)(NH4)2SO4溶液中,各离子浓度由大到小的关系为___________ 。
(3)室温下,在某NaHSO3、Na2SO3混合溶液中, 、
、 物质的量分数随
物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=___________ 。

(4)室温下,某浓度的(NH4)2SO3溶液中:
①(NH4)2SO3为___________ (填“强”或“弱”)电解质。
②
___________ (填“>”、“<”或“=”)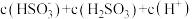 。
。
③往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为___________ ,此时所得溶液的pH___________ (填“变大”、“变小”或“不变”)。
(1)Al2(SO4)3溶液显
(2)(NH4)2SO4溶液中,各离子浓度由大到小的关系为
(3)室温下,在某NaHSO3、Na2SO3混合溶液中,
 、
、 物质的量分数随
物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=
(4)室温下,某浓度的(NH4)2SO3溶液中:
①(NH4)2SO3为
②

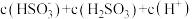 。
。③往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为
您最近一年使用:0次
2022-01-24更新
|
257次组卷
|
4卷引用:贵州省遵义市2021-2022学年高二上学期期末考试化学试题
解题方法
7 . 电解质在工农业生产和社会生活中的应用越来越广泛。回答下列问题:
(1)常温下,0.1 mol∙L−1的CH3COOH溶液与pH=13的NaOH溶液等体积混合后,溶液中的pH_____ 7(填“>”、“<”或“=”)。
(2)明矾常用作净水剂,请用离子方程式解释其净水原理_____ 。
(3)硫氢化钠(NaHS)常用作有机合成的中间体,其水溶液显碱性。则NaHS溶液中Na+、H+、HS-、OH-离子浓度由大到小的顺序为_____ 。
(4)碳酸钠的水溶液中存在着多种离子和分子,以下关系式正确的是_____ (填字母序号)。
a.c(Na+)+c(H+)=c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
b.c(Na+)=2c(CO )+2c(HCO
)+2c(HCO )+2c(H2CO3)
)+2c(H2CO3)
c.c(OH-)=c(H+)+c(HCO )+c(H2CO3)
)+c(H2CO3)
(5)常温下,0.1 mol∙L−1的H2SO4溶液与pH=13的KOH溶液等体积混合后,混合溶液pH=_____ 。(已知lg2=0.3;lg5=0.7)
(1)常温下,0.1 mol∙L−1的CH3COOH溶液与pH=13的NaOH溶液等体积混合后,溶液中的pH
(2)明矾常用作净水剂,请用离子方程式解释其净水原理
(3)硫氢化钠(NaHS)常用作有机合成的中间体,其水溶液显碱性。则NaHS溶液中Na+、H+、HS-、OH-离子浓度由大到小的顺序为
(4)碳酸钠的水溶液中存在着多种离子和分子,以下关系式正确的是
a.c(Na+)+c(H+)=c(CO
 )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)b.c(Na+)=2c(CO
 )+2c(HCO
)+2c(HCO )+2c(H2CO3)
)+2c(H2CO3)c.c(OH-)=c(H+)+c(HCO
 )+c(H2CO3)
)+c(H2CO3)(5)常温下,0.1 mol∙L−1的H2SO4溶液与pH=13的KOH溶液等体积混合后,混合溶液pH=
您最近一年使用:0次
解题方法
8 . 宏观辨识和微观探析是化学学科的核心素养之一。下列指定反应的离子方程式书写正确的是
A.向 溶液中加入过量稀盐酸: 溶液中加入过量稀盐酸: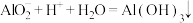 |
B.明矾净水: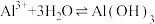 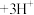 |
C.用氨水吸收足量的 气体: 气体: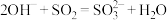 |
D.稀硝酸溶解FeO固体: |
您最近一年使用:0次
2022-09-26更新
|
163次组卷
|
2卷引用:贵州省2022-2023学年高三上学期联考化学试题
解题方法
9 . 下列离子方程式书写错误的是
A.泡沫灭火器工作原理:2Al3++3CO +3H2O=2Al(OH)3↓+3CO2↑ +3H2O=2Al(OH)3↓+3CO2↑ |
B.NH4Cl溶液可以除去铁锈的原因:NH +H2O +H2O NH3·H2O+H+ NH3·H2O+H+ |
| C.工业上用FeS除去废水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq) |
D.草酸使酸性高锰酸钾溶液褪色:5H2C2O4+2MnO +6H+=l0CO2↑+2Mn2++8H2O +6H+=l0CO2↑+2Mn2++8H2O |
您最近一年使用:0次
10 . 下列用于解释事实的方程式书写错误的是
A.碱性锌锰电池的负极反应式: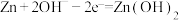 |
B.明矾可以用作净水剂: |
C. 溶液与ZnS反应生成CuS: 溶液与ZnS反应生成CuS: |
D.家庭中用白醋洗涤水垢中的 : : |
您最近一年使用:0次



