解题方法
1 . 物质的制备是化学学科的基本研究方向。
(1)已知用金属钠制取氧化钠,可有多种方法:
①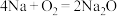 ;②
;② ;③
;③
在上述三种方法中最好的是_______ (填序号),若生成相同物质的量的 ,转移电子的物质的量之比是
,转移电子的物质的量之比是_______ 。
(2)某同学拟用100
 溶液吸收
溶液吸收 气体制备
气体制备 溶液,他设计了如下实验步骤:
溶液,他设计了如下实验步骤:
①取50 该
该 溶液吸收过量的
溶液吸收过量的 气体,至
气体,至 气体不再溶解;
气体不再溶解;
②小心加热溶液1~2min;
③在实验步骤②得到的溶液中加入另一半(50 )
) 溶液,使溶液充分混合。
溶液,使溶液充分混合。
制备过程中涉及到的化学反应用离子方程式分别表示为_______ 、_______ 。若没有实验步骤②,则产品中可能含有的杂质是_______ (填化学式)。
(3)已知 溶液呈碱性,
溶液呈碱性, 溶液呈弱酸性。用
溶液呈弱酸性。用 溶液和
溶液和 溶液发生复分解反应制备
溶液发生复分解反应制备 ,在烧杯中制备
,在烧杯中制备 沉淀时,为避免生成
沉淀时,为避免生成 沉淀,应选用的加料方式是
沉淀,应选用的加料方式是_______ (填字母)。
A.将 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中
B.将 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中
(4)过氧化钙( )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取 ,再经脱水制得
,再经脱水制得 ,
,
不溶于水 ,在0℃时稳定,加热至130℃时逐渐变为无水 ,已知
,已知 不稳定,受热易分解,其制备过程如下:
不稳定,受热易分解,其制备过程如下:

I.“沉淀”时反应温度不能过高的原因:①防止氨水挥发;②_______ ;
II.“沉淀”时发生的反应用化学方程式表示为:_______ 。
(1)已知用金属钠制取氧化钠,可有多种方法:
①
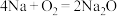 ;②
;② ;③
;③
在上述三种方法中最好的是
 ,转移电子的物质的量之比是
,转移电子的物质的量之比是(2)某同学拟用100

 溶液吸收
溶液吸收 气体制备
气体制备 溶液,他设计了如下实验步骤:
溶液,他设计了如下实验步骤:①取50
 该
该 溶液吸收过量的
溶液吸收过量的 气体,至
气体,至 气体不再溶解;
气体不再溶解;②小心加热溶液1~2min;
③在实验步骤②得到的溶液中加入另一半(50
 )
) 溶液,使溶液充分混合。
溶液,使溶液充分混合。制备过程中涉及到的化学反应用离子方程式分别表示为
(3)已知
 溶液呈碱性,
溶液呈碱性, 溶液呈弱酸性。用
溶液呈弱酸性。用 溶液和
溶液和 溶液发生复分解反应制备
溶液发生复分解反应制备 ,在烧杯中制备
,在烧杯中制备 沉淀时,为避免生成
沉淀时,为避免生成 沉淀,应选用的加料方式是
沉淀,应选用的加料方式是A.将
 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中B.将
 溶液缓慢加入到盛有
溶液缓慢加入到盛有 溶液的烧杯中
溶液的烧杯中(4)过氧化钙(
 )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取 ,再经脱水制得
,再经脱水制得 ,
,
 ,已知
,已知 不稳定,受热易分解,其制备过程如下:
不稳定,受热易分解,其制备过程如下:
I.“沉淀”时反应温度不能过高的原因:①防止氨水挥发;②
II.“沉淀”时发生的反应用化学方程式表示为:
您最近一年使用:0次
解题方法
2 . 漂白粉与“84”消毒液是常用的高效含氯消毒剂。
(1)将氯气制成漂白粉的主要目的是______ 。
A.增强漂白和消毒作用
B.使氯气转化为较稳定物质,便于保存和运输
C.增加氯元素的质量分数,提高消毒效率
(2)漂白粉溶于水后,和空气中的二氧化碳作用,生成具有杀菌和漂白作用的次氯酸,反应的化学方程式为______ ,次氯酸电子式为______ 。
(3)漂白粉的有效成分是 ,下列说法中错误的是______。
,下列说法中错误的是______。
(4)“84”消毒液的制备原理为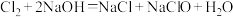 ,则“84”消毒液的有效成分是
,则“84”消毒液的有效成分是______ ,其中的化学键类型是______ 。
(5)下列物质中可以增强84消毒液的消毒能力的是______。
(6)如图是某品牌“84消毒液”的使用注意事项。
①注意事项4“易使有色衣物脱色”,是因为“84消毒液”具有______ 。
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的化学方程式______ 。
(1)将氯气制成漂白粉的主要目的是
A.增强漂白和消毒作用
B.使氯气转化为较稳定物质,便于保存和运输
C.增加氯元素的质量分数,提高消毒效率
(2)漂白粉溶于水后,和空气中的二氧化碳作用,生成具有杀菌和漂白作用的次氯酸,反应的化学方程式为
(3)漂白粉的有效成分是
 ,下列说法中错误的是______。
,下列说法中错误的是______。| A.漂白粉可以漂白棉、麻、纸张 |
| B.漂白粉可以用作游泳池消毒剂 |
C.将 通入冷的消石灰可制得漂白粉 通入冷的消石灰可制得漂白粉 |
| D.漂白粉很稳定,可敞口放置 |
(4)“84”消毒液的制备原理为
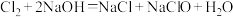 ,则“84”消毒液的有效成分是
,则“84”消毒液的有效成分是(5)下列物质中可以增强84消毒液的消毒能力的是______。
| A.氢氧化钠 | B.白醋 | C.纯碱 | D.食盐 |
(6)如图是某品牌“84消毒液”的使用注意事项。
| 注意事项 1、外用消毒液,勿口服; 2、现用现配,使用时注意戴手套防护; 3、不适用于钢和铝制品的消毒; 4、易使有色衣物脱色; 5、避光、阴凉处保存; 6、不可与酸性物质同时使用。 |
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 以下是有关铝的实验探究,请回答相关问题:
(1)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(2)向铝粉中添加少量 固体并充分混合,将其加热到1000℃时可与
固体并充分混合,将其加热到1000℃时可与 反应制备
反应制备 ,已知
,已知 溶液显酸性,下列说法正确的是___________。
溶液显酸性,下列说法正确的是___________。
(3)用打磨过的铝片进行如下实验,下列分析不合理的是___________。

(4)为探究铝片(未打磨)与 溶液的反应,实验如下:
溶液的反应,实验如下:
下列说法不正确的是___________。
(5)某铝土矿的主要成分为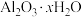 ,还含有
,还含有 和
和 杂质。称取
杂质。称取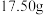 铝土矿样品,加入
铝土矿样品,加入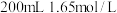 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
①该试样中 的物质的量为
的物质的量为___________ mol。
②样品中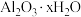 的x=
的x=___________ 。
(1)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:(2)向铝粉中添加少量
 固体并充分混合,将其加热到1000℃时可与
固体并充分混合,将其加热到1000℃时可与 反应制备
反应制备 ,已知
,已知 溶液显酸性,下列说法正确的是___________。
溶液显酸性,下列说法正确的是___________。A. 是一种金属材料 是一种金属材料 |
B. 与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
C.少量 能够破坏Al表面的 能够破坏Al表面的 薄膜 薄膜 |
D. 与足量盐酸反应的离子方程式为 与足量盐酸反应的离子方程式为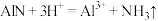 |

| A.①中铝片表面被浓硝酸氧化,生成了一层致密的氧化物薄膜,阻止了酸与内层金属的进一步反应 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
C.③中沉淀溶解的离子方程式是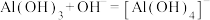 |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
 溶液的反应,实验如下:
溶液的反应,实验如下: |  | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色沉淀,产生大量气泡(经检验为 和 和 ) ) |
A. 溶液呈碱性 溶液呈碱性 |
B.对比Ⅰ、Ⅲ,推测 溶液能破坏铝表面的氧化膜 溶液能破坏铝表面的氧化膜 |
C.Ⅳ溶液中可能存在大量 |
D.推测出现白色浑浊的可能原因: |
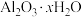 ,还含有
,还含有 和
和 杂质。称取
杂质。称取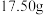 铝土矿样品,加入
铝土矿样品,加入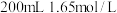 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。①该试样中
 的物质的量为
的物质的量为②样品中
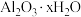 的x=
的x=
您最近一年使用:0次
名校
解题方法
4 . 某化学实验小组探究学习钠盐相关内容。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示 在水中溶解过程的微观状态示意图。
在水中溶解过程的微观状态示意图。
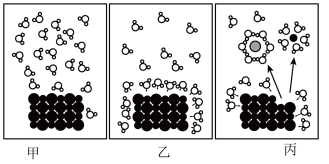
下列说法中,不正确的是______________ 。
a.干燥的 固体不导电,是由于其中不存在
固体不导电,是由于其中不存在 和
和
b.由上图可知,水分子在形成自由移动的 和
和 中起到了至关重要的作用
中起到了至关重要的作用
c. 溶液能导电,是由于在电流作用下,其可解离出自由移动的
溶液能导电,是由于在电流作用下,其可解离出自由移动的 和
和
d.加热至熔融状态的 也可以解离出自由移动的
也可以解离出自由移动的 和
和
(2)电解熔融 可制得单质钠,钠与水反应的化学方程式为
可制得单质钠,钠与水反应的化学方程式为____________________________________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有 、
、 ,
, 等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:
等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有: 溶液、
溶液、 溶液、
溶液、 溶液和盐酸。
溶液和盐酸。
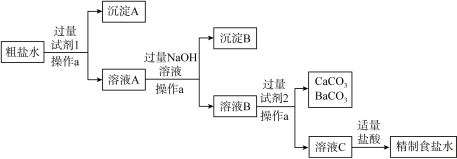
(3)操作 的名称是
的名称是_______________ ,试剂2是_______________ 。
(4)溶液 中除
中除 和
和 外,还存在的离子有
外,还存在的离子有_______________ 。
(5)沉淀 主要成分的化学式是
主要成分的化学式是________________ 。
(6)用离子方程式表示盐酸的作用_______________ 、_______________ 。
Ⅲ.探究碳酸氢钠的性质
(7)探究实验1:在锥形瓶内装入饱和 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 的分压,测得
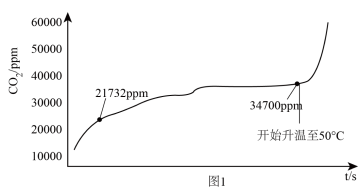
的分压,测得 的分压与温度的变化如图1所示。温度在50℃之前,
的分压与温度的变化如图1所示。温度在50℃之前, 的分压增大的主要原因是
的分压增大的主要原因是________________________ :温度升高到50℃之后, 的分压急剧增大的原因是
的分压急剧增大的原因是____________________________________ 。
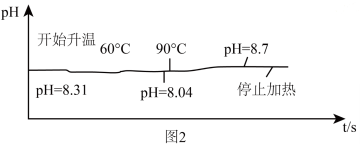
(8)探究实验2:将 为8.31的
为8.31的 溶液装入烧杯中,加入几滴酚酞溶液,加热,溶液
溶液装入烧杯中,加入几滴酚酞溶液,加热,溶液 变化与加热时间的关系如图2所示,冷却至室温,测得溶液
变化与加热时间的关系如图2所示,冷却至室温,测得溶液 为8.86。根据溶液
为8.86。根据溶液 的变化,请用文字描述加热过程中的溶液的颜色变化
的变化,请用文字描述加热过程中的溶液的颜色变化______________________________________________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示
 在水中溶解过程的微观状态示意图。
在水中溶解过程的微观状态示意图。
下列说法中,不正确的是
a.干燥的
 固体不导电,是由于其中不存在
固体不导电,是由于其中不存在 和
和
b.由上图可知,水分子在形成自由移动的
 和
和 中起到了至关重要的作用
中起到了至关重要的作用c.
 溶液能导电,是由于在电流作用下,其可解离出自由移动的
溶液能导电,是由于在电流作用下,其可解离出自由移动的 和
和
d.加热至熔融状态的
 也可以解离出自由移动的
也可以解离出自由移动的 和
和
(2)电解熔融
 可制得单质钠,钠与水反应的化学方程式为
可制得单质钠,钠与水反应的化学方程式为Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有
 、
、 ,
, 等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:
等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有: 溶液、
溶液、 溶液、
溶液、 溶液和盐酸。
溶液和盐酸。
(3)操作
 的名称是
的名称是(4)溶液
 中除
中除 和
和 外,还存在的离子有
外,还存在的离子有(5)沉淀
 主要成分的化学式是
主要成分的化学式是(6)用离子方程式表示盐酸的作用
Ⅲ.探究碳酸氢钠的性质
(7)探究实验1:在锥形瓶内装入饱和
 溶液,用
溶液,用 传感器测定密闭装置中
传感器测定密闭装置中 的分压,测得
的分压,测得 的分压与温度的变化如图1所示。温度在50℃之前,
的分压与温度的变化如图1所示。温度在50℃之前, 的分压增大的主要原因是
的分压增大的主要原因是 的分压急剧增大的原因是
的分压急剧增大的原因是
(8)探究实验2:将
 为8.31的
为8.31的 溶液装入烧杯中,加入几滴酚酞溶液,加热,溶液
溶液装入烧杯中,加入几滴酚酞溶液,加热,溶液 变化与加热时间的关系如图2所示,冷却至室温,测得溶液
变化与加热时间的关系如图2所示,冷却至室温,测得溶液 为8.86。根据溶液
为8.86。根据溶液 的变化,请用文字描述加热过程中的溶液的颜色变化
的变化,请用文字描述加热过程中的溶液的颜色变化
您最近一年使用:0次
名校
5 . 用含铬不锈钢废渣(含 、
、 、
、 、
、 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:

回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是___________ 。
(2) 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(3)“水浸”时,碱熔渣中的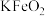 强烈水解生成的难溶物为
强烈水解生成的难溶物为___________ (填化学式);
(4)常温下“酸化”时,pH不宜过低的原因是___________ ;
(5)“还原”时,发生反应的离子方程式为___________ 。
(6)由 制取铬绿的方法是
制取铬绿的方法是___________ 。
 、
、 、
、 、
、 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是
(2)
 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为(3)“水浸”时,碱熔渣中的
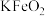 强烈水解生成的难溶物为
强烈水解生成的难溶物为(4)常温下“酸化”时,pH不宜过低的原因是
(5)“还原”时,发生反应的离子方程式为
(6)由
 制取铬绿的方法是
制取铬绿的方法是
您最近一年使用:0次
2023-10-26更新
|
92次组卷
|
2卷引用:河北省秦皇岛市青龙满族自治县2校联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 某钴矿石的主要成分有CoO、 、MnO、
、MnO、 、MgO和
、MgO和 等。由该矿石粉制备
等。由该矿石粉制备 固体的方法如下(部分催化剂已略)。
固体的方法如下(部分催化剂已略)。
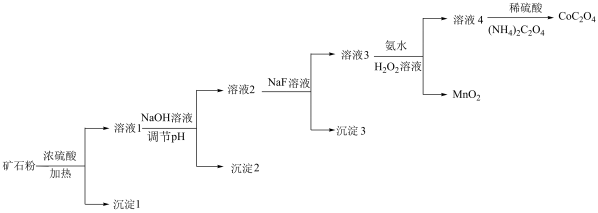
已知:金属离子沉淀的pH:
(1) 溶于浓硫酸,生成
溶于浓硫酸,生成 和一种可使带火星的木条复燃的气体,该气体是
和一种可使带火星的木条复燃的气体,该气体是___________ 。
(2)向溶液1中加入NaOH溶液将pH调至3,目的是___________ 。
(3)向溶液2中加入NaF溶液,去除的离子是___________ 。
(4)向溶液3中加入氨水和过氧化氢溶液,将 转化为
转化为 。补充完整下列离子方程式:
。补充完整下列离子方程式:_______
___________ +___________
+___________ ___________
___________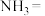 ___________
___________ ___________
___________
(5)溶液4中,若将1 mol 全部转化为
全部转化为 沉淀,需要消耗
沉淀,需要消耗
___________ mol。
(6)关于上述流程,下列说法正确的是___________ (填序号)。
a.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的
b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
 、MnO、
、MnO、 、MgO和
、MgO和 等。由该矿石粉制备
等。由该矿石粉制备 固体的方法如下(部分催化剂已略)。
固体的方法如下(部分催化剂已略)。
已知:金属离子沉淀的pH:
 |  |  |  |  | |
| 开始沉淀时 | 1.5 | 6.3 | 8.9 | 8.2 | 7.4 |
| 完全沉淀时 | 2.8 | 8.3 | 10.9 | 10.2 | 9.4 |
 溶于浓硫酸,生成
溶于浓硫酸,生成 和一种可使带火星的木条复燃的气体,该气体是
和一种可使带火星的木条复燃的气体,该气体是(2)向溶液1中加入NaOH溶液将pH调至3,目的是
(3)向溶液2中加入NaF溶液,去除的离子是
(4)向溶液3中加入氨水和过氧化氢溶液,将
 转化为
转化为 。补充完整下列离子方程式:
。补充完整下列离子方程式:___________
 +___________
+___________ ___________
___________ ___________
___________ ___________
___________(5)溶液4中,若将1 mol
 全部转化为
全部转化为 沉淀,需要消耗
沉淀,需要消耗
(6)关于上述流程,下列说法正确的是
a.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的

b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
您最近一年使用:0次
2023-10-15更新
|
166次组卷
|
7卷引用:北京一零一中2021-2022学年高一下学期期末考试(等级考)化学试题
北京一零一中2021-2022学年高一下学期期末考试(等级考)化学试题北京市西城区2021届高三上学期期末考试化学试题(已下线)大题01 化学工艺流程题(一)-【考前抓大题】备战2021年高考化学(全国通用)(已下线)北京市第四中学2021-2022学年高三上学期期中考试化学试题北京市首都师范大学附属中学2023-2024学年高三上学期10月月考化学试题北京市清华大学附属中学2023-2024学年高三上学期10月统练(四)化学试题北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
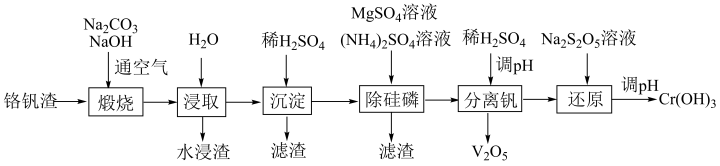
7 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示: 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ (写化学式)。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ (写化学式)。
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,还原Cr2O ,写出该反应的离子方程式为
,写出该反应的离子方程式为___________ 。
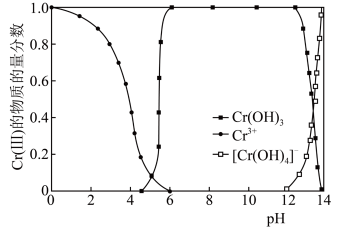
(5)已知:Cr(III)的存在形态的物质的量分数随溶液pH的分布如图所示___________ ,低温烘干,得到高纯Cr(OH)3晶体。【实验中须使用的试剂:2mol/LNaOH溶液、0.1mol/L AgNO3溶液、0.1mol/LHNO3溶液、蒸馏水】
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,还原Cr2O
 ,写出该反应的离子方程式为
,写出该反应的离子方程式为(5)已知:Cr(III)的存在形态的物质的量分数随溶液pH的分布如图所示
您最近一年使用:0次
解题方法
8 . 氨水和 均可用于脱除烟气中
均可用于脱除烟气中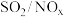 。
。
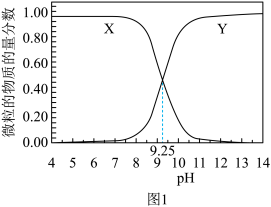
(1)以氨水作为吸收剂吸收 。25℃时,氨水中
。25℃时,氨水中 、
、 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
①氨水与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②25℃时,氨水的电离常数
___________ 。(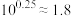 )
)
(2)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
① 溶液的水解平衡常数
溶液的水解平衡常数
___________ 。
②现有25℃时等浓度的5种溶液:A. ;B.
;B. ;C.
;C. ;D.
;D. ; E.
; E. ;F.(NH4)2CO3,这6种溶液中
;F.(NH4)2CO3,这6种溶液中 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:___________ (填字母)。
(3) 可对烟气中NOx、
可对烟气中NOx、 进行协同脱除。
进行协同脱除。
①电解 溶液制备
溶液制备 气体的装置如图2所示。
气体的装置如图2所示。 通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为___________ 。

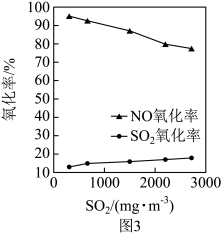
②保持其他条件不变,调节烟气中SO2初始浓度,将烟气按一定流速通入反应器与 反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是___________ 。
 均可用于脱除烟气中
均可用于脱除烟气中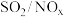 。
。(1)以氨水作为吸收剂吸收
 。25℃时,氨水中
。25℃时,氨水中 、
、 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
①氨水与
 反应生成
反应生成 的离子方程式为
的离子方程式为②25℃时,氨水的电离常数

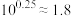 )
)(2)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
| 化学式 |  |  | HSCN |
| 电离平衡常数 |  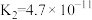 | 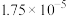 | 0.13 |
 溶液的水解平衡常数
溶液的水解平衡常数
②现有25℃时等浓度的5种溶液:A.
 ;B.
;B. ;C.
;C. ;D.
;D. ; E.
; E. ;F.(NH4)2CO3,这6种溶液中
;F.(NH4)2CO3,这6种溶液中 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:(3)
 可对烟气中NOx、
可对烟气中NOx、 进行协同脱除。
进行协同脱除。①电解
 溶液制备
溶液制备 气体的装置如图2所示。
气体的装置如图2所示。 通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
通过阳离子交换膜向阴极室迁移,电解时阴极的电极反应为
②保持其他条件不变,调节烟气中SO2初始浓度,将烟气按一定流速通入反应器与
 反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
反应,测得NO、SO2氧化率随SO2初始浓度的变化如图3所示。SO2氧化率始终低于NO氧化率的原因可能是
您最近一年使用:0次
名校
解题方法
9 . 实验小组探究酸对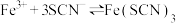 平衡的影响。将0.005mol/L
平衡的影响。将0.005mol/L 溶液(接近无色)和0.01mol/L
溶液(接近无色)和0.01mol/L 溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
(1) 水解显酸性的原因是
水解显酸性的原因是___________ (用方程式表示)。
(2)甲同学认为加入酸后,会使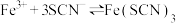 体系中
体系中___________ 浓度改变,导致该平衡正向移动,溶液颜色加深。
【设计并实施实验】
【查阅资料】Fe3+和 、
、 均能发生络合反应:
均能发生络合反应: (黄色);
(黄色); (无色)。
(无色)。
(3) 离子的空间构型为
离子的空间构型为___________ ,与 配位的原子是
配位的原子是___________ 。
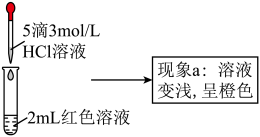
实验Ⅰ.探究现象a中溶液颜色变化的原因
(4)实验(1)的目的是___________ 。
(5)根据实验(1)和实验(2)的结果,从平衡移动角度解释现象a:___________ 。
实验Ⅱ.探究现象b中溶液呈浅黄色的原因
(6)结合实验(3)可推测现象b中使溶液呈浅黄色的微粒可能有两种,分别是___________ 。
(7)乙同学进一步补充了实验(4),确证了现象b中使溶液呈浅黄色的微粒只是(5)中的一种,请将实验④的操作及现象补充完整:___________ 。
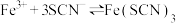 平衡的影响。将0.005mol/L
平衡的影响。将0.005mol/L 溶液(接近无色)和0.01mol/L
溶液(接近无色)和0.01mol/L 溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。(1)
 水解显酸性的原因是
水解显酸性的原因是(2)甲同学认为加入酸后,会使
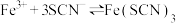 体系中
体系中【设计并实施实验】
 |  |
 、
、 均能发生络合反应:
均能发生络合反应: (黄色);
(黄色); (无色)。
(无色)。(3)
 离子的空间构型为
离子的空间构型为 配位的原子是
配位的原子是实验Ⅰ.探究现象a中溶液颜色变化的原因
| 编号 | 操作 | 现象 |
| ① | 向2mL红色溶液中滴加5滴水 | 溶液颜色无明显变化 |
| ② | 向2mL红色溶液中滴加5滴3mol/L 溶液 溶液 | 溶液颜色变浅,呈橙色 |
(5)根据实验(1)和实验(2)的结果,从平衡移动角度解释现象a:
实验Ⅱ.探究现象b中溶液呈浅黄色的原因
| 编号 | 操作 | 现象 |
| ③ | 取1mL 0.0025mol/L 溶液(无色),加入1mL 0.01mol/L 溶液(无色),加入1mL 0.01mol/L 溶液,再加入5滴1.5mol/L 溶液,再加入5滴1.5mol/L 溶液 溶液 | 溶液先变红,加硫酸后变为浅黄色 |
| ④ | 取1mL 0.005mol/L 溶液 溶液 | ___________ |
(7)乙同学进一步补充了实验(4),确证了现象b中使溶液呈浅黄色的微粒只是(5)中的一种,请将实验④的操作及现象补充完整:
您最近一年使用:0次
2023-05-01更新
|
137次组卷
|
2卷引用:北京市第八十中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
10 . 某小组同学探究盐对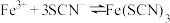 平衡体系的影响。
平衡体系的影响。
实验Ⅰ:探究KCl对 和
和 平衡体系的影响
平衡体系的影响
将等体积、低浓度的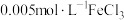 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和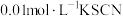 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
② 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。
(1)稀盐酸酸化 溶液的目的是
溶液的目的是___________ 。采用浓度较低的 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免___________ (填离子符号)的颜色对实验干扰。
(2)从实验结果来看,KCl溶液确实对 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向___________ (填“正”或“逆”)反应方向移动。
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。
(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
①上述实验可证明盐效应影响了 和
和 平衡体系的是
平衡体系的是___________ (填字母序号)。
a.1和2 b.1和3 c.1和4
②选择实验___________ (填序号)可得出结论: 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。
(4)取等体积的溶液a继续进行实验,结果如下表。
上述实验可证明副反应影响了 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:___________ 。
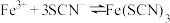 平衡体系的影响。
平衡体系的影响。实验Ⅰ:探究KCl对
 和
和 平衡体系的影响
平衡体系的影响将等体积、低浓度的
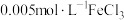 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和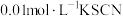 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②
 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。(1)稀盐酸酸化
 溶液的目的是
溶液的目的是 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免(2)从实验结果来看,KCl溶液确实对
 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使
 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。原因2:溶液中存在副反应
 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
| 序号 | 加入少量盐 | 溶液颜色 |
| 1 | 无 | 红色 |
| 2 | KCl | 变浅 |
| 3 |  | 略变浅 |
| 4 | NaCl | 变浅程度较大 |
 和
和 平衡体系的是
平衡体系的是a.1和2 b.1和3 c.1和4
②选择实验
 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。(4)取等体积的溶液a继续进行实验,结果如下表。
| 序号 | 加入溶液 | 溶液颜色 |
| 5 | 1mL浓盐酸 | 明显变浅,溶液偏黄 |
| 6 | 1mL去离子水 | 略变浅 |
 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:
您最近一年使用:0次
2023-04-20更新
|
117次组卷
|
4卷引用:江西省五校2022-2023学年高一下学期直升班联考化学试题



