1 . 回答下列问题:
(1)常温下,将0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是_______。
(2)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw=_______ mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH=_______ 。
(3)常温下在20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。

回答下列问题:
①在同一溶液中,H2CO3、HCO 、CO
、CO
_______ (填“能”或“不能”)大量共存。
②已知在25 ℃时,CO 水解反应的平衡常数Kh=
水解反应的平衡常数Kh= =2×10-4,当溶液中c(HCO
=2×10-4,当溶液中c(HCO ):c-(CO
):c-(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=_______ 。
(1)常温下,将0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是_______。
| A.c(HA)<c(A-) | B.c(HA)一定大于0.1 mol·L-1 |
| C.c(Na+)=c(HA)+c(A-) | D.2c(OH-)=2c(H+)+[c(HA)-c(A-)] |
①该温度下水的离子积常数Kw=
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH=
(3)常温下在20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。

回答下列问题:
①在同一溶液中,H2CO3、HCO
 、CO
、CO
②已知在25 ℃时,CO
 水解反应的平衡常数Kh=
水解反应的平衡常数Kh= =2×10-4,当溶液中c(HCO
=2×10-4,当溶液中c(HCO ):c-(CO
):c-(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=
您最近一年使用:0次
2 . NA表示阿伏加德罗常数的数值,下列说法正确的是
①3.9g苯与足量的H2反应时,参与反应的碳碳双键数为0.15NA
②3.1g氧化钠和3.9g过氧化钠的混合物中含有的阴离子总数为0.1NA
③1.8g14CH4和水蒸气(H218O)的混合气体中含电子数目为NA
④常温下1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液所含NH 的数目相同
的数目相同
⑤常温下,4.6gNO2和N2O4组成的混合气体中所含原子总数为0.3NA
⑥1molSiO2晶体中含有非极性共价键数目为2NA
⑦将1molCl2通入足量水中,溶液中HClO、Cl—、C1O—粒子数之和为2NA
⑧高温下,16.8gFe与足量水蒸气完全反应转移电子数为0.8NA
①3.9g苯与足量的H2反应时,参与反应的碳碳双键数为0.15NA
②3.1g氧化钠和3.9g过氧化钠的混合物中含有的阴离子总数为0.1NA
③1.8g14CH4和水蒸气(H218O)的混合气体中含电子数目为NA
④常温下1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液所含NH
 的数目相同
的数目相同⑤常温下,4.6gNO2和N2O4组成的混合气体中所含原子总数为0.3NA
⑥1molSiO2晶体中含有非极性共价键数目为2NA
⑦将1molCl2通入足量水中,溶液中HClO、Cl—、C1O—粒子数之和为2NA
⑧高温下,16.8gFe与足量水蒸气完全反应转移电子数为0.8NA
| A.①②⑥ | B.②⑤⑧ | C.②③⑦ | D.③⑤⑧ |
您最近一年使用:0次
3 . 下列说法错误的是
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c( )+c(
)+c( )
)
③在0.1mol/L氨水中滴加0.lmol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol/L
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c( )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
⑥25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
①NaHCO3溶液加水稀释,
 的比值保持增大
的比值保持增大②浓度均为0.1mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(
 )+c(
)+c( )
)③在0.1mol/L氨水中滴加0.lmol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol/L
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(
 )均增大
)均增大⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
⑥25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
| A.②⑤ | B.②④ | C.①③ | D.①④ |
您最近一年使用:0次
解题方法
4 . 学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
(1)常温下,某硫化钠溶液中滴入酚酞,溶液呈红色,则该溶液呈___________ 性,原因是___________ ;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于___________ ;
(3)已知在H2S溶液中存在下列平衡: H2S H++HS-。
H++HS-。
①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向___________ 移动,(填“左”或“右”),c(H+)___________ 。(填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向___________ 移动,(填“左”或“右”)c(S2—)___________ 。(填“增大”、“减小”或“不变”)
(1)常温下,某硫化钠溶液中滴入酚酞,溶液呈红色,则该溶液呈
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于
(3)已知在H2S溶液中存在下列平衡: H2S
 H++HS-。
H++HS-。①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向
②向H2S溶液中加入NaHS固体时,电离平衡向
您最近一年使用:0次
解题方法
5 . X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16,在适当条件下三种单质两两直接化合,可发生如图所示变化。已知一个B分子中含有Z元素的原子个数比C分子中的Z元素的原子个数少一个。请回答下列问题:
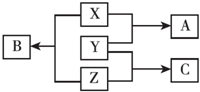
(1)Y元素在周期表中的位置为_______ 。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质名称是_______ 负极电极反应式为_______ 。
(3)X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W溶液吸收生成一种盐。该盐水溶液pH_______ 7(填“大于”、“小于”或“等于”)
(4)试写出实验室制取C的化学方程式_______ 。

(1)Y元素在周期表中的位置为
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质名称是
(3)X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W溶液吸收生成一种盐。该盐水溶液pH
(4)试写出实验室制取C的化学方程式
您最近一年使用:0次
解题方法
6 . 室温下,将两种浓度均为0.1 mol/L的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
A.NaHCO3-Na2CO3混合溶液(pH=10.30):c(Na+)>c(OH-)>c( )>c( )>c( ) ) |
B.氨水-NH4Cl混合溶液(pH=9.25):c( )+c(H+)=c(NH3∙H2O)+c(OH-) )+c(H+)=c(NH3∙H2O)+c(OH-) |
| C.CH3COOH-CH3COONa混合溶液(pH=4.76):c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+) |
D.H2C2O4-NaHC2O4混合溶液(pH=1.68,H2C2O4为二元弱酸):c(H+)+c(H2C2O4)=c(Na+)+ c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
7 . 按要求填空:
I.
(1)AlCl3的水溶液pH_______ 7 ( 填>、=、<),其原因为_______ (用离子方程式表示),将其溶液加热蒸干并灼烧最终得到的物质是_______ (填化学式)。
(2)常温下,Cr(OH)3的溶度积Ksp= c(Cr3+)∙c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_______ 。
(3)物质的量浓度相同的三种溶液:①(NH4)2SO4 ②氨水 ③NH4HSO4,c( )大小顺序是
)大小顺序是_______ (用序号表示)
(4)常温下两种溶液:a.pH=4的NH4Cl b.pH=4的盐酸,其中水电离出的c(H+)之比为_______ 。
II.室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol/LHA溶液中逐滴加入0.1000mol/L的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
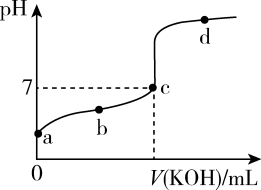
(5)a、b、c、d四点中水的电离程度最大的是_______ 点,滴定过程中宜选用_______ 作指示剂,滴定终点在_______  填“c点以上”或“c点以下”
填“c点以上”或“c点以下” 。
。
(6)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_______。
(7)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_______ mol/L。 保留
保留 位有效数字
位有效数字
I.
(1)AlCl3的水溶液pH
(2)常温下,Cr(OH)3的溶度积Ksp= c(Cr3+)∙c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
(3)物质的量浓度相同的三种溶液:①(NH4)2SO4 ②氨水 ③NH4HSO4,c(
 )大小顺序是
)大小顺序是(4)常温下两种溶液:a.pH=4的NH4Cl b.pH=4的盐酸,其中水电离出的c(H+)之比为
II.室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol/LHA溶液中逐滴加入0.1000mol/L的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

(5)a、b、c、d四点中水的电离程度最大的是
 填“c点以上”或“c点以下”
填“c点以上”或“c点以下” 。
。(6)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_______。
| A.滴定前碱式滴定管未用标准KOH溶液润洗 |
| B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定 |
| C.滴定过程中,溶液出现变色后,立即停止滴定 |
| D.滴定结束后,仰视液面,读取KOH溶液体积 |
 保留
保留 位有效数字
位有效数字
| 实验序号 | KOH溶液体积/mL | 待测HA溶液体积/mL |
 | 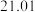 |  |
 | 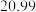 |  |
 |  |  |
您最近一年使用:0次
8 . 现有室温下溶质浓度均为 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)在④溶液中,各离子浓度大小顺序为:_______
(2)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=_______ (已知 )
)
(3)pH=5的硫酸铵溶液与硫酸溶液,由水电离产生的c(H+)=_______
(4)若将③溶液和⑥溶液等体积混合,溶液呈碱性,原因是_______ (用离子反应方程式表示)
(5)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是_______
 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:(1)在④溶液中,各离子浓度大小顺序为:
(2)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
 )
)(3)pH=5的硫酸铵溶液与硫酸溶液,由水电离产生的c(H+)=
(4)若将③溶液和⑥溶液等体积混合,溶液呈碱性,原因是
(5)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是_______
A.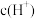 | B.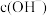 | C.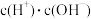 | D. |
您最近一年使用:0次
名校
解题方法
9 . 常温下,下列说法正确的是
A.1mol/L和0.01mol/L的氨水中水电离出的 浓度:前者是后者的100倍 浓度:前者是后者的100倍 |
B.pH相等的 溶液和NaOH溶液: 溶液和NaOH溶液: |
| C.同浓度的HF和HCN,Ka(HF) > Ka( HCN),则NaF溶液的pH比NaCN溶液的大 |
D.在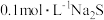 溶液中: 溶液中: |
您最近一年使用:0次
2022-04-09更新
|
62次组卷
|
2卷引用:江西省山江湖协作体2021-2022学年高二上学期联考(统招班)化学试题
10 . 设NA为阿伏加德罗常数的数值,下列有关说法正确的是
| A.1L 1 mol/L Na2S溶液中S2-的数目为NA |
| B.常温下,1L pH= 3的醋酸溶液中OH-的数目为10-11NA |
| C.常温下,1L 0.1 mol/L H2SO3溶液中H+的数目为0.2NA |
| D.常温下,0.1L pH=13的Ba(OH)2 溶液中OH-的数目为0.02NA |
您最近一年使用:0次



