名校
解题方法
1 . 常温下,已知Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是
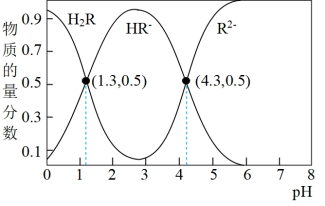

A.反应H2R+R2- 2HR-的平衡常数K=1000 2HR-的平衡常数K=1000 |
B.向Na2CO3溶液中加入少量H2R溶液,发生的反应是:CO +H2R=CO2↑+H2O+R2- +H2R=CO2↑+H2O+R2- |
| C.等体积、等浓度的NaOH溶液与H2R溶液混合后,溶液中:(R2-)<c(H2R) |
| D.在pH=4的溶液中:3c(R2-)>c(Na+)+c(H+)-c(OH-) |
您最近一年使用:0次
2021-05-23更新
|
585次组卷
|
4卷引用:重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题
重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题重庆市长寿中学2021届高三5月考前模拟化学试题(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 已知:25℃时,Ka(CH3COOH)=1.7×10-5,Kb(NH3·H2O)=1.7×10-5。用0.01 mol/L的CH3COOH溶液滴定20 mL由浓度均为0.01 mol/L的NaOH溶液和氨水组成的混合溶液,溶液的相对导电能力随加入CH3COOH溶液体积的变化趋势如图所示。下列叙述错误的是
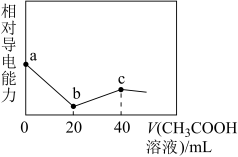
A.a点时混合溶液中:c( )≈1.7×10-5 mol·L-1 )≈1.7×10-5 mol·L-1 |
B.b点时混合溶液中:c(CH3COOH)<c( ) ) |
C.c点时混合溶液中:c(CH3COO- )+c(CH3COOH)=c( )+c(NH3·H2O)+c(Na+) )+c(NH3·H2O)+c(Na+) |
| D.c点时混合溶液中:pH=7 |
您最近一年使用:0次
2021-05-13更新
|
966次组卷
|
11卷引用:2024届重庆市高三下学期二模考试化学试题
2024届重庆市高三下学期二模考试化学试题福建省莆田市2021届高三第三次质量检测化学试题辽宁省朝阳市2021届高三第三次模拟考试化学试题山东省泰安市与济南章丘区2021届高三5月联合模拟考试化学试题山西省2020-2021学年高二下学期5月考试化学试题湖南省长沙市明德中学2021届高三下学期第三次模拟考试化学试题湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练湖南省汨罗市第二中学2021-2022学年高三下学期4月月考化学试题广东省肇庆市百花中学2021届高三下学期5月模拟考试化学试题陕西省西安市5校联考2023-2024学年高二上学期1月期末化学试题
3 . 实验测得0.5mol·Lˉ1Na2SO3溶液、NaHCO3和CH3COONa的pH随温度变化如图所示。已知25℃电离平衡常数(Ka)
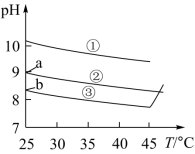
下列说法不正确 的是

| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| Ka | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.0×10-7 |
| A.25℃时,若Na2SO3浓度为0.1mol·Lˉ1,则溶液pH=10 (忽略二级水解和H2O的电离) |
| B.③曲线45℃时的变化,主要原因是NaHCO3发生分解生成Na2CO3 |
| C.由图表可知,①曲线为CH3COONa溶液 |
| D.a、b两点的pH前者大于后者,主要原因是酸式盐在水溶液中既发生水解又发生电离 |
您最近一年使用:0次
2021-04-27更新
|
757次组卷
|
6卷引用:选择题11-14
(已下线)选择题11-14浙江省温州市2021届高三3月适应性测试(二模)化学试题(已下线)2021年高考化学押题预测卷(浙江卷)(02)(含考试版、答题卡、参考答案、全解全析)(已下线)小题21 盐类水解、微粒浓度大小比较及滴定曲线、分布系数曲线的分析——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押山东卷第15题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(山东卷)(已下线)考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)
名校
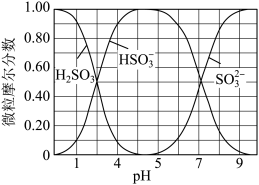
4 . 25 ℃时,在 c(H2SO3) + c(HSO )+ c(SO
)+ c(SO )=1.63mol/L 的溶液中,三种粒子的摩尔分数(α)随溶液pH 变化的关系如图所示。下列说法不正确的是
)=1.63mol/L 的溶液中,三种粒子的摩尔分数(α)随溶液pH 变化的关系如图所示。下列说法不正确的是
 )+ c(SO
)+ c(SO )=1.63mol/L 的溶液中,三种粒子的摩尔分数(α)随溶液pH 变化的关系如图所示。下列说法不正确的是
)=1.63mol/L 的溶液中,三种粒子的摩尔分数(α)随溶液pH 变化的关系如图所示。下列说法不正确的是
| A.25 ℃时,NaHSO3溶液显酸性 |
B.pH=4 时,c(H2SO3)=c(SO )=0 )=0 |
C.pH>1 时,c(HSO )+ 2c(SO )+ 2c(SO )+ c(OH-) > c(H+) )+ c(OH-) > c(H+) |
D.25 ℃时,向1.63mol/L的H2SO3溶液中加Ca(OH)2固体至pH=7,c(SO )< 0.815mol/L(忽略溶液体积变化) )< 0.815mol/L(忽略溶液体积变化) |
您最近一年使用:0次
13-14高三·浙江嘉兴·阶段练习
名校
解题方法
5 . 已知:常温下浓度为0.1mol•L-1的下列溶液的pH如表:
下列有关说法正确的是
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF |
B.若将CO2通入0.1mol•L-1Na2CO3溶液中至溶液中性,则溶液2c(CO )+c(HCO )+c(HCO )=0.1mol•L-1 )=0.1mol•L-1 |
C.根据上表,水解方程式ClO-+H2O HClO+OH-的水解常数K≈10-7.6 HClO+OH-的水解常数K≈10-7.6 |
| D.向上述NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>c(H+)> c(HClO)>c(OH-) |
您最近一年使用:0次
2021-03-20更新
|
476次组卷
|
14卷引用:2015届重庆一中高高三下期第三次月考化学试卷
2015届重庆一中高高三下期第三次月考化学试卷(已下线)2014届浙江省嘉兴市高三教学测试(一)理综化学试卷2015届山东省沂水县一中高三上学期12月月考化学试卷2015届浙江省丽水中学高三第二次模拟理综化学试卷2015届山东省枣庄市八中高三4月模拟考试化学试卷2016届黑龙江省大庆实验中学高三考训练四理综化学试卷江西省临川第二中学2018届高三上学期第四次月考(期中)化学试题安徽省合肥二中2019-2020学年度高三上学期第一次段考化学试题江西省南昌市莲塘第一中学2019-2020学年高二上学期期末质量检测化学试题广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题辽宁省滨海实验中学2019-2020学年高二上学期期末化学试题河南省延津第一高级中学2021-2022学年高二上学期第五次考试化学试题广东省新南方联盟2024届高三下学期4月联考化学试题
名校
6 . 常温下,现有0.1mol•L-1 NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时,各微粒浓度占总微粒浓度之和的分数)与pH的关系如图所示:
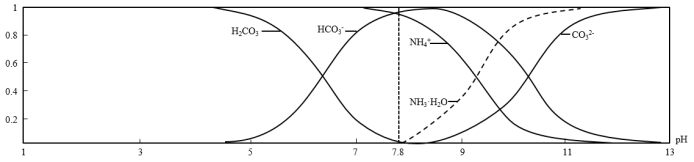
下列说法不正确的是

下列说法不正确的是
| A.分析可知,常温下Kb(NH3•H2O)>Ka1(H2CO3) |
B.0.1 mol•L-1 NH4HCO3溶液中存在:c(NH3•H2O)=c(H2CO3)+c(CO ) ) |
C.当溶液的pH=9时,溶液中存在:c(HCO )>c(NH )>c(NH )>c(NH3•H2O)>c(CO )>c(NH3•H2O)>c(CO ) ) |
D.向pH=7.8的上述溶液中逐滴滴加氢氧化钠溶液时,NH 和HCO 和HCO 浓度逐渐减小 浓度逐渐减小 |
您最近一年使用:0次
2021-03-11更新
|
256次组卷
|
4卷引用:重庆市重庆实验外国语学校2021-2022学年高二上学期1月月考化学试题
名校
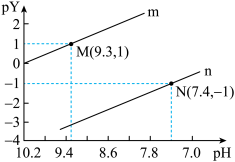
7 . 常温下,向一定浓度的Na2R溶液中滴入稀硫酸,粒子浓度与混合溶液pH的变化关系如下图所示。已知:H2R是二元弱酸,Y表示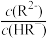 或
或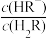 ,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是
,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是
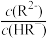 或
或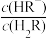 ,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是
,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是
A.曲线m表示p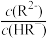 与混合溶液pH的变化关系 与混合溶液pH的变化关系 |
B.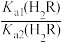 =103.9 =103.9 |
| C.NaHR溶液中存在:c(Na+)<c(HR-)+2c(R2-) |
D.滴加稀硫酸的过程中,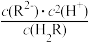 保持不变 保持不变 |
您最近一年使用:0次
2021-03-07更新
|
1808次组卷
|
11卷引用:重庆市强基联合体2021届高三下学期质量检测化学试题
重庆市强基联合体2021届高三下学期质量检测化学试题河南省鹤壁市高中2020-2021学年高二下学期第三次段考化学试题河南省洛阳市2021届高三5月第三次统一考试理综化学试题(已下线)2021年高考化学押题预测卷(广东卷)(02)(已下线)【浙江新东方】高中化学20210621-010【2021】【高三下】(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)二轮拔高卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)专题十三水溶液中的离子平衡(已下线)专题10 溶液中离子浓度的关系(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练
名校
8 . 常温下,在10mL0.1mol·L-1Na2CO3溶液中逐滴加入0.1mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示,下列说法不正确的是
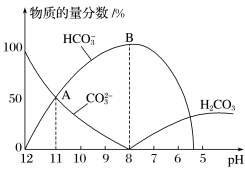

| A.溶液的pH为7时,溶液的总体积大于20mL |
B.在B点所示的溶液中:c(Na+)+c(H+)=2c( )+c( )+c( )+c(OH-)+c(Cl-) )+c(OH-)+c(Cl-) |
C.在A点所示的溶液中:c(Na+)=c( )=c( )=c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
D.已知 水解常数为2×10-4,当溶液中c( 水解常数为2×10-4,当溶液中c( )=2c( )=2c( )时,溶液的pH=10 )时,溶液的pH=10 |
您最近一年使用:0次
2020-10-29更新
|
350次组卷
|
5卷引用:重庆市万州第二高级中学2020-2021学年高二上学期10月月考化学试题
重庆市万州第二高级中学2020-2021学年高二上学期10月月考化学试题吉林省长春市第一中学2021届高三上学期期末考试化学试题宁夏固原市第一中学2020-2021学年高三下学期第一次模拟考试理综化学试题贵州省龙里县九八五实验学校2020届高三上学期1月月考化学试题(已下线)课时44 滴定曲线、分布系数曲线的分析-2022年高考化学一轮复习小题多维练(全国通用)
名校
9 . 室温下,向某Na2CO3和NaHCO3的混合溶液中逐滴加入BaCl2溶液,溶液中lgc(Ba2+)与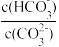 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
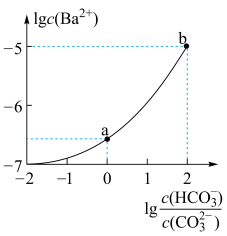
(已知:H2CO3的Ka1、Ka2分别为4.2×10-7、5.6×10-11)
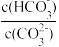 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是 
(已知:H2CO3的Ka1、Ka2分别为4.2×10-7、5.6×10-11)
| A.a对应溶液的pH小于b |
| B.b对应溶液的c(H+)=4.2×10-7mol·L-1 |
C.a→b 对应的溶液中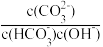 减小 减小 |
D.a 对应的溶液中一定存在:2c(Ba2+)+c(Na+)+c(H+)=3c( )+c(Cl-)+c(OH-) )+c(Cl-)+c(OH-) |
您最近一年使用:0次
2020-10-21更新
|
693次组卷
|
7卷引用:重庆市主城区2021届高考适应性(一)化学试题
名校
10 . 二甲胺[(CH3)2NH]在水中电离与氨相似, 。常温下,用0.100mol/L的HCl分别滴定20. 00mL浓度均为0.100mol/L的NaOH和二甲胺溶液,测得滴定过程中溶液的电导率变化曲线如图所示。下列说法正确的是
。常温下,用0.100mol/L的HCl分别滴定20. 00mL浓度均为0.100mol/L的NaOH和二甲胺溶液,测得滴定过程中溶液的电导率变化曲线如图所示。下列说法正确的是
 。常温下,用0.100mol/L的HCl分别滴定20. 00mL浓度均为0.100mol/L的NaOH和二甲胺溶液,测得滴定过程中溶液的电导率变化曲线如图所示。下列说法正确的是
。常温下,用0.100mol/L的HCl分别滴定20. 00mL浓度均为0.100mol/L的NaOH和二甲胺溶液,测得滴定过程中溶液的电导率变化曲线如图所示。下列说法正确的是
A.b点溶液:  |
B.d点溶液: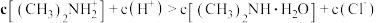 |
C.e点溶液中: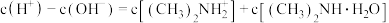 |
D.a、b 、c、d点对应的溶液中,水的电离程度: |
您最近一年使用:0次
2020-09-06更新
|
944次组卷
|
5卷引用:重庆市巴蜀中学2022-2023学年高二上学期期中考试化学试题



